布地格福吸入气雾剂(倍择瑞®令畅®)于2019年12月获我国国家药品监督管理局(NMPA)正式批准,用于慢阻肺患者的维持治疗,并且获批为2.3类创新药物,这就意味着,在稳定期治疗中可以通过使用创新共悬浮给药技术单装置给予三联制剂,标志着中国慢阻肺患者吸入治疗新时代赫然而来。
今日凌晨2:00点,布地格福的重磅III期临床研究于新英格兰医学杂志发布,进一步证明了布地格福对比双联吸入药物在中至极重度高风险慢阻肺患者中的多个方面的获益。

研究设计 [1-2]
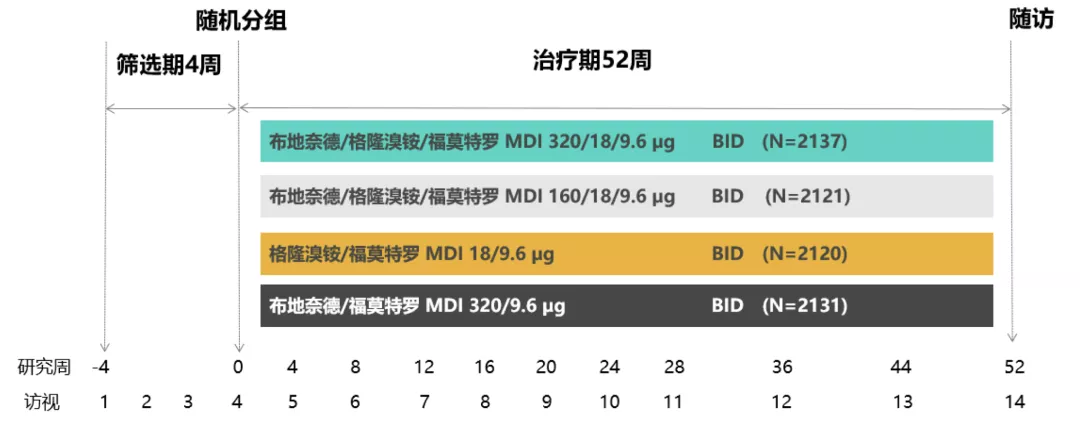
> 纳入患者:既往有频繁急性加重史的中至极重度慢阻肺患者
> 主要终点:中/重度急性加重发生率
ETHOS研究是一项随机,双盲,平行组,多中心的全球性研究,纳入了8572例中至极重度的慢阻肺患者,观察布地格福的疗效和安全性。因为其主要终点是观察患者中重度急性加重的发生情况,研究时间长达52周,并且在入组时,要求患者既往有频繁急性加重史,因此其结果可以更好地体现布地格福对于急性加重终点的获益情况。至此,布地格福在不同特点的慢阻肺患者群中证据更为完整。
ETHOS研究不仅是一个以急性加重获益为终点研究,且ETHOS还首次探讨了不同剂量的ICS三联治疗在慢阻肺患者中的获益情况。在研究设计中,设置了布地格福320作为研究药物,布地格福160、格隆溴铵/福莫特罗及布地奈德/福莫特罗作为对照组,其创新性点是慢阻肺治疗领域的一大亮点。
研究结果 [1-2]
> 布地格福320显著降低急性加重发生率
> 布地格福320显著降低全因死亡风险
ETHOS的研究结果显示
> 与LAMA/LABA相比,布地格福320显著降低24%中/重度急性加重发生率;
> 与ICS/LABA相比,布地格福320显著降低13%中/重度急性加重发生率
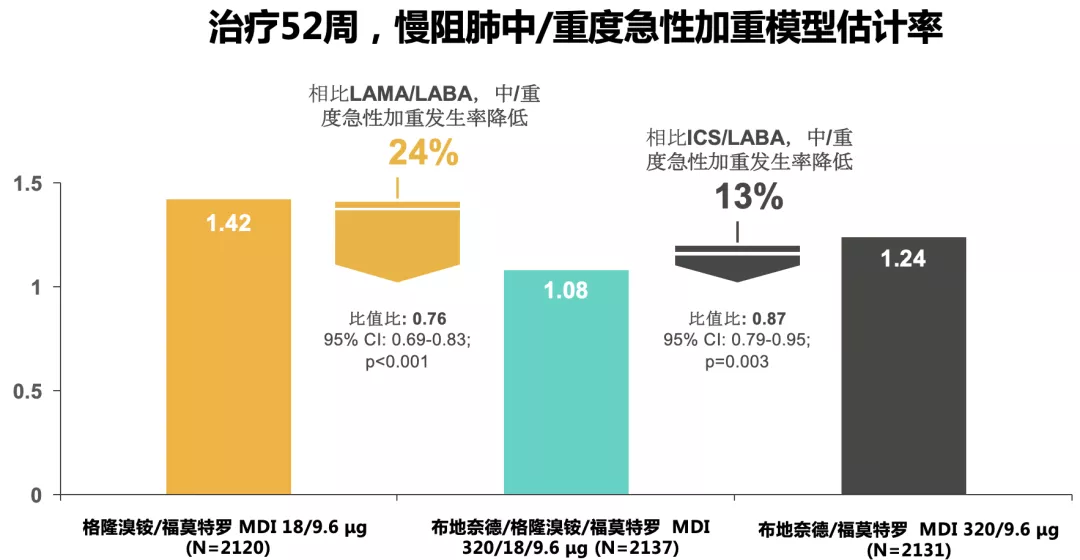
(ETHOS主要终点研究结果)
> 其它次要终点显示:布地格福320较双支扩可显著延长到达首次急性加重的时间,并且显著改善其症状评分和肺功能,减少了急救药物的使用率。
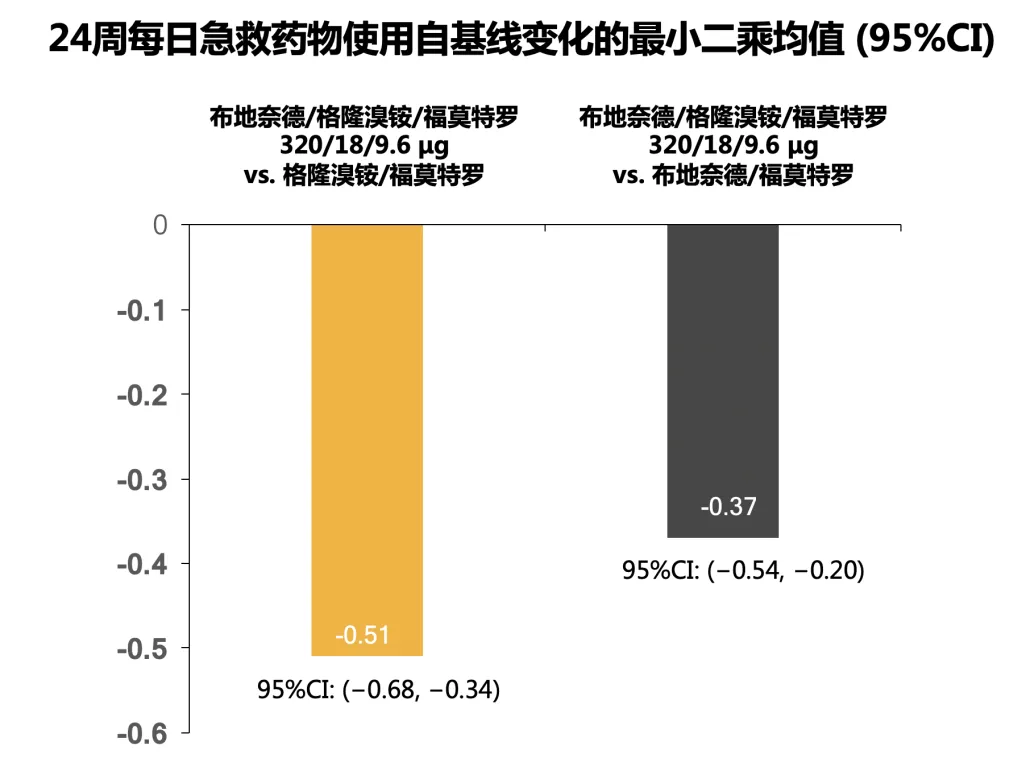
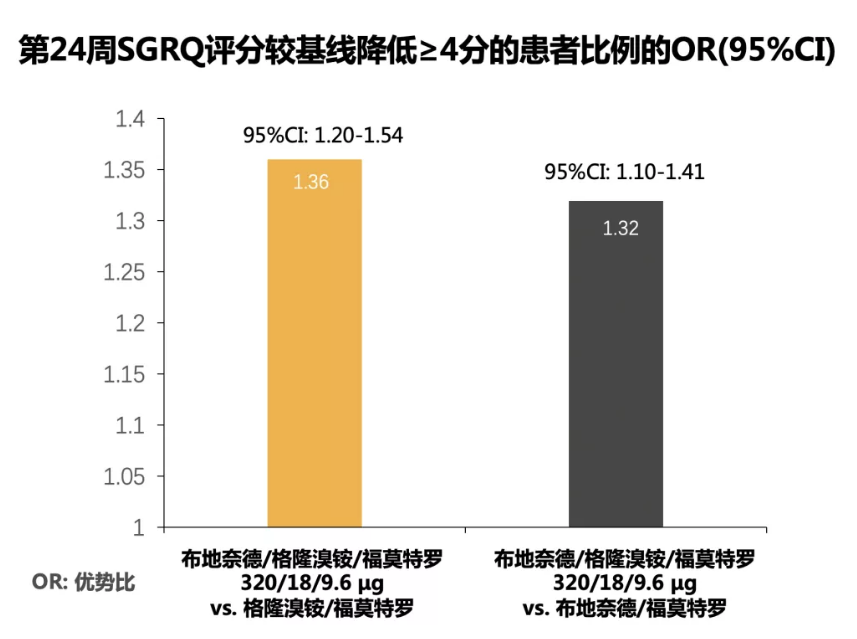
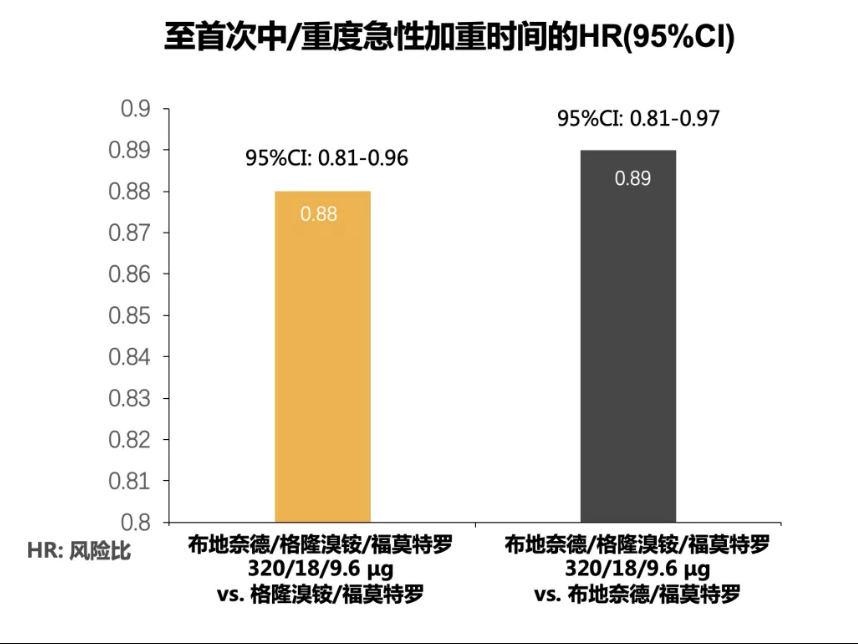
(ETHOS次要终点研究结果)
> 在此,需要值得一提的是,与LAMA/LABA相比,布地格福320显著降低46%的全因死亡率。在慢阻肺领域中,这是首个将全因死亡率作为次要终点观察的大型临床研究。
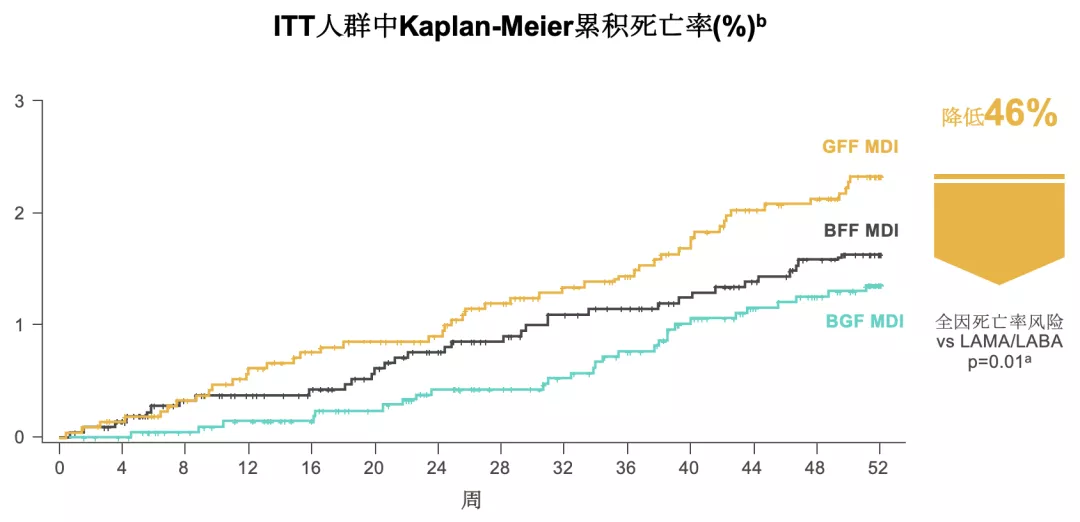
(ETHOS次要终点研究结果)
> 安全性结果显示:布地格福320安全性与各药物成分安全性一致,且与双支扩相比,布地格福不增加主要心血管不良事件发生率。
因此,ETHOS研究给慢阻肺领域三联疗法增加了重要的循证学证据支持,并且表明布地格福在多症状高风险人群中也可以显著降低其急性加重发生风险,改善症状和肺功能,同时,也让我们惊喜的看到,在慢阻肺治疗领域,首个将全因死亡率作为次要终点的大型临床研究,并且发现可以显著降低其死亡风险。因此ETHOS研究的发布,结合KRONOS研究,可以为中国慢阻肺布地格福的临床实践提供充分且有利的循证医学证据,使更多的慢阻肺患者受益。

* 主办单位:北京健康促进会
参考文献
[1] Klaus F. Rabea, Fernando J. Martinezb, Gary T. Ferguson,et al.A phase III study of triple therapy with budesonide/glycopyrrolate/formoterol fumarate metered dose inhaler 320/18/9.6 μg and 160/18/9.6μg using co-suspension delivery technology in moderate-to-very severeCOPD: The ETHOS study protocol.2019;158:59-66;
[2] Rabe KF et al. Online ahead of print. N Engl J Med. 2020;


