推荐语
慢阻肺是一种复杂的异质性疾病,寻找合适的生物标志物以预测疾病进程、判断预后和评估治疗反应,对患者进行个体化管理值得进一步研究;血生物标志物具有便于检测、稳定性和可重复性好的特点,可用于判断慢阻肺预后,但特异性较差,一些较好的生物标志物或可进入临床初步应用。而随着高通量检测技术的发展,采用诸如基因芯片、蛋白组学等技术分析慢阻肺生物标志物特征对个体进行精确分型是未来的研究方向。
慢性阻塞性肺疾病(英文简称COPD)是一个发病率高而起病较隐匿的疾病,其患病率、死亡率逐年攀升。慢阻肺是一种可以预防和可以治疗的常见疾病,其特征为持续存在的气流受限,呈进行性发展,并伴随气道和肺对有害颗粒或气体导致的慢性炎症反应的增加。慢阻肺的病理生理改变不仅局限在肺部,还包括全身性效应(系统性炎症),出现许多肺外表现(全身并发症)。目前临床上常用于诊断和评估慢阻肺的方法是肺功能,而肺功能作为评估慢阻肺的金指标正受到越来越多的质疑。
肺功能在慢阻肺评估中存在缺陷
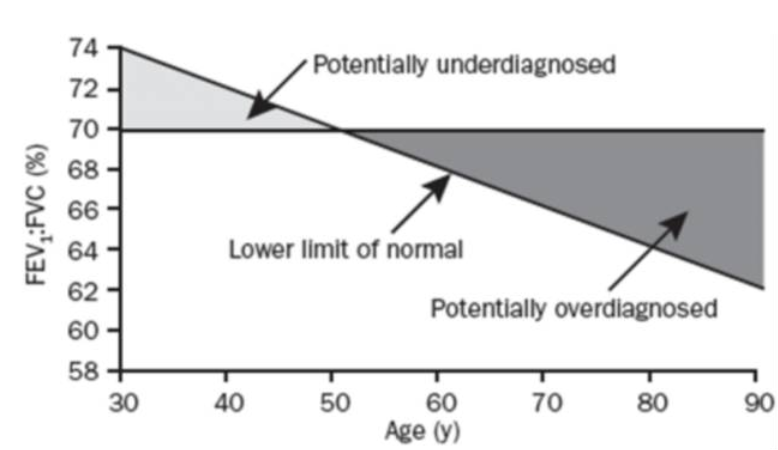
慢阻肺在对外来因素如吸烟的易感性及临床症状、疾病严重程度和进展速度及治疗反应中存在极大的异质性。但目前慢阻肺诊断和评估中往往仅以肺功能为金标准,肺功能具有力量依赖性和年龄依赖性,同时也是非特异性的,并不能完全反映慢阻肺患者的全部临床状况。以舒张后FEV1/FVC<70%为分界点来判定有无气流受限存在对年轻人诊断不足而老年患者过度诊断的缺陷,而肺功能检查在社区的质控往往也不尽如人意。因此,有必要探索慢阻肺评估的新方法。
生物标志物助力慢阻肺评估
生物标志物是指是指可以标记系统、器官、组织、细胞及亚细胞结构或功能改变或可能发生的改变的生化指标,可用于疾病诊断、判断疾病分期或者用来评价药物或治疗在目标人群中的安全性及有效性。理想的慢阻肺生物标志物应该具有肺特异性,能够帮助判断预后,预测急性加重,预测疾病的活动性,并且对治疗产生反应。慢性炎症是慢阻肺主要病因,慢性炎症让慢阻肺的临床表现复杂、多样,并出现很大的差异。ECLIPSE研究发现,存在系统性炎症反应的患者,其病死率和急性加重次数明显增高,提示血液中系统性炎症反应标志物可能成为慢阻肺的理想生物标志物。我们筛选了当前一些研究较多且可能符合理想的慢阻肺生物标志物标准的系统性炎症反应标志物来进行解读,主要包括:嗜酸性粒细胞(Eosinophils),C反应蛋白(CRP),降钙素原(PCT),纤维蛋白原(Fibrinogen),Clara细胞分泌蛋白16 (CC-16),肺部活化调节趋化因子/趋化因子配体18 (PARC/CCL-18),表面活性蛋白D(SP-D)等。
看看研究最火热的嗜酸性粒细胞
(Eosinophils,Eos)
当前研究最火热的要属嗜酸性粒细胞(Eos)了。Eos是白细胞的组成部分,来源于骨髓的造血干细胞,具有杀伤细菌、寄生虫的功能,参与机体的免疫反应与过敏反应,可释放颗粒中的内容物,引起组织损伤,促进炎症进展;研究发现其作为生物标志物可用于评估慢阻肺急性加重风险和对糖皮质激素治疗的敏感性,并且可能成为慢阻肺潜在的治疗靶点。但将Eos作为慢阻肺生物标志物,有4个问题需要回答。
其一,Eos在评估慢阻肺时其界值应如何选取,选择绝对计数还是百分比?当前研究尚无定论。研究显示,高Eos是慢阻肺急性加重的独立危险因素,在调整潜在的混杂因素后, 1年内慢阻肺急性加重风险显著增高:≧ 300/ mm3(RR, 1.25);≧ 400/ mm3(RR, 1.48);≧ 500/ mm3(RR, 1.76);而另一项研究将Eos=0.34×109 cells/L作为界点,则发现Eos>0.34×109 cells/L是以LNN诊断慢阻肺急性加重的危险因素(IRR, 1.78);而Eos ≧ 2%仅是临床诊断慢阻肺重度急性加重的危险因素(IRR, 1.88)。也就是说EOS不同绝对值和百分比均可用于判断慢阻肺急性加重风险,但临床应用其界值究竟如何选择仍未确定。
其二,Eos是否可用于选择慢阻肺用药?研究显示用2%Eos作为界值指导慢阻肺急性加重时口服激素治疗,可显著降低治疗失败率,Eos ≧ 2%未接受泼尼松治疗患者,治疗失败率为66%,而接受泼尼松治疗组则仅为11%。同时Eos可用于指导慢阻肺吸入性糖皮质激素用药。而来源于FLAME研究的数据显示,无论Eos界值为2%,3%还是5%,均不能用于判断慢阻肺的ICS/LABA与LABA/LAMA选择。
其三,Eos是慢阻肺治疗靶点吗?2014年贝那利珠单抗的II期临床试验未获得阳性结果。2017年10月最新发表在NEJM上的一项研究对慢阻肺患者美泊珠单抗III期临床试验进行了事后分析。发现在两项研究(MENSA和DREAM)中,100mg美泊珠单抗可降低频繁急性加重嗜酸性粒细胞亚型慢阻肺患者总中重度急性加重次数,而在未分型频繁急性加重慢阻肺患者和具有嗜酸性粒细胞亚型的慢阻肺患者中,结果无统计学差异。说明嗜酸性粒细胞是否是慢阻肺治疗靶点仍是令人疑惑的。

其四,是选择血Eos还是痰Eos作为慢阻肺生物标志物呢?最新发表在Lancet呼吸子刊的文章显示,痰Eos与慢阻肺相关性更好,而血EOS与慢阻肺严重程度、急性加重、痰EOS相关性并不佳,该文建议临床试验中应更多考虑使用痰Eos评估慢阻肺嗜酸性粒细胞性炎症。

综上所述,尽管嗜酸性粒细胞的界值尚未得到确认,但其在判断慢阻肺预后和指导慢阻肺治疗方面具有较好的作用,并且可能成为慢阻肺的一个新的治疗靶点。因此,Bafadhel等人总结了以下Eos临床应用的流程。

临床最常见的C反应蛋白(CRP)
CRP在临床应用中非常普遍,那么它在慢阻肺评估中有哪些作用呢?
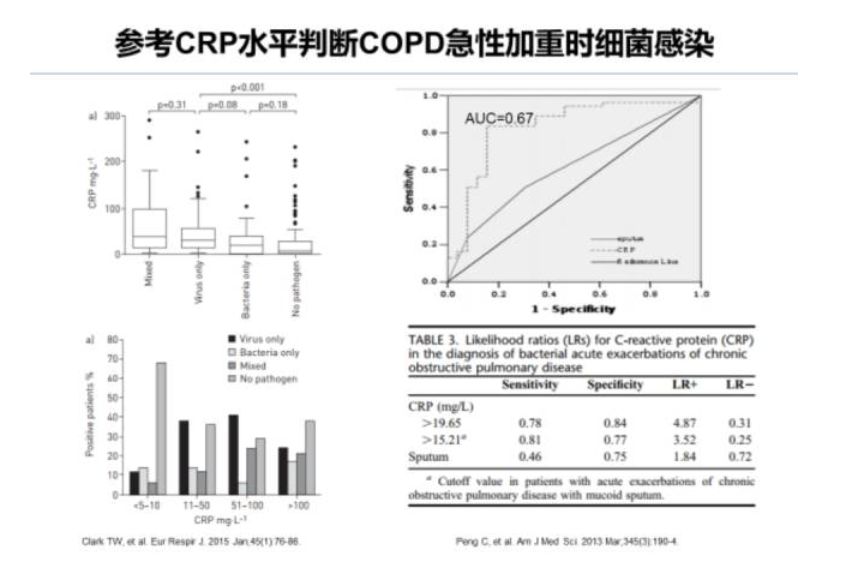
CRP是一种主要由肝脏合成的非特异性急性时相蛋白,在急性炎症反应中增高,可用于辅助诊断慢阻肺急性加重。CRP在慢阻肺急性加重期可显著增高,但仅依靠CRP增高来诊断慢阻肺急性加重其特异性和敏感性都欠佳(AUC=0.73),但如果将CRP与任何一个急性加重的主要症状(如呼吸困难、痰量改变或者是否为脓痰)结合起来用于诊断慢阻肺急性加重,则诊断效能显著提高(AUC=0.88)。CRP可用于判断慢阻肺预后,基线高CRP水平可能预示着慢阻肺患者更高的住院和死亡风险。同时,参考CRP水平可用于判断慢阻肺急性加重时是否发生细菌感染,CRP>15.21mg/L具有较好的敏感性和特异性。
降钙素原(PCT)指导慢阻肺抗生素治疗
临床常用语判断细菌感染的降钙素原(PCT)也可能成慢阻肺生物标志物。PCT是一种由116个氨基酸组成的糖蛋白,是降钙素的多肽前体, 由甲状腺的滤泡旁细胞(C细胞)以及肺和小肠的神经内分泌细胞分泌,与细菌、真菌、寄生虫感染和脓毒症休克等相关;可用于鉴别细菌性与非细菌性炎性反应,以指导慢阻肺治疗中抗生素的使用。研究显示,依据PCT指导抗生素使用可显著降低慢阻肺初始抗生素的使用率以及抗生素使用时间。

纤维蛋白原(Fibrinogen)
——FDA首个认证慢阻肺生物标志物
纤维蛋白原(Fibrinogen)是一种由肝脏合成的具有凝血功能的蛋白质,水平增加与心血管疾病风险相关,但排除心血管疾病影响,纤维蛋白原在慢阻肺中是增加的,并且与慢阻肺进展相关,可预测慢阻肺急性加重风险和死亡风险。2005年,一篇发表在JAMA杂志上的meta分析显示:血浆纤维蛋白原水平不仅与冠心病等心血管疾病死亡风险相关,其与非心血管疾病死亡风险也具有较好的相关性,纤维蛋白原水平在原基础上增加1g/L是疾病死亡的危险因素,但是该文章建议在评估纤维蛋白原水平与疾病的关系时仍需要进一步的研究。
那么纤维蛋白原与慢阻肺的相关性就行如何呢。 一份来自包括8955名研究对象的哥本哈根城市心脏病(Copenhagen City Heart Study)队列研究显示,无论是吸烟还是未吸烟者,纤维蛋白原越高,FEV1越低,并且高纤维蛋白原与高慢阻肺住院率相关,纤维蛋白原> 393 mg/dL是慢阻肺死亡和住院风险的高危因素。同时,研究发现急性加重次数大于2.5次/年患者其血浆纤维蛋白原水平较急性加重次数小于2.5次/年患者更高,并且增长更快;而血浆纤维蛋白原>3.95g/L组其FEV1%pred下降率较低纤维蛋白原<3.95g/L者多0.4%/yr,并且纤维蛋白原增加越快,FEV1%pred降低越快,这一改变与吸烟、系别和初始FEV1值无关。说明血浆纤维蛋白原水平与慢阻肺的疾病进展之间存在很好的相关性,预示着纤维蛋白原可作为预测慢阻肺进展良好生物标志物。
血浆纤维蛋白原是首个被FDA认证的慢阻肺生物标志物。在2015年,慢阻肺生物标志物鉴定协会(CBQC)综合了包括ECLIPSE研究在内的5个大型研究结果的数据,共纳入了6376名通过肺功能确诊的慢阻肺患者的资料,以350mg/dL为界点,分为血浆纤维蛋白原高水平和低水平组,对慢阻肺患者急性加重与死亡的风险进行了评估。
Kaplan-Meier曲线分析结果显示,高水平组和低水平组在12月内因急性加重住院的比率分别为16.8%和9.5%(HR: 1.64),并且高水平组与低水平组慢阻肺在36个月内死亡的比率分别为13%和6%(HR: 1.94),提示高纤维蛋白原水平是慢阻肺急性加重和死亡的危险因素。急性加重病史与纤维蛋白原可共同预测慢阻肺未来急性加重,在既往有任何一次急性加重病史组中,高纤维蛋白原水平组在12个月内出现中重度急性加重的比例高达75.6%,而无论有无急性加重,高纤维蛋白原组急性加重比例均较低纤维蛋白原组显著增高。
这些结果均提示高纤维蛋白原水平与慢阻肺急性加重风险增高和死亡风险增高显著相关,如果结合慢阻肺患者既往急性加重病史,可能作为预测慢阻肺人群急性加重和死亡风险的一个十分有用的临床血清标志物,临床实际工作中值得推广。
纤维蛋白原与慢阻肺药物治疗也存在相关性。一项进行了12周的RCT研究证实,在p38-MAPK抑制剂组(75mg,bid)、沙美特罗/氟替卡松吸入组(50ug/500ug)和安慰剂组三组间,进行12周的治疗,p38抑制剂使纤维蛋白原水平下降了约11%,而支气管舒张剂干预组则出现了纤维蛋白原的轻度升高,二者治疗反应不同,说明纤维蛋白原可能成为p38-MAPK抑制剂药物开发中的一个生物标志物。
参与慢阻肺发病的Clara细胞分泌蛋白16
( CC-16)
CC-16是由分布于终末支气管和呼吸性支气管上皮的无纤毛细胞即Clara细胞分泌的一种蛋白,具有抗炎、抗氧化的生物学活性,参与慢阻肺发病。研究显示,在重度慢阻肺患者(GOLD IV)气道上皮中,CC16几乎全部丢失,并且在烟雾暴露下,CC16-/-小鼠更易于出现肺气肿和小气道重塑。而另一项大型队列研究显示,低CC-16与吸烟者慢性支气管炎发生显著相关。提示CC-16可能是慢阻肺的治疗靶点。
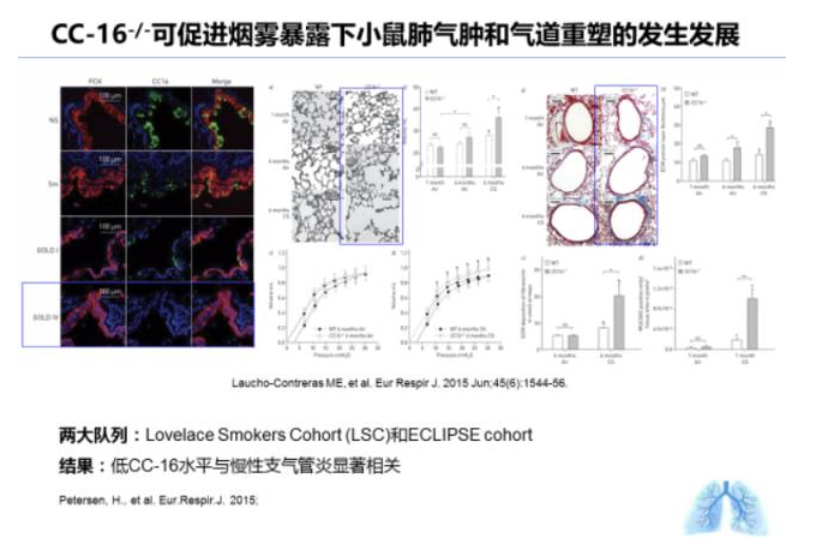
在Lung Health Study这项对4724名轻中度气流受限患者进行9年的随访的大样本人群研究中,发现CC-16在吸烟者尤其是持续吸烟者血清中显著降低,并且与FEV1下降是显著相关,CC16浓度越低,FEV1年下降水平越大,并且这种相关不受年龄、性别、现阶段吸烟状况、BMI以及基线FEV1水平的影响。那么在慢阻肺患者中,情况又如何呢?在ECLIPSE研究中,Jorgen Vestbo等通过对2163名慢阻肺患者进行长达三年的随访,并检测了IL-6、CC-16等7种血清标志物的变化情况,发现只有CC-16水平与FEV1年下降率显著相关,并且CC-16每减少1个SD值,FEV1额外减低约4ml/yr。2015年一项发表在Lancet杂志呼吸子刊上的文章同样也证实,基线期CC-16水平越低,FEV1下降得越快,是高水平CC-16的FEV1下降速度的2倍,并且儿童期低水平的CC-16在成年时期更有可能出现气流受限。说明CC-16可能成为预测慢阻肺疾病进程的一个良好的生物标志物。

肺部调节趋化因子/趋化因子配体18
(PARC/CCL-18)
PARC/CCL-18主要由树突状细胞与单核细胞合成,在肺内高表达,能趋化原始淋巴细胞,在多种肺部疾病中增高。探索慢阻肺生物标志物的ECLIPSE研究同样探讨了PARC/CCL-18作为慢阻肺生物标志物的可能性,研究发现,慢阻肺患者PARC/CCL-18显著增高(P <0.001),但是在GOLD分级中没有差异,而以147ng/ml为界点,PARC/CCL18>147ng/ml的慢阻肺患者全因死亡率增高(HR: 1.9),说明高PARC/CCL-18水平是慢阻肺全因死亡的危险因素。CCL-18与AE慢阻肺发作频率也相关,可用于鉴别重度慢阻肺急性加重需要住院治疗者。
研究还发现,PARC/CCL-18与FEV1%pred显著负相关,并且在系统性抗炎时产生动态变化:口服泼尼松龙治疗2周后,血清PARC/CCL-18水平显著降低,但当降低泼尼松剂量后,PARC/CCL-18水平也逐渐增高,在激素撤退以后,恢复到与安慰剂组相似水平,说明PARC/CCL-18与激素治疗具有良好的相关性,或可用于监测激素用药情况,更多大型的研究可对PARC/CCL18在慢阻肺中的生物标志物作用进行进一步验证。
表面活性蛋白D(SP-D)
SP-D是主要由II型肺上皮细胞分泌的一种亲水糖蛋白,肺固有免疫的重要组成部分,具有抗炎、抗氧化以及保护呼吸道免受感染等作用,在慢阻肺患者的BALF中水平降低,但在血液中却增高。ECLIPSE研究发现在高SP-D水平组,慢阻肺全因死亡率显著增高。另有研究显示,一旦慢阻肺患者血清SP-D水平高于正常者95%上限(175.4 ng.mL-1),则其在一年发生急性加重的风险显著增高(OR:1.30)。SP-D在慢阻肺全身激素治疗时可发生改变。经泼尼松龙20mg/d治疗后,SP-D水平逐渐降低,在第4周达到最低,在逐渐撤除激素的过程中,SP-D水平逐渐增高,但与舒张后FEV1变化趋势不一致。以上研究结果说明,SP-D可能在判断慢阻肺预后中发挥作用,并具有较好肺特异性,但有待进一步验证。
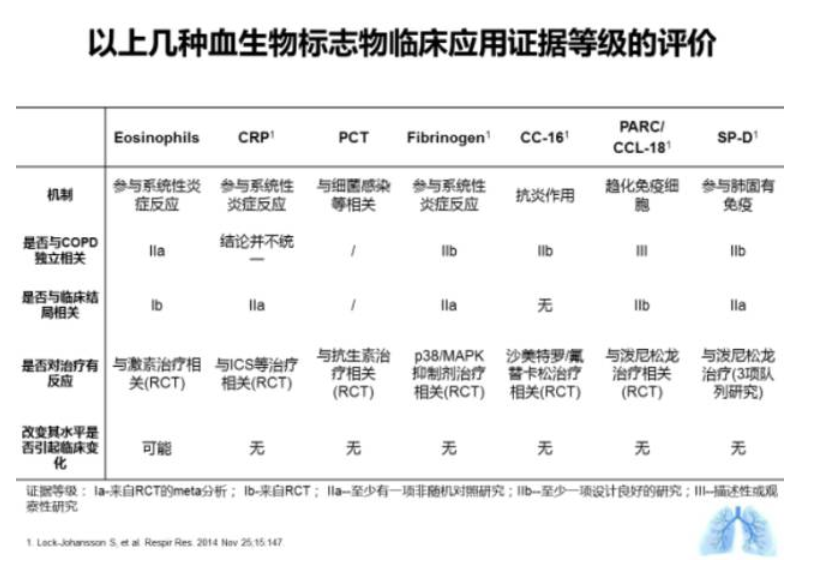
上图是对以上7种生物标志物的总结。从这个表格中可以发现,这些因子在慢阻肺预后判断中具有指导作用。而尽管这7种血蛋白都能对治疗产生反应,或可参与慢阻肺发病,但针对这些标志物进行干预是否能对慢阻肺产生疗效或临床指标的干煸尚无结论或相关研究。血生物标志作为慢阻肺生物标志物的临床依据尚待进一步完善。
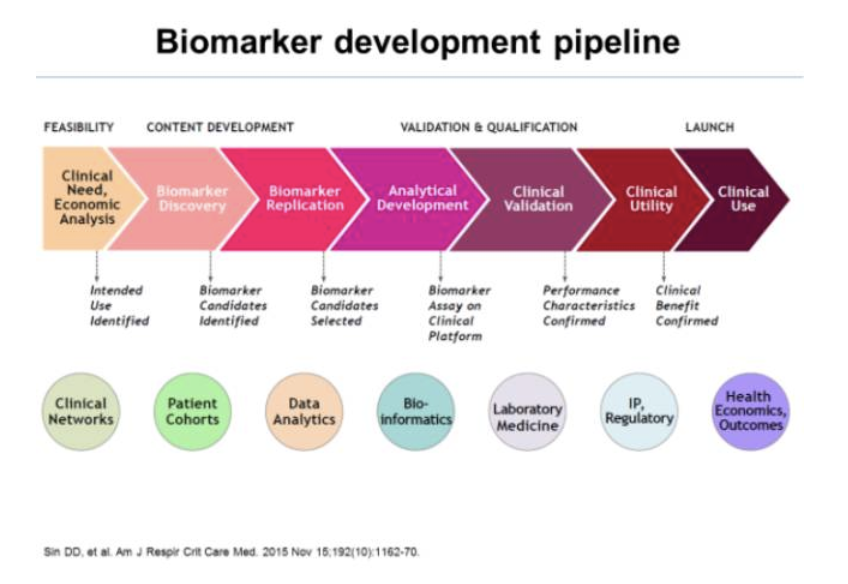
那么,是否还有其他的或一些新的血清蛋白可能成为慢阻肺的生物标志物呢?SinDD等人对慢阻肺生物标志开发做了如下图的总结,开发慢阻肺生物标志物尚有很长的一段路要走。
小结
慢阻肺是一种复杂的异质性疾病,寻找合适的生物标志物以预测疾病进程、判断预后和评估治疗反应,对患者进行个体化管理值得进一步研究;血生物标志物具有便于检测、稳定性和可重复性好的特点,可用于判断慢阻肺预后,但特异性较差,一些较好的生物标志物或可进入临床初步应用。而随着高通量检测技术的发展,采用诸如基因芯片、蛋白组学等技术分析慢阻肺生物标志物特征对个体进行精确分型是未来的研究方向。




