摘要
慢性阻塞性肺疾病(慢阻肺)全球创议(global initiative for chronic obstructive lung disease,GOLD)2021年修订版于2020年11月17日发布,总体来说对于慢阻肺的诊断、评估、个体化治疗同GOLD 2020,其最重要的改变是增加了世界卫生组织关于中低收入国家慢阻肺筛查干预的基本保健措施,特别增加了第七章「新型冠状病毒疫情防控期间慢阻肺患者的管理」。本文对新增内容进行简介和解读。
关键词
慢性阻塞性肺疾病 ;世界卫生组织慢阻肺基本筛查干预措施 ;合并症 ;新型冠状病毒肺炎 ;远程医疗
1998年慢性阻塞性肺疾病(慢阻肺)全球创议(global initiative for chronic obstructive lung disease,GOLD)启动,其目标是根据已发表的最佳研究结果制订慢阻肺的管理推荐。第1版慢阻肺诊断、治疗及预防全球策略于2001年发布,并于2006年和2011年[1]分别根据已发表的研究进行了全面修订。GOLD 2011修订版的修订分别于2013年1月、2014年 1月、2015年1月和2016年1月发布,国内呼吸领域相关专家亦分别对其进行了解读[2-5]。2015—2016年,GOLD科学委员会发现,关于慢阻肺的病理生理、诊断、评估和治疗方法有较多新内容出现,因此需要进行全面修订,由写作委员会制订各章节大纲。2016年9月,GOLD科学委员会对各章节进行审阅,然后送至GOLD委员会之外的10名专家处,提出建议并进行修改。GOLD 2017作为第4次全面修订,于2016年11月16日在美国费城举办的GOLD慢阻肺全程管理会议上发布,笔者分别对GOLD 2017、GOLD 2018、GOLD 2019、GOLD 2020进行了详细解读[6-9]。
2018年GOLD峰会讨论认为中低收入国家慢阻肺流行病学和临床特征数据有限,各国之间存在明显差异,这些国家存在慢阻肺的危险因素,如销售便宜的烟草产品、室内空气污染等,肺量计测定未得到普及,可及的有质量保证的药物和非药物治疗存在重大问题。GOLD关注个人、社区、各国政府和国际机构是否高度重视慢阻肺,致力于改善慢阻肺高危人群和慢阻肺患者的健康状况,无论他们出生于何处,希望尽自己的力量帮助实现联合国可持续发展目标,减少非传染性疾病患者的过早死亡,如至2030年将慢阻肺死亡率减少1/3[10-12]。
GOLD 2021是GOLD 2020的修订版,新增2019年1月至2020年7月的244篇参考文献,其中24篇来自中国学者的研究,于2020年11月17日发布[13]。总体来说,GOLD 2021关于慢阻肺定义、诊断、评估、初始治疗和随访期管理与GOLD 2020相同,重要的变化之处在于增加了世界卫生组织(World Health Organization,WHO)关于中低收入国家慢阻肺筛查干预的基本保健措施[14],特别增加了第七章「新型冠状病毒疫情防控期间慢阻肺患者的管理」。2020年11月18日是第19个世界慢阻肺日,主题为「改善慢阻肺生活,无论何人与何地(Living well with COPD,everybody, everywhere)」。本文对GOLD 2021重要更新内容进行简介和解读。
第一章:慢阻肺定义和概述
关键点
- 慢阻肺是一种常见,可预防和可治疗的疾病,其特征在于持续的呼吸道症状和气流受限,这是由于气道和/或肺泡异常所致,通常是由于长期暴露于有害颗粒或气体所引起。
- 最常见的呼吸系统症状包括呼吸困难、咳嗽和/或咳痰。患者对这些症状的报告可能不足。
- 慢阻肺的主要危险因素是吸烟,但其他环境暴露,如生物燃料暴露和空气污染可能参与发病。除暴露外,个体宿主易感性也会导致慢阻肺的发生,其中包括基因异常、肺发育异常和加速衰老。
- 慢阻肺可伴有呼吸系统症状的急性恶化,称为慢阻肺急性加重。
- 大多数慢阻肺患者存在重大的共患慢性病,可增加慢阻肺的致残率和死亡率。
更新要点
GOLD 2021新增影响慢阻肺发生、发展的危险因素,包括遗传易感性、生物燃料与慢阻肺的关系,关注欧洲人群中α1抗胰蛋白酶(αlpha-1 antitrypsin,AAT)缺乏PiZZ基因型发生率,提出目前仍然缺乏与生物燃料有关的慢阻肺研究。
1.1 遗传易感性与慢阻肺
重度AAT缺乏是常染色体共显性遗传罕见病,由SERPINA1基因突变所致,主要影响欧洲后裔高加索种族。96%的AAT缺乏患者为SERPINA1 Z突变(Glu342Lys)纯合子,表达ZZ基因型(PiZZ),不同研究之间PiZZ基因型百分比差异很大。对20项针对欧洲人群的研究进行了系统回顾,发现36 298例(95%CI:23 643~56 594)高风险的PiZZ个体和30 849 709例(95%CI:21 411 293~40 344 496)慢阻肺患者,PiZZ/慢阻肺比率为0.12%(0.08%~0.24%),北欧患病率为1/408,西欧为1/944,中欧为1/1051,南欧为1/711,东欧为1/1274。这些数据可能有助于规划未来的研究和诊断策略,并使可用的治疗资源合理化[15]。
1.2 生物燃料与慢阻肺
木材、动物粪便、农作物残梗、煤炭以明火或在通风功能不佳的炉灶中燃烧,可导致严重的室内空气污染。越来越多的证据表明,烹饪过程中使用的现代和传统燃料产生的室内生物暴露可能使许多发展中国家女性慢阻肺发生风险增加。世界范围内近30亿人使用生物燃料或煤炭作为主要的烹饪、取暖及其他家务需要的能源,危险人群数量很大。GOLD 2020引用中国慢性病前瞻性研究项目(简称CKB)队列,对中国280 000名非吸烟成人的调查显示,烹饪使用固体燃料与罹患重大呼吸道疾病、死亡的风险更高有关,改用清洁燃料或使用通风炉灶者上述风险较未改用者降低[16]。GOLD 2021提出目前证据仍然有限,需要进一步研究。
第二章:诊断和初始评估
关键点
- 存在呼吸困难、慢性咳嗽或咳痰,有复发性下呼吸道感染史和/或有接触该疾病危险因素史的患者均应考虑慢阻肺。
- 肺功能检查是确诊慢阻肺的必备条件。如支气管扩张剂后第1秒用力呼气容积(forced expiratory volume in one second,FEV1)/用力肺活量(forced vital capacity,FVC)<0.70,可确定存在持续气流受限。
- 慢阻肺评估的目标在于确定气流受限程度、疾病对患者健康状况的影响和远期不良风险(如慢阻肺急性加重、住院或死亡),从而用以指导治疗。
- 慢阻肺患者常合并心血管疾病、骨骼肌功能障碍、代谢综合征、骨质疏松、抑郁、焦虑、肺癌等慢性病。这些合并症是影响患者住院和死亡的独立危险因素,因此,对慢阻肺患者均应积极寻找合并症,并给予正确治疗。
更新要点
GOLD 2021慢阻肺的初始评估与GOLD 2020相同,要评价患者的症状、气流受限程度、急性加重发生风险、合并症,依据症状、急性加重风险将患者分为A—D组。GOLD 2021参考WHO在基层医疗中诊断慢阻肺的最低限度干预措施。疲劳、体重减轻、肌肉萎缩和厌食是重度和极重度慢阻肺患者的常见问题。在获取病史时,抑郁和/或焦虑症状值得具体询问,因为它们在慢阻肺中很常见,并与较差的健康状况、急性加重风险增加和紧急入院相关。
2.1 WHO关于基层医疗慢阻肺的诊断方法
GOLD 2021最大的改动是增加了WHO关于「慢阻肺在中低收入国家的必要干预措施建议」。慢阻肺诊断:当患者存在慢性咳嗽、呼吸困难、胸闷或喘息的症状时,临床医生应考虑慢阻肺或者哮喘诊断。如果存在下列特征,需要考虑慢阻肺诊断:①既往诊断慢阻肺;②每天吸烟20支以上超过15年;③在封闭空间有长期大量生物燃料暴露史或职业粉尘接触史;④40岁以上出现症状、慢性病程,进行性加重;⑤表现为慢性咳嗽或咳痰、逐渐出现活动后呼吸困难;⑥症状持续存在,较少发生日间变异。根据当地肺结核感染的风险,如果咳嗽持续2周以上应该怀疑肺结核的可能,并做进一步检查。为明确诊断,需要测定呼气峰流速(peak expiratory flow rate,PEFR),在吸入短效β2受体激动剂沙丁胺醇2喷后15 min重复测定,如果PEFR改善<20%,则考虑慢阻肺诊断可能性大;如果PEFR改善≥20%,则考虑哮喘可能性大。
慢阻肺严重程度评估:如果条件允许,测定PEFR和氧饱和度。根据呼吸困难程度判断慢阻肺严重程度,正常活动出现呼吸困难为中度,休息时出现呼吸困难为重度。
WHO关于慢阻肺的诊断,仅仅是「症状提示慢阻肺」,没有提及常规肺功能检查(FEV1/FVC)的诊断标准,如果可能则测定PEFR。PEFR测定所需仪器相对简单,价格便宜,便于推广,容易被中低收入国家人群所接受。当然,PEFR用于慢阻肺的诊断,不及常规肺功能检查(FEV1/FVC)准确,如有条件,仍建议做肺量计检查。
2.2 肌肉减少与慢阻肺不良预后
疲劳、体重减轻、肌肉萎缩和厌食是重度和极重度慢阻肺患者的常见症状。慢阻肺患者经常发生肌肉减少,但是缺乏系统评估肌肉减少对不良结局的影响。应用美国全国住院患者(nationwide inpatient sample,NIS)数据库[17]分析2011年1月1日至12月31日174 808例慢阻肺急性加重住院患者肌肉减少,发现有12 977例(7.4%)次要诊断为肌肉减少。与非肌肉减少患者相比,肌肉减少表型院内死亡率(14.6%∶5.7%)、住院天数[(13.3±17.1)d∶(5.7±7.6)d]和每位患者的中位住院费用($ 13 947∶$ 6610)均显著增加。多元回归分析显示,肌肉减少使死亡率增加111.0%,住院天数增加68.4%,直接护理费用增加83.7%。慢阻肺急性加重肌肉减少表型患者的院内死亡率、住院天数和医疗保健费用较高,需要联合营养科、康复医学科,加强对这些患者的营养评估和康复指导。
2.3 抑郁与慢阻肺急性加重
慢阻肺常合并焦虑和/或抑郁症状,在询问慢阻肺患者病史时需要予以关注,可以采用不同的量表评估焦虑和/或抑郁。医院焦虑抑郁量表(hospital anxiety and depression scale,HADS)包含14个问题,由患者自测,评分为0~21分,界值8分以上诊断抑郁的灵敏度为0.82(95%CI:0.73~0.80),特异度为0.74(95%CI:0.60~0.84)。对英国6家初级保健机构355例慢阻肺患者进行为期12个月的前瞻性随访,发现高龄、有多种合并症、重度慢阻肺、既往急诊就诊、抑郁均与未来1年的急诊就诊和急诊入院独立相关。HADS抑郁评分为4~7分,急诊入院率增加2.8倍,而HADS抑郁评分>8分,急诊就诊率增加4.8倍[18]。抑郁与较差的健康状况、急性加重风险增加和急诊入院相关,这表明需要在初级保健中评估焦虑和/或抑郁,并采取综合管理措施,这不仅可以改善患者躯体症状,而且可以改善其精神症状。根据疾病严重程度,可以采取认知行为治疗或药物干预治疗。
第三章:预防和维持治疗的支持证据
关键点
- 戒烟是关键。药物治疗和尼古丁替代疗法确实提高了长期戒烟率。由医疗专业人员提供的立法禁烟和咨询提高了戒烟率。
- 目前,电子烟作为戒烟辅助手段的有效性和安全性尚不确定。
- 药物治疗可减轻慢阻肺症状,降低急性加重发生频率和严重程度,改善患者健康状况和运动耐力。近期数据显示其可降低死亡率。
- 每种药物治疗方案均应根据症状的严重程度、急性加重的风险、不良反应、合并症、药物的可用性和成本以及患者的反应、偏好和使用各种药物递送装置的能力进行个体化指导。
- 需要定期评估吸入技术。
- 流感疫苗可降低下呼吸道感染的发生率。
- 肺炎链球菌疫苗可减少下呼吸道感染。
- 美国疾病控制与预防中心建议慢阻肺患者如青春期未接种Tdap疫苗(dTaP/dTPa)应该补接种,以预防百日咳、破伤风和白喉的发生。
- 肺康复可以改善症状、生活质量和日常活动中的身体和精神状况。
- 长期氧疗可提高严重静息慢性低氧血症患者的生存率。
- 对于稳定期慢阻肺患者和静息或运动引起的中度氧合下降慢阻肺患者,不应常规进行长期氧疗。但是,在评估患者对补充氧气的需求时,必须考虑患者的个体因素。
- 对于有严重慢性高碳酸血症和急性呼吸衰竭住院史的患者,长期无创通气可降低死亡率并防止再次住院。
- 对于某些内科治疗无效的晚期肺气肿患者,外科手术或支气管镜介入治疗可能获益。
- 姑息治疗是控制晚期慢阻肺症状的有效方法。
更新要点
GOLD 2021稳定期慢阻肺支气管扩张剂、抗炎药物的使用原则同GOLD 2020,增加了关于慢阻肺双支气管扩张剂、三联药物治疗、肺康复等非药物治疗的更多循证医学证据。
3.1 电子烟与肺损伤
电子烟作为戒烟辅助方法,其有效性和安全性仍有争议。已有电子烟相关肺损伤的报道,长期不良效应(如是否会导致肺癌、慢阻肺发生风险增加)目前尚无数据。电子烟提供了可汽化且可计量的尼古丁,并且对于希望戒烟的人群来说,电子烟可以代替卷烟的使用量,但对于既往从未吸烟的年轻烟民,这种趋势正在上升。电子烟已有15年的历史,它不仅包含尼古丁,还包含其他化学物质,如植物甘氨酸、丙二醇、各种调味剂、挥发性羰基化合物、二乙酰基、活性氧、呋喃酮和金属,长期使用对健康的影响未知[19,20]。
3.2 疫苗
美国疾病控制与预防中心建议慢阻肺患者如青春期未接种Tdap疫苗(dTaP/dTPa)应该补接种,以预防百日咳、破伤风和白喉的发生[21]。
3.3 WHO确定了基层医疗机构中稳定期慢阻肺管理的最低限度干预措施
推荐中低收入国家给予慢阻肺患者吸入沙丁胺醇,按需2喷,每日最多4次,如果症状继续存在,考虑加用低剂量茶碱。如果可能则吸入异丙托溴铵,替代沙丁胺醇,但是该药价格较昂贵。
充分考虑中低收入国家的国情,WHO方案中的慢阻肺治疗药物都是20世纪应用的呼吸系统疾病治疗药物。我国各级医疗机构需要根据药物可及性、价格、患者偏好、疗效、不良反应等因素为患者制订合适的治疗方案。
3.4 甲基黄嘌呤
在甲基黄嘌呤部分新增了其与常用药物之间的相互作用,澄清了同类药物之间的作用差异,明确指出了甲基黄嘌呤与红霉素(但不是阿奇霉素)、某些喹诺酮类抗生素(环丙沙星,但不是氧氟沙星)、别嘌呤醇、西咪替丁(但不是雷尼替丁)、5-羟色胺摄取抑制剂(氟伏沙明)和5-脂氧合酶抑制剂等常用药物具有显著的相互作用。
3.5 双支气管扩张剂联合治疗
EMAX研究是一项为期24周的多中心、随机、双盲、平行试验[22]。该研究在全球213个中心开展,入选40岁以上、慢阻肺评估测试(COPD assessment test,CAT)≥10分、中重度慢阻肺,过去1年≤1次中度急性加重,未接受吸入性糖皮质激素(inhaled corticosteroid,ICS)、长效抗胆碱能药物(long-acting muscarinic antagonists,LAMA)/长效β2受体激动剂(long-acting β2-agonists,LABA)维持治疗,随机分组,每天1次乌美溴铵/维兰特罗62.5/25 μg,或每天1次乌美溴铵62.5 μg,或每天2次沙美特罗50 μg。结果发现,治疗第24周使用双支气管扩张剂治疗的患者FEV1谷值与基线的变化较乌美溴铵增加66 ml(95%CI:43~89),较沙美特罗增加141 ml(95%CI:118~164)。与两种单支气管扩张剂相比,双支气管扩张剂持续改善呼吸困难变化指数[乌美溴铵/维兰特罗∶乌美溴铵:0.37(95%CI:0.06~0.68);乌美溴铵/维兰特罗∶沙美特罗:0.45(95%CI:0.15~0.76)],且双支气管扩张剂联合治疗显著降低了首次临床重要恶化的风险。与长效支气管扩张剂单一疗法相比,长效双支气管扩张剂(LABA/LAMA)可改善患者肺功能和临床症状,对于症状多、低风险患者,早期使用双支气管扩张剂有助于优化慢阻肺的治疗。
3.6 ICS
GOLD 2021关于慢阻肺患者初始治疗需要应用ICS的联合治疗推荐方案同GOLD 2020,强烈支持:中度急性加重≥2次/年,或因急性加重住院,血嗜酸性粒细胞≥300 cells/μl,既往有哮喘病史或目前合并哮喘;可考虑使用:既往中度急性加重,血嗜酸性粒细胞为100~300 cells/μl;不支持使用:反复发生的肺炎,血嗜酸性粒细胞<100 cells/μl,有结核分枝杆菌感染。随访期间调整治疗方案,根据患者呼吸困难和急性加重情况判断是否需要增加或撤除ICS。
吸烟会导致「类固醇抵抗」,从而降低ICS的作用。一项荟萃分析纳入7项研究,关注肺功能下降和急性加重情况。4项研究纳入17 892例受试者,使用ICS治疗约30个月,与轻度吸烟者相比,重度吸烟者(>36包年)FEV1下降幅度更大(-75 ml~-22 ml),吸烟者与戒烟者相比FEV1变化从-8 ml到+77 ml。4项研究纳入21 270例受试者,观察52周时慢阻肺急性加重频率的差异。与既往吸烟者或轻度吸烟者相比,当前吸烟或重度吸烟者的急性加重频率更高[RR:(0.81~0.99)∶(0.92~1.29)],吸烟抵消了ICS的治疗效果。与轻度吸烟者或既往吸烟者相比,尽管使用ICS治疗对重度吸烟者或当前吸烟者急性加重的影响程度较低,但当前吸烟者和既往吸烟者的肺功能和急性加重频率均可从ICS治疗中获益[23]。
另外有多项研究仍在探索ICS治疗与肺癌发生风险之间是否存在矛盾。对慢阻肺患者进行的几项观察性研究报道了不一致的结果:使用ICS治疗可以显著降低肺癌发生率,也可能是无效的。利用魁北克医疗数据库进行的一项纳入63 276例慢阻肺受试者的队列研究结果显示,相对于未使用ICS,ICS暴露相关的肺癌调整后风险发生率为1.01(95%CI:0.94~1.08),ICS使用时间较长(>4年)的风险发生率为0.92(95%CI:0.83~1.03),而平均ICS日高剂量(>1000 μg氟替卡松当量)使用的风险发生率为1.36(95%CI:1.03~1.81),表明ICS与慢阻肺患者的肺癌发生率降低无关。因此,进行相关随机试验的提议需谨慎考虑[24]。
3.7 三联治疗
慢阻肺治疗的远期目标是降低死亡率。与单独使用LABA、LABA/LAMA和LABA/ICS相比,LABA/LAMA/ICS三联治疗可以改善患者的肺功能和症状,并减少急性加重。IMPACT研究是一项为期52周的随机、双盲、多中心大型临床试验,纳入10 355例慢阻肺患者,研究糠酸氟替卡松/维兰特罗/乌美溴铵(FLU/VI/UMEC)100/62.5/25 μg三联治疗、糠酸氟替卡松/维兰特罗(FLU/VI)100/25 μg和维兰特罗/乌美溴铵(VI/UMEC)62.5/25 μg双联治疗的疗效和安全性。主要终点为全因死亡率。FLU/VI/UMEC与VI/UMEC比较死亡风险比为0.72(95%CI:0.53~0.99),与FLU/VI比较死亡风险比为0.89(95%CI:0.67~1.16),心血管疾病和呼吸系统疾病的死亡率以及与慢阻肺相关的死亡率均较低。三联治疗在降低治疗期间年中/重度急性加重频率的主要终点和一系列临床重要终点(包括肺功能和健康相关生活质量)方面均优于其他两类双联治疗。
ETHOS研究是一项为期52周的Ⅲ期随机对照试验(randomized controlled trial,RCT),入选了8509例过去1年中至少发生1次急性加重的中重度慢阻肺患者,按1∶1∶1∶1比例随机分配,其中2137例患者吸入布地奈德/格隆溴铵/福莫特罗320/18/9.6 μg,2121例患者吸入布地奈德/格隆溴铵/福莫特罗160/18/9.6 μg,2120例患者吸入格隆溴铵/福莫特罗18/9.6 μg,2131例患者吸入布地奈德/福莫特罗320/9.6 μg,均为每日2次。320 μg布地奈德三联疗法急性加重频率显著低于格隆溴铵/福莫特罗(降低24%,95%CI:0.69~0.83)或布地奈德/福莫特罗(降低13%,95%CI:0.79~0.95)。另外,320 μg布地奈德三联疗法与格隆溴铵/福莫特罗比较死亡风险比为0.54(降低46%,95%CI:0.34~0.87)。在最终获取数据集中(包括99.6%的意向性治疗人群),320 μg布地奈德三联疗法与格隆溴铵/福莫特罗比较死亡风险比为0.51(降低49%,95%CI:0.33~0.80),与布地奈德/福莫特罗比较死亡风险比为0.72(降低28%,95%CI:0.44~1.16)。心血管疾病引起的死亡在320 μg布地奈德三联疗法与格隆溴铵/福莫特罗组的发生率分别为0.5%和1.4%。
ETHOS研究和IMPACT研究是2项大型的1年期RCT,在有频繁和/或重度急性加重病史的有症状患者中对比固定剂量吸入三联疗法与双联治疗的疗效和安全性。在这2项高质量的研究证据中(ETHOS研究为较高剂量ICS组),三联疗法组患者死亡率显著低于双支气管扩张剂组。这些患者既往接受过三联疗法、LABA/ICS或单或双长效支气管扩张剂维持治疗。进一步的分析或研究可能有助于确定其他特定的患者亚组是否显示出更大的生存获益[25-27]。
3.8 β受体阻滞剂
观察性研究表明,β受体阻滞剂可以降低中重度慢阻肺患者急性加重和死亡的风险,但这些结果尚未在RCT中得到证实。一项RCT研究将532例患者随机分为美托洛尔组和安慰剂组,患者年龄为(65.0±7.8)岁,FEV1占预计值百分比为(41.1±16.3)%。两组患者首次出现急性加重的中位时间比较差异无统计学意义(美托洛尔组为202 d,安慰剂组为222 d;95%CI:0.84~1.32),美托洛尔与慢阻肺急性加重导致住院的风险较高有关(HR=1.91;95%CI:1.29~2.83)。两组中可能与美托洛尔有关的不良反应发生率相似,非呼吸性严重不良事件的总发生率也相似。在治疗期间,美托洛尔组11例患者死亡,安慰剂组5例患者死亡。在无明确β受体阻滞剂使用指征的中度或重度慢阻肺患者中,与安慰剂相比,应用美托洛尔并不会延长首次急性加重的时间,并且在美托洛尔组急性加重所致的住院更常见。建议选择性β1受体阻滞剂仅用于治疗具有心血管适应证的慢阻肺,而不是仅仅为了预防慢阻肺急性加重[28]。
3.9 吸入技术和药物依从性
在哮喘和慢阻肺患者中,吸入技术错误、药物不依从是疾病控制欠佳的两种重要原因,需要多学科团队进行患者教育。一项荟萃分析纳入12项研究,评估药师主导的干预措施对哮喘和慢阻肺患者吸入技术、药物依从性的影响,发现药师主导的干预措施提高了慢阻肺和哮喘患者的药物依从性[1.34(95%CI:1.18~1.53)]和吸入技术[1.85(95%CI:1.57~2.17)],亚组荟萃分析中,仅在慢阻肺患者中发现药物依从性显著改善[1.41(95%CI:1.24~1.61)]。另外一项研究从低收入慢阻肺人群(主要是非裔美国人)中招募了重度慢阻肺患者282例。参与者被随机分配接受9个月的非医疗专业人员的健康指导或常规护理,研究结果为过去7 d自我报告对吸入药物的依从性和对操作步骤准确性的观察。与接受常规护理的患者相比,在9个月时,接受健康指导的患者自我报告对吸入药物的依从性天数更多(分别为6.4 d和5.5 d),并且有更多的患者在最近7 d内坚持吸入5 d(90%∶69%),吸入设备的完全掌握(24%∶7%)和掌握基本步骤(40%∶11%)均有显著优势。由药师主导的干预措施和健康指导可以改善慢阻肺患者的吸入技术和药物依从性[29,30]。
3.10 肺康复
3.10.1 经鼻高流量氧疗(high-flow nasal therapy,HFNT):在肺康复方面新增证据表明,与常规吸氧相比,在康复训练过程中给予HFNT可能改善慢阻肺患者的运动耐力,但仍需进一步研究评估。运动训练期间吸氧可以使慢阻肺患者耐受较高的活动水平,并减轻劳累性症状,最终改善其生活质量。一项荟萃分析纳入18岁以上不符合长期氧疗标准的慢阻肺患者,运动训练持续时间≥3周,每周至少进行2次训练。5项RCT符合纳入和排除标准,吸氧组能延长恒定功率运动训练的运动时长,加权平均差异为2.68 min(95%CI:0.07~5.28),平均运动时间由6 min增加至14 min,对照组由6 min增加至12 min。同时,恒定功率运动测试的Borg评分显著改善加权平均差异为-1.22单位(95%CI:-2.39~-0.06)。一项研究中穿梭步行试验后Borg评分显著改善了-1.46个单位(95%CI:-2.72~-0.19),但最大运动量、6 min步行距离、穿梭步行距离、健康相关生活质量或氧合状态比较差异均无统计学意义。表明运动训练期间吸氧能够改善慢阻肺患者的运动耐力和呼吸困难症状。但根据GRADE分级,纳入研究证据质量较低,需要进一步开展大规模研究。
通过测量膈肌压力、呼吸模式和气体交换等评估,HFNT与无创机械通气(noninvasive ventilation,NIV)均能够不同程度地改善高碳酸血症患者慢阻肺运动训练时的呼吸模式,可能在患者的长期治疗中发挥作用。对于低氧血症性慢阻肺患者,运动训练可以有效提高运动能力,不同的氧疗方式会有区别。在8家康复医院连续招募171例慢性低氧血症的慢阻肺患者,HFNT组和文丘里面罩(V-mask)组患者运动能力均显著提高,6 min步行距离组间差异显著(平均值:17.14 m;95%CI:0.87~33.43),但两组患者耐力时间比较差异无统计学意义(平均值:141.85 s;95%CI:-18.72~302.42)。HFNT组在耐力时间训练和6 min步行距离训练中达到最小临床重要差异的患者占比均高于V-mask组。与V-mask比较,HFNT并不能延长耐力时间,但能够有效增加步行距离。
肺康复的推荐疗程至少6周,但在许多国家受到保险公司和/或国家医保基金的限制。虚拟肺康复作为代替方式结合或不结合传统肺康复,可能被一些肺康复项目疗程限制少于4周的国家采用。使用非沉浸式虚拟现实(virtual reality,VR)训练的慢阻肺患者与传统肺康复计划相结合可能取得更好的效果,从而缩短肺康复项目疗程。研究招募106例慢阻肺患者,分别接受传统肺康复(34例)、VR训练(34例)以及二者结合的训练计划(38例),进行为期2周、每周5次的高强度治疗,传统肺康复计划包括健身运动、阻抗和放松训练。Xbox360®和Kinect®Adventures软件用于下半身和上半身的力量、耐力、躯干控制和动态平衡的VR训练。比较三组患者高级体能测验的差异。结果显示,传统肺康复+VR组患者曲臂、座椅站立、抓背、坐姿伸展、起立行走、6 min步行试验的训练结果均优于传统肺康复组。VR组患者曲臂、座椅站立、6 min步行试验的训练结果均优于传统肺康复组。结果表明,传统肺康复计划结合VR训练能够在多方面优化训练结果,是改善慢阻肺患者预后的有效措施[31-35]。
3.10.2 自我管理:因慢阻肺急性加重住院的患者具有较高的再住院率,且生活质量降低,改善近期急性加重出院后的慢阻肺患者的长期自我管理对预后的影响有待阐明。240例因慢阻肺住院患者被随机分为干预组和常规护理组,护士通过标准化工具为干预组患者及其家庭护理者提供有关慢阻肺自我管理的特殊培训,培训为期3个月,并且在出院30 d内提供过渡支持。结局指标为6个月时发生的慢阻肺相关急性护理事件(住院和急诊就诊)的数量和圣乔治呼吸问卷(St.George's respiratory questionnaire,SGRQ)评分。干预组在6个月时与慢阻肺相关急性护理事件的平均数为1.40(95%CI:1.01~1.79),而常规护理组为0.72(95%CI:0.45~0.97)。干预组在6个月时SGRQ总得分的平均变化为2.81,而常规护理组为-2.69。与常规护理相比,接受特殊培训并进行长期自我管理的慢阻肺患者在出院后6个月内的慢阻肺相关住院和急诊就诊次数显著增加。这些数据表明,与常规护理相比,近期住院患者的自我管理策略可能导致医疗资源利用率升高[36]。
3.10.3 针灸:非药物疗法是缓解呼吸困难的有效策略。针灸对缓解早期慢阻肺患者的呼吸困难有效,但对于疾病晚期患者的疗效尚未知。一项荟萃分析纳入关于针灸和指压12项研究597例患者(347例慢阻肺、190例晚期癌症),发现针灸组患者呼吸困难严重程度均显著改善[10项研究480例患者;标准平均差(standard mean difference,SMD)=-1.77;95%CI:-3.05~-0.49;P=0.007;I2=90%],与假针灸且治疗持续时间至少3周的亚组比较仍有差异(6项研究302例患者;SMD=-2.53;95%CI:-4.07~-0.99;P=0.001;I2=91%),同时,针灸组患者的运动耐力(6 min步行距离)显著改善(6项研究287例患者;SMD=0.93;95%CI:0.27~1.59;P=0.006;I2=85%)。在6项研究中有4项研究的针灸组患者生活质量得到了改善。针灸可以改善疾病晚期患者的呼吸困难严重程度、运动耐力和生活质量。但研究本身存在的局限性有待进一步解决[37]。
3.10.4 呼吸支持:NIV能降低慢阻肺患者的死亡率和住院风险,但是家庭NIV与慢阻肺高碳酸血症的结局之间的关联尚不确定。一项荟萃分析纳入21项RCT和12项观察性研究,包含使用家庭NIV超过1个月的伴有高碳酸血症的51 085例慢阻肺成人患者。与不使用NIV相比,使用双水平气道正压通气(bilevel positive airway pressure,BiPAP)的患者死亡(95%CI:-10.29%~-0.76%)和住院风险(95%CI:-49.39%~-21.12%)均显著降低,且插管需求较少(95%CI:-14.77%~-1.28%);而使用家庭NIV的患者全因住院率显著降低(95%CI:0.35~0.71),不良事件发生率比较差异无统计学意义。对于伴有高碳酸血症的慢阻肺患者,BiPAP能够降低患者的死亡和住院风险,减少插管需求,家庭NIV能够降低患者住院率,但二者对患者生活质量的改善均不明显。NIV可降低死亡和住院风险,但最为适合的患者人群[按近期住院史或动脉血二氧化碳分压(partial pressure of carbon dioxide in arterial blood,PaCO2)进行分层]仍有待进一步研究[38]。
第四章:稳定期慢阻肺的管理
关键点
- 稳定期慢阻肺的管理策略应主要基于症状的评估和未来急性加重的风险。
- 应大力鼓励和支持所有吸烟者戒烟。
- 主要治疗目标是减轻症状和降低未来急性加重的风险。
- 管理策略包括药物和非药物干预。
更新要点
GOLD 2021药物治疗的初始治疗原则和随访管理与GOLD 2020相同。将慢阻肺治疗推荐方案细化为诊断、初始评估、初始管理、回顾、调整。起始治疗在缺乏高质量证据的情况下,按照ABCD分组进行药物推荐。随访治疗不再依据ABCD分组推荐用药,而是依据可治疗的特征将患者分为呼吸困难和急性加重两类进行治疗调整,对于急性加重次数多的患者同时考虑其血EOS数量,推荐相应包含ICS的治疗。GOLD 2021增加了新型冠状病毒肺炎(corona virus disease 2019,COVID-19)疫情暴发流行需要修改肺康复的操作流程,项目的开展应保持社交距离。居家结合远程监督的肺康复训练方案可能促进患者出院后早期肺康复训练的开展,同时也更加经济。
4.1 慢阻肺的管理循环
GOLD 2021与GOLD 2020相同,纳入了完整的慢阻肺管理流程图,包括初始评估、初始管理、随访评估和随访治疗调整,提升了指南的临床可用性。该管理流程是基于患者症状严重程度和急性加重风险制订的,临床医生可根据患者病情进行升级或降级治疗(图1)。这些管理建议结合了RCT证据和专家的临床经验用以支持临床决策。
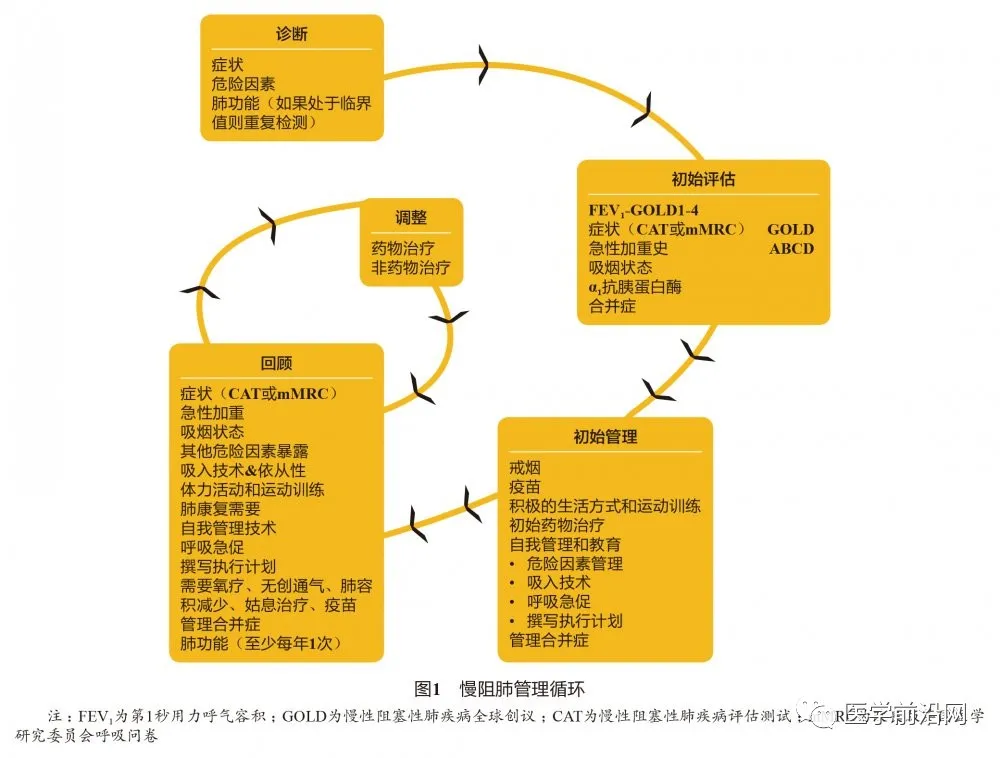
4.2 慢阻肺初始药物治疗和随访期药物治疗 同GOLD 2020(图2、图3)。
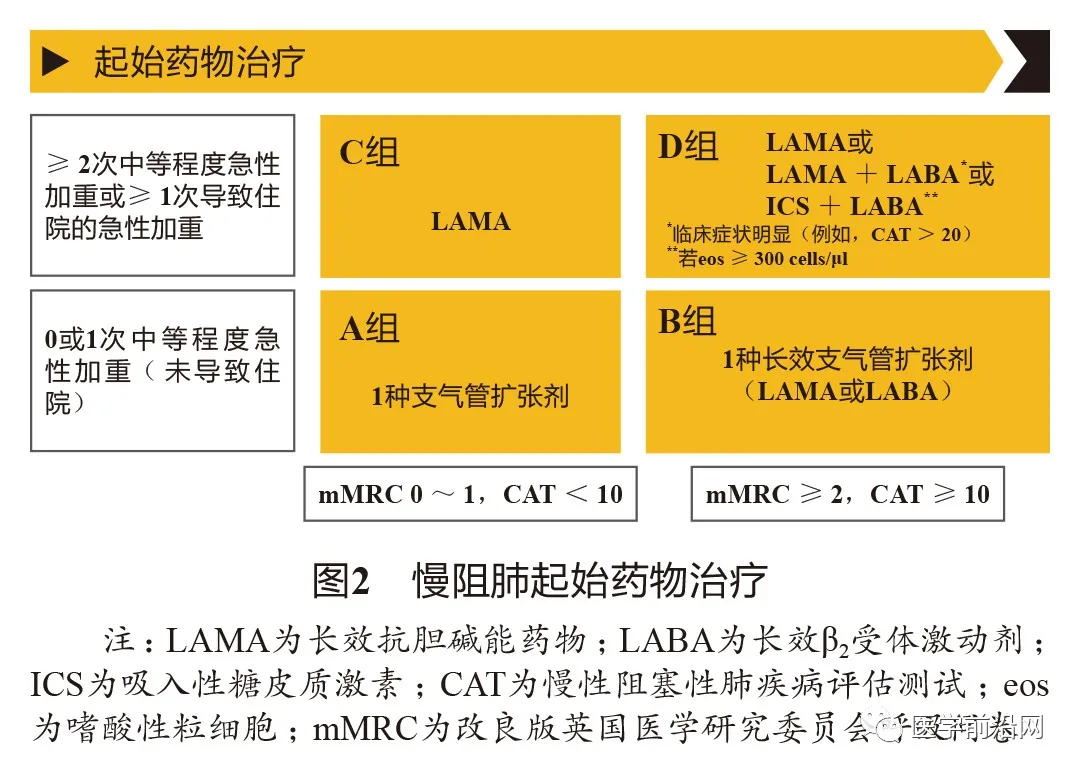
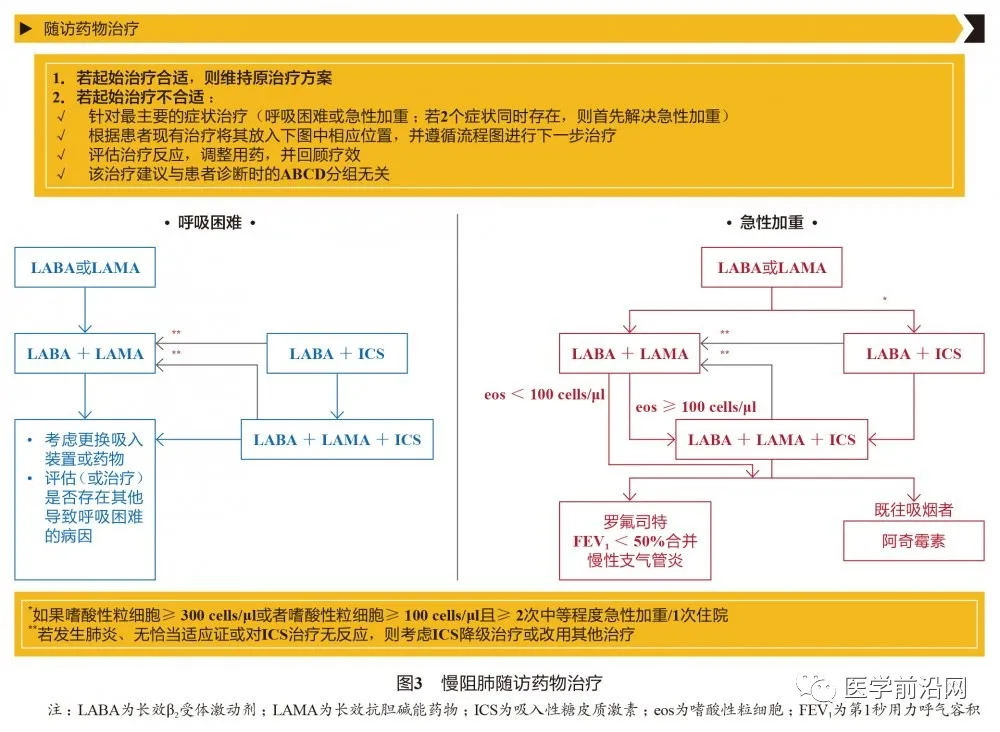
4.3 体育锻炼
缺乏体育锻炼与慢阻肺的不良预后相关。但是目前尚无大规模的基于人群的临床研究证实体育锻炼能够降低慢阻肺急性加重事件发生风险和死亡率。在美国南加州8家医疗中心募集2707例有慢阻肺急性加重史的患者,将其随机分为体育活动干预组和标准治疗组,进行为期12个月的随访。体育活动干预组根据患者实际的活动耐受能力行走步数监测,半自动步数目标推荐,个体化强化及家庭支持;标准治疗组仅为常规管理。评估的主要结局指标包括全因住院率、急诊就诊率、死亡率,次要结局指标包括体育锻炼自我报告率、慢阻肺相关的急性加重护理使用率、临床症状、生活质量、心血管代谢指标(血压、糖化血红蛋白、血脂)等。研究发现,体育活动干预组和标准治疗组患者主要结局指标和次要结局指标比较差异均无统计学意义。该研究表明,社区体育锻炼指导干预措施尚不能改善有慢阻肺急性加重史的患者慢阻肺相关的急性加重护理使用率和生存率[39]。
美国另一项基于网络技术的体育锻炼干预措施的前瞻性研究纳入稳定期慢阻肺患者109例,进行为期15个月的随访。将入选患者随机分为对照组(只有计步器)和试验组(计步器联合网络反馈、目标设定、疾病教育、社区干预)。每3个月评估1次急性加重事件,分别于入组时、随访6个月、随访15个月和干预结束后3个月评估每日步数计量、健康相关及生活质量(health related quality of life,HRQL)、自我效能感。通过研究发现,试验组患者急性加重风险较对照组降低(OR=0.51;95%CI:0.31~0.85),然而两组患者的年龄、FEV1预计值、行走步数基线、入组前1年急性加重事件和随访持续时间比较差异均无统计学意义[40]。
4.4 居家肺康复与早期肺康复
GOLD明确指出,肺康复训练作为慢阻肺规范化管理的一部分,能够提高患者的活动耐量、改善临床症状及生活质量等。但是,对于慢阻肺患者来说,肺康复训练也是一项不小的经济负担,慢阻肺康复场所和康复时机一直是研究的热点。COVID-19暴发流行导致需要修改肺康复的操作流程,项目的开展应保持社交距离。以家庭为基础的肺康复计划与远程监督可能促进出院后更早的随访,且可能是高性价比的。澳大利亚一项RCT比较了稳定期慢阻肺患者基于康复中心的8周肺康复训练和基于家庭的新型肺康复训练的成本效益及效用。患者分别于计划开始前、完成时和完成后12个月接受临床评估,比较了效用[基于SF6D效用评分计算质量调整生命年(quality-adjusted life year,QALY)]、效益(基于6 min步行距离的变化)和成本(基于医疗部门和政府数据库统计的康复后1年个人花费)。根据成本效益及效用分析发现,居家模式的肺康复训练在成本效益和效用方面更优,成本低效益高占63%,有意愿支付居家肺康复模式占78%。说明基于家庭的新型肺康复训练可能成为无法参与医疗中心为基础康复计划的慢阻肺患者的一种经济有效的替代模式[41]。
一项分析轻度慢阻肺与家庭肺康复训练关系的RCT共纳入58例轻度慢阻肺患者(FEV1/FVC<70%;FEV1>80%预计值),随机分为家庭肺康复组和标准护理组,进行为期8周的家庭肺康复训练或标准护理。比较6 min步行距离和改良版英国医学研究委员会呼吸问卷(modified version of British Medical Reseach Council dyspnoea scale,mMRC)和慢性呼吸道疾病问卷(chronic respiratory disease questionnaire,CRQ)得分。研究发现,两组患者的活动耐力、临床症状和生活质量均得到改善,但6 min步行距离在干预结束时(MD=-3 m,95%CI:-64~58)和干预6个月后(MD=7 m,95%CI:-59~72)并无明显差异。随访6个月后,家庭肺康复训练患者CRQ中情绪有改善(家庭肺康复组50%,对照组0)。家庭肺康复训练和标准肺康复训练均能改善患者的活动耐力、临床症状和生活质量,且家庭肺康复训练更能改善患者的情绪[42]。
一项慢阻肺急性加重后早期肺康复训练与慢阻肺稳定期后进行肺康复训练的前瞻性研究比较了患者的死亡率、入院率、身体活动能力和生活质量。该研究共纳入150例因慢阻肺急性加重入院治疗的患者。随机分为出院后2周内进行肺康复训练组和2个月后处于稳定期时进行肺康复训练组。研究发现,与稳定期康复训练相比,早期肺康复训练并未延长首次入院时间或死亡时间(HR=0.79;95%CI:0.47~1.23),慢阻肺评估测试亦无显著差异(1.43,95%CI:-3.44~0.59);但是干预2个月后,早期肺康复训练患者增量往返步行试验较稳定期康复训练患者明显改善(33.9 m,95%CI:4.18~63.7);耐力往返步行试验具有临界意义(140 s,95%CI:-2.03~282.76)。在慢阻肺急性加重后早期进行肺康复训练虽然不能改善患者生存率和住院时间,但是可使慢阻肺患者身体活动能力得到快速改善[43]。
第五章:慢阻肺急性加重的管理
关键点
- 慢阻肺急性加重定义为导致额外治疗的呼吸道症状严重恶化。
- 由于慢阻肺症状具有非特异性,应考虑相关的鉴别诊断。
- 慢阻肺急性加重可由多种因素引起,最常见的原因是呼吸道感染。
- 慢阻肺急性加重的治疗目标是尽量减少本次急性加重造成的不良影响,并预防未来急性加重的发生。
- 单用短效β2受体激动剂,联用或不联用短效抗胆碱能药物,推荐为慢阻肺急性加重的初始治疗。
- 长效支气管扩张剂的维持治疗应在出院前尽快开始。
- 全身性糖皮质激素可改善肺功能和氧合作用,并缩短恢复时间和住院天数,治疗时间不应超过5~7 d。
- 抗生素治疗可以缩短恢复时间,降低早期复发、治疗失败和住院天数增加的风险,治疗时间应为5~7 d。
- 甲基黄嘌呤会增加不良反应,不推荐使用。
- NIV是慢阻肺急性呼吸衰竭无绝对禁忌证患者的首选通气方式,因其可以改善气体交换,减少呼吸功和插管,缩短住院天数,提高生存率。
- 急性加重发生后应采取适当措施预防急性加重。
更新要点
GOLD 2021增加了WHO慢阻肺急性加重的最低限度干预措施,不建议使用降钙素原(procalcitonin,PCT)方案来决定慢阻肺急性加重患者是否应使用抗生素,需要通过严谨的方法进行验证研究。样本小、患者的异质性以及随访时间短是目前在解释HFNT对慢阻肺患者总体价值方面的局限性。病情恶化的原因、严重程度、影响、治疗和时间进程因患者而异,社区设施和医疗系统因国而异。导致短期再入院和全因死亡率增加的反复恶化与急性恶化的首次住院有关。一项系统评价显示,慢阻肺急性加重患者住院后,合并症、既往病情加重、住院和住院时间延长是30 d和90 d全因再入院的重要危险因素。此外,与出院后短时间相比,动脉氧饱和度和血气分析将在长期随访方面更精确地决定是否需要长期氧疗。
5.1 WHO定义了中低收入国家基层医疗机构慢阻肺急性加重的最低限度干预措施
如果急性加重有感染的证据,应给予抗生素治疗。严重急性加重给予口服泼尼松龙30~40 mg,疗程7 d。雾化吸入大剂量沙丁胺醇,或者使用带有储物罐的定量吸入装置(1 h内每20分钟4喷)。根据需要给予氧疗,吸氧浓度控制在24%~28%。
5.2 PCT指导慢阻肺急性加重抗生素使用研究
2020年GOLD报告指出,PCT可以辅助制订慢阻肺急性加重初始抗生素治疗方案。然而,美国一项系统回顾及荟萃分析评估了应用PCT指导慢阻肺急性加重时抗生素处方治疗,研究发现,PCT可以将慢阻肺急性加重患者抗生素使用时间减少2.01 d;但是对住院时间、治疗失败、全因死亡率等临床预后无明显影响。然而,慢阻肺急性加重时,大多数患者血液PCT水平低于使用抗生素的临界值,而且将PCT作为生物标志物与重症监护病房患者更差的预后相关。此外,根据补充的敏感性分析(排除高风险偏倚或具有转换结果值),PCT对RCT中抗生素持续使用时间的影响无统计学意义(MD=-1.88 d,95%CI:-3.95~0.19,P=0.08和MD=-1.72 d,95%CI:-4.28~0.83,P=0.19)。目前不推荐应用PCT指导慢阻肺急性加重的抗生素治疗,仍需要通过严谨的方法进行验证研究[44]。
5.3 慢阻肺与呼吸支持
越来越多的证据支持使用HFNT治疗急性呼吸衰竭,特别是慢阻肺患者。但是,目前缺乏研究数据证明HFNT在稳定期慢阻肺患者中的作用。美国一项系统回顾及荟萃分析共纳入6项RCT(共339例慢阻肺患者)分析比较了经鼻高流量吸入空气或氧气与不经此设备吸入相同气体对慢阻肺患者的作用。研究发现,HFNT可以降低患者长期和短期PaCO2(长期有2项研究,MD=-3 mmHg,95%CI:-4~-2;短期有2项研究,MD=-3 mmHg,95%CI:-4~-2);同时,HFNT可以显著提高患者的生活质量(2项研究,MD=-5,满分为100分,95%CI:-8~-2)、降低1年急性加重频率(1项研究,比率为0.6,95%CI:0.6~0.7)。但研究发现,HFNT未能显著改善患者的活动能力及降低住院率和死亡率,但是可以改善呼吸方式。说明HFNT有潜在的降低稳定期慢阻肺患者的PaCO2、减少急性加重频率及改善患者短期和长期生活质量的能力,特别是对不能配合NIV的患者,但是这需要更多的研究证据支持[45]。
5.4 慢阻肺住院患者出院后家庭氧疗再评估
慢阻肺急性加重相关低氧血症通常会随着时间延长而减轻,当前指南建议,近期出院的进行家庭氧疗的患者,未经评估低氧血症就不应更新处方。一项研究纳入5家退伍军人事务部的慢阻肺住院患者,主要结果是在出院90 d内通过血氧饱和度监测确定家庭氧疗再评估的频率,次要结果包括潜在的有停用氧疗指征的患者比例。研究发现,有43.6%的队列完成了90 d内再评估。根据Medicare指南,近50%完成重新评估的患者有资格终止治疗(43.2%;n=124/287);当使用LOTT提供的最新证据时,大多数队列没有静息性低氧血症(84.3%;n=393/466),可以停止家庭氧疗。上述研究说明,慢阻肺出院患者长期家庭氧疗的必要性再评估不足,而在研究中完成再评估的人群大多数没有静息性低氧血症,可以终止家庭氧疗,提高家庭氧疗的质量和价值[46]。
5.5 慢阻肺急性加重出院后再入院危险因素分析
目前研究发现,慢阻肺患者急性加重住院治疗后再入院率居高不下,患者再入院率与多种因素相关。一项荟萃分析共检索3533篇论文摘要,最终纳入14篇研究共3 792 506例患者。分析发现慢阻肺急性加重患者出院后30 d、90 d再入院率分别为8.8%~26.0%、17.5%~39.0%。其中合并症、既往急性加重住院史和首次住院时间延长是患者30 d和90 d再入院的主要危险因素。调整后OR显示心力衰竭[1.29(1.22~1.37)]、肾衰竭[1.26(1.19~1.33)]、抑郁症[1.19(1.05~1.34)]和饮酒[1.11(1.07~1.16)]与30 d全因再入院风险增加相关,而女性为保护因素[0.91(0.88~0.94)]。需要深入了解慢阻肺急性加重风险的复杂生物学机制,以便早期识别和管理[47,48]。
第六章:慢阻肺合并症
关键点
- 慢阻肺常合并其他疾病,对预后有显著影响。
- 总体来说,合并症的存在不应改变慢阻肺的治疗方案,并且合并症应按照常规标准进行治疗,而与慢阻肺的存在无关。
- 肺癌常见于慢阻肺患者中,是导致患者死亡的主要原因。
- 心血管疾病是慢阻肺常见且重要的合并症。
- 骨质疏松和抑郁/焦虑是慢阻肺常见的重要合并症,常被漏诊,并与不良的健康状况和预后相关。
- 胃食管反流与慢阻肺急性加重风险增加和健康状况差有关。
- 当慢阻肺是多种疾病护理计划的一部分时,应注意确保治疗的简便性并最大限度地减少多药物治疗。
更新要点
GOLD 2021在合并症方面关注慢阻肺合并肺癌患者的预后和慢阻肺患者的认知功能。
6.1 慢阻肺与肺癌
GOLD 2021增加了慢阻肺与肺癌的新章节。肺癌死亡人数超过结肠癌、乳腺癌和前列腺癌的总和,全球每年估计有160万人死于肺癌。不幸的是,绝大多数肺癌确诊时已处于晚期,导致患者总体存活率很低。因此,初级和二级预防以及早期发现对于提高患者存活率非常重要。国际癌症研究机构的GLOBOCAN系列现已统计了27种主要癌症以及2012年所有癌症的全球发病率和死亡率的估计值,总体而言,2012年有1410万新病例,死亡820万例。最常见的癌症是肺癌(182万例)、乳腺癌(167万例)和结直肠癌(136万例)。癌症死亡的最常见原因是肺癌(160万例死亡)、肝癌(74.5万例死亡)和胃癌(72.3万例死亡)。
有证据表明慢阻肺和肺癌之间存在联系,这一点已经在几项流行病学和观察性队列研究中得到了系统的证实。这两种疾病的共同起源似乎不仅是烟草暴露,遗传易感性、DNA甲基化的表观遗传学改变、局部肺部慢性炎症和肺修复机制异常也被认为是肺癌发生的最重要的潜在因素。气流阻塞的严重程度是否与肺癌发生的更大风险直接或负相关仍存在争议。肺癌与肺气肿程度之间的相关性较肺癌与气流阻塞程度之间的相关性更强,并且在合并诊断为肺气肿的受试者中观察到最大的风险。肺癌的最好预防措施(如同对慢阻肺一样)是预防吸烟,吸烟者应戒烟。几项涉及使用低剂量胸部CT(low-dose chest computed tomography,LDCT)筛查的研究表明,老年人(年龄55~74岁)、目前吸烟者或在过去15年内戒烟且吸烟史至少30包年的人的存活率有所提高。这些研究对美国预防服务工作组(United State Preventive Services Task Force,USPSTF)支持每年进行肺癌筛查的建议具有决定性意义。一些研究表明,如果将年龄、吸烟史、体质指数、气流阻塞和/或肺气肿的存在以及肺癌家族史等其他变量添加到目前的筛查标准中,将会提高CT筛查的效率。
在可能的情况下实施筛查计划可能是有用的,但必须在适当的环境中实施,以避免过度诊断、更高的发病率和死亡率,以及对良性异常、焦虑和不完全随访的不必要诊断程序。另外,丹麦的一项研究表明,作为肺癌筛查计划的一部分,显著促进戒烟,以及对不同研究的回顾得出结论,在LDCT筛查期间戒烟可以改善肺活量,减少微结节。因此,对肺癌和慢阻肺有利。戒烟干预作为CT筛查计划的一部分可能是有用的(表1)。

鉴于慢阻肺和肺癌的密切关系,一项多中心前瞻性随访研究共纳入2994例非小细胞肺癌并经外科手术切除的患者进行肺功能检查,以明确是否合并慢阻肺。通过计算总生存率和条件生存率(手术后2年、3年或5年生存可能性)以及肺功能受损程度(FEV1%百分比)建立预后模型。研究发现无论是否合并慢阻肺,所有患者的总生存率相似。然而条件生存率在随访的60个月的每个阶段均不同,在24~36个月的生存率差异具有统计学意义。极重度肺功能受损是肺癌合并慢阻肺患者预后不良的危险因素。非小细胞肺癌经手术切除后,无论是否合并慢阻肺,总生存率无明显差异,但是条件生存率并不相同,术后2年合并慢阻肺患者的生存率差异有统计学意义,慢阻肺可被视为预后不良的危险因素,且与肺功能受损的严重程度相关[49-68]。
6.2 慢阻肺急性加重与心脑血管疾病死亡率
慢阻肺急性加重可能伴随心脑血管疾病的恶化。目前研究证明,慢阻肺急性加重患者急性心脑血管疾病发病率增加。中国台湾一项前瞻性研究纳入慢阻肺患者进行为期13年的随访研究,研究发现,慢阻肺急性加重住院与急性心肌梗死(OR=1.33;95%CI:1.24~1.43)、缺血性脑卒中(OR=1.33;95%CI:1.24~1.43)、脑出血(OR=1.19;95%CI:1.06~1.32)90 d死亡率独立相关;慢阻肺急性加重住院与急性心肌梗死(HR=1.23;95%CI:1.19~1.27)、缺血性脑卒中(HR=1.29;95%CI:1.26~1.33)、脑出血(HR=1.19;95%CI:1.13~1.26)的总体死亡率相关;且与对照组相比,慢阻肺急性加重的次数越频繁,上述心脑血管疾病患者90 d总体死亡风险越高[69]。
6.3 慢阻肺患者高敏肌钙蛋白浓度与心血管事件及其发生风险
慢阻肺与心血管事件高风险有关,一项随机双盲对照试验共纳入16 485例慢阻肺合并心脑血管疾病或有心脑血管疾病高危因素的患者,将其随机分为安慰剂组、糠酸氟替卡松吸入组、维兰特罗吸入组,对其中1599例患者进行血浆高敏肌钙蛋白检测。研究发现,在所有检测的患者中,1542例(96%)患者的高敏肌钙蛋白I水平高于检测极限,在3个月时吸入制剂不影响高敏肌钙蛋白I的血浆浓度。血浆肌钙蛋白I浓度处于最高1/5的患者较血浆肌钙蛋白I浓度处于最低1/5的患者心血管事件的发生风险更高(HR=3.7;95%CI:1.3~10.1)、心血管疾病死亡率更高(HR=20.1;95%CI:2.4~165.2);相比之下,慢阻肺急性加重频率没有明显差异(HR=1.1;95%CI:0.8~1.5)。血浆肌钙蛋白I的浓度与患者心血管疾病发生和死亡率相关,吸入药物对肌钙蛋白的浓度没有明显影响[70]。
6.4 慢阻肺与认知损害
认知损害(cognitive impairment,CI)在慢阻肺患者中常见,平均患病率为32%,患病率和严重程度因评估类型而异。广泛的神经心理学测试提示高达56%的患者可能患有CI。中国中年慢阻肺患者CI的发生风险更高,慢阻肺与痴呆的发展有关。肺功能检查不同严重程度患者都可能患有CI。CI与基本日常生活活动受损相关,并与健康状况不良有不同程度的相关性。因慢阻肺急性加重住院治疗的患者,CI与疾病的严重程度和急性加重期间住院时间增加有关,且患者出院后CI难以恢复。与独立的慢阻肺或CI患者相比,慢阻肺与CI共存的患者呼吸系统相关住院率升高48%,死亡率升高3倍。因此对两种疾病的规范化管理尤为重要。CI对慢阻肺患者的健康产生负面影响,低氧血症和炎症,生活方式,饮食不足和缺乏体育活动,以及合并症如阻塞性睡眠呼吸暂停和抑郁,可能会协同促进慢阻肺患者CI的发生。慢阻肺合并CI的患者需要额外的帮助应对日常生活、治疗依从性及有效的自我管理,个体化的筛查和干预措施可能会改善慢阻肺患者的CI,但这需要进一步研究[71-82]。
第七章:新型冠状病毒疫情防控期间慢阻肺患者的管理
关键点
- 慢阻肺患者如果出现新的或加重的呼吸系统症状,如发热和/或任何其他可能与COVID-19相关的症状,即使这些症状较轻,也应该检查是否可能感染了严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)。
- 患者应按照医嘱继续使用口服和吸入性药物治疗慢阻肺,因为没有证据表明在COVID-19大流行期间应该改变慢阻肺治疗药物。
- 在社区COVID-19高流行期间,肺功能检查应限制使用,仅限紧急或必须通过检查以诊断慢阻肺的患者,和/或评估介入治疗或手术患者的肺功能状态。
- 物理上的距离和防护,或适当的隔离,不应导致社会孤立和不活动。患者可通过远程沟通方式与朋友和家人保持联系,继续保持活动,并应该确保他们有足够的药物。
- 应鼓励患者使用权威可信的资源获取有关COVID-19及其管理的医疗信息。
- 远程(电话/虚拟/在线)对慢阻肺患者进行随访指导,并提供打印清单。
更新要点
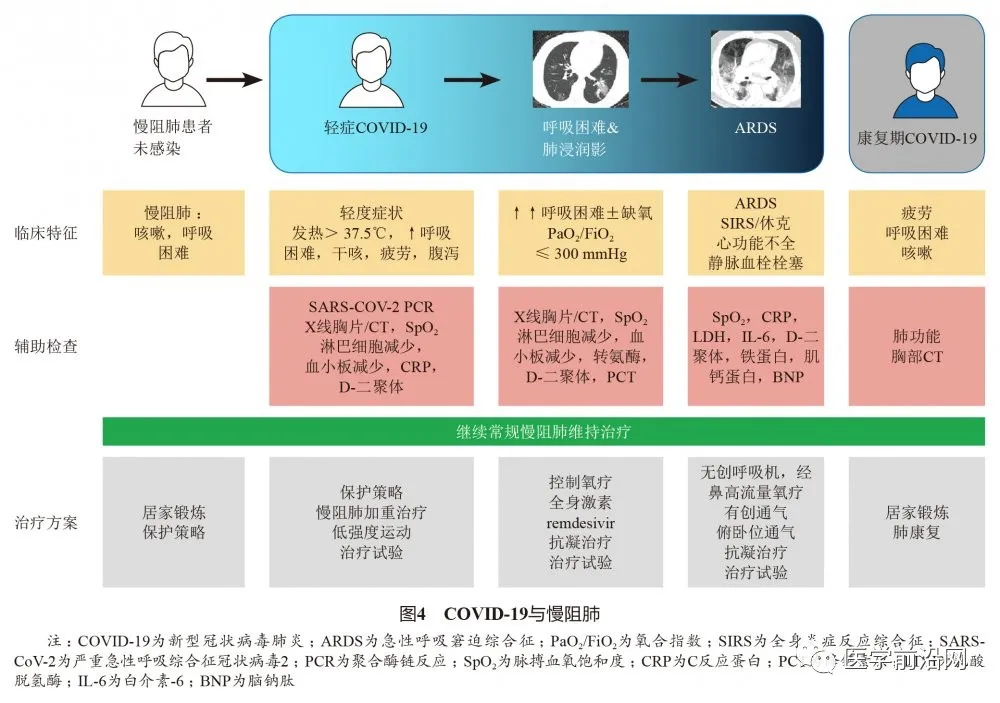
GOLD 2021新增关于慢阻肺和COVID-19的章节,包括新增的表格(表2和表3)、1个新的图(图4)和168篇文献。SARS-CoV-2大流行引出了许多关于慢阻肺患者管理的问题,以及是否需要对其治疗方案进行修改。GOLD科学委员会利用已有的文献综述方法,概述了COVID-19大流行期间对慢阻肺患者的管理。


7.1 慢阻肺患者感染SARS-CoV-2的风险
根据小样本和不完整共患病数据显示,COVID-19住院患者慢阻肺患病率低于人群患病率,然而大型研究显示,住院患者慢阻肺患病率高达19%,是COVID-19住院的独立危险因素(HR=1.55;95%CI:1.46~1.64)。部分研究发现慢阻肺增加重症或死亡的风险,多种因素造成不良结局风险增加,包括治疗依从性差、COVID-19大流行期间难以进行自我管理、获得医疗保健的机会有限、呼吸储备减少。在COVID-19住院患者中,吸烟与疾病严重程度和死亡风险相关。综上所述,根据现有证据,慢阻肺患者感染SARS-CoV-2的风险似乎并未显著增加,但这可能反映了保护性策略的效果,COVID-19大流行期间慢阻肺住院率下降,因COVID-19住院的风险增加,患严重疾病和死亡的风险也可能增加。
7.2 SARS-CoV-2的检测
慢阻肺患者出现呼吸道症状、发热或其他提示SARS-CoV-2感染的症状,即使症状轻微,也应检测SARS-CoV-2病毒核酸,必要时连续取样。如果慢阻肺患者接触过已知COVID-19感染的人群,应该联系自己的医疗服务人员,确定是否需要进行特定检测,感染后期可进行抗体检测。根据患者年龄、季节或临床环境,除了对SARS-CoV-2进行检测外,还应对其他呼吸道病原体进行检测,对疑似复发或复发的COVID-19患者应进行重复检测。
7.3 肺功能检查
在COVID-19高度流行社区,肺功能检查应仅限于紧急或必需检测以诊断慢阻肺患者,和/或通过肺功能状态评估介入治疗或外科手术的患者。在可能的情况下,患者应进行SARS-CoV-2的实时荧光定量聚合酶链反应(realtime polymerase chain reaction,RT-PCR)测试,检测呈阳性的患者肺功能检查通常应该推迟,直至检测为阴性。当常规肺活量测定无法使用时,家用PEFR结合患者问卷调查可用于支持或排除慢阻肺的可能诊断,但其特异性较低。也可以通过电子便携肺量计,使用视频技术进行指导。
7.4 支气管镜检查
在COVID-19大流行期间,一些慢阻肺患者可能需要进行诊断和治疗性支气管镜检查。PCR检测阴性可以行择期支气管镜检查。在COVID-19感染状况不明的紧急病例中,应将所有病例视为阳性处理,必要时可使用一次性支气管镜,工作人员应穿戴个人防护装备。
7.5 影像学
X线胸片对轻度或早期SARS-CoV-2感染不敏感,不作为无症状COVID-19的常规筛查,可以帮助排除或确诊其他疾病(如大叶性肺炎、气胸或胸腔积液)。床旁肺部超声也可用于检测COVID-19的肺部表现。推荐使用CT作为COVID-19诊断和严重程度评估的一部分,与非慢阻肺患者相比,合并COVID-19的慢阻肺患者CT结果显示磨玻璃影、斑片状影和间质异常的发生率更高。CT的可及性可能受感染控制要求的限制。COVID-19患者深静脉血栓形成和肺血栓栓塞的发生率增加,如果怀疑有肺栓塞,应进行CT肺动脉造影。
7.6 慢阻肺患者的保护策略
慢阻肺患者应采取基本的感染防控措施,包括保持社交距离和洗手,以帮助预防SARS-CoV-2感染。佩戴口罩或面罩可降低感染传播的风险,即使是重度气流受限的患者,佩戴外科口罩似乎也不会影响换气,但N95口罩会对患者产生不利影响,在大多数情况下,建议使用更宽松的口罩,甚至是面罩。除非必要,否则慢阻肺患者应该避免旅行,必要时补充氧气。如果FEV1<50%,mMRC≥3,有急性加重住院史,或需要LTOT或NIV的慢阻肺患者应特别注意加强防护,并开展呼吸康复训练。应制订行动计划,确保食品、药品、氧气、支助性保健服务和其他基本必需品的供应。
7.7 区分COVID-19与慢阻肺的日常症状
超过60%的COVID-19患者出现咳嗽和呼吸困难,通常还伴有发热、疲劳、意识模糊、腹泻、恶心、呕吐、肌肉疼痛、嗅觉缺失、神经功能障碍和头痛。慢阻肺患者症状加重,特别是伴有发热、味觉或嗅觉受损、胃肠道不适的患者,需要警惕COVID-19。在SARS-CoV-2检测呈阳性14~21 d后,仅65%的患者恢复到以前的健康水平,一些患者咳嗽、疲劳和呼吸困难持续数周,少数患者持续数月(图4)。
7.8 COVID-19大流行期间慢阻肺的维持药物治疗
在COVID-19大流行期间,没有确凿的数据支持改变慢阻肺的维持药物治疗以降低COVID-19发生风险,或者因为担心药物治疗可能增加COVID-19发生风险。同样,没有关于激素、长效支气管扩张剂LAMA或LABA、罗氟米司特、大环内酯在慢阻肺患者中的使用和SARS-COV-2感染的临床结果/风险的数据。因此,慢阻肺患者应该继续服用治疗慢阻肺所需的药物。
7.9 雾化吸入治疗
气溶胶疗法增加了飞沫的产生和疾病传播的风险,如有可能,应使用定量气雾吸入装置(pressurized metered-dose inhalers,pMDIs)、干粉吸入装置(dry powder inhalers,DPIs)和软雾吸入装置(soft mist inhalers,SMI)代替雾化吸入给药。避免在其他人在场的情况下使用雾化器,并确保雾化器在开窗或空气流通的地方使用。接受呼吸支持的COVID-19重症患者可能需要雾化吸入治疗,为了保持呼吸回路的完整和防止病毒的传播,推荐使用筛网雾化器。
7.10 在COVID-19大流行期间的慢阻肺非药物治疗
在COVID-19大流行期间,慢阻肺患者应继续进行非药物治疗。患者应该每年接种流感疫苗,不适合在中心进行康复治疗,基于网络或智能手机的应用程序可能有助于在COVID-19大流行期间支持家庭康复。遵循当地指导应用的感染控制的一般原则。
7.11 慢阻肺患者在COVID-19大流行期间的随访
为了最大限度地减少SARS-COV-2传播,尽量减少面对面的访视,建议使用在线、电话和视频的远程咨询,为患者制订访问日程,并提供一个标准化的随访清单。
7.12 慢阻肺患者COVID-19的治疗
针对COVID-19的临床试验集中在抗病毒药物和抗炎治疗上,包括抗病毒药物remdesivir和用于重症COVID-19患者的全身激素治疗,合并COVID-19的慢阻肺患者应该使用与其他COVID-19相同的治疗方案。
7.13 慢阻肺急性加重
预防和治疗急性加重是慢阻肺管理的重要目标。COVID-19使预防和管理慢阻肺急性加重面临困难。冠状病毒是引起慢阻肺急性加重的呼吸道病毒之一,目前为止,在慢阻肺急性加重患者中尚无中东呼吸综合征冠状病毒(middle east respiratory syndrome coronavirus,MERS-CoV)、SARS-CoV和SARS-CoV-2感染的报道。如怀疑感染COVID-19,应进行RT-PCR检测。如果确认COVID-19感染,则无论是否存在慢阻肺,都应进行COVID-19感染的治疗。SARS-COV-2感染引起血管损伤、低氧血症相关的肺炎、凝血障碍、全身炎症(「细胞因子风暴」)和多器官损伤,这些特征与典型的慢阻肺加重不同。然而,SARS-COV-2感染可能类似于慢阻肺急性加重。与慢阻肺急性加重相比,COVID-19发热、厌食、肌痛和胃肠道症状更常见,淋巴细胞显著下降。发生COVID-19的慢阻肺患者较非慢阻肺患者报告更严重的疲劳、呼吸困难和腹泻。在COVID-19患者中,淋巴细胞和血小板减少,D-二聚体、C反应蛋白、PCT、肌酸激酶、转氨酶、肌酐和乳酸脱氢酶水平升高与不良预后独立相关。
7.14 全身激素
对SARS-CoV和MERS-CoV感染患者的观察性研究提示,全身应用大剂量激素与提高生存率之间没有关联,但可引起骨坏死和病毒清除能力降低等不良反应。在COVID-19感染开始时不常规使用糖皮质激素,但下述2种情况除外:成人急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)和慢阻肺急性加重。6 mg/kg地塞米松治疗10 d可降低有创机械通气(invasive mechanical ventilation,IMV)或氧疗患者的死亡率,甲泼尼龙治疗可提高COVID-19合并ARDS患者的生存率,降低COVID-19患者28 d死亡率,特别是未使用有创机械通气或血管活性药物支持治疗的患者。无论是否有SARS-COV-2感染的证据,全身激素都应用于慢阻肺加重期,没有证据表明激素应用改变对SARS-COV-2感染的易感性或急性加重预后。
7.15 抗生素
如果慢阻肺患者出现呼吸困难、痰量增加、脓性痰3种主要症状中的2种,包括脓性痰增加,或需要机械通气,则提示患者需要应用抗生素治疗。在COVID-19中很少报告合并细菌感染。然而,COVID-19的严重程度增加了并发感染的风险,有高达46%的样本检测到细菌合并感染。在实践中,大多数住院患者,特别是重症患者都接受了经验性抗生素治疗。在地方/国家指南的指导下对重症COVID-19患者使用广谱抗生素,对临床怀疑为细菌感染的轻症COVID-19患者使用广谱抗生素,发生COVID-19的慢阻肺患者更经常发生细菌或真菌合并感染。
7.16 肺和肺外并发症
ARDS可能是COVID-19的主要病理改变,但COVID-19常见肺外侵犯,并导致发病率、残疾率和死亡率升高。肾脏、心脏、神经、皮肤、肝脏和胃肠道都可发生损伤,慢阻肺可加重这些损伤。与肺部病毒载量相比,肾脏、肝脏、心脏和大脑的SARS-CoV-2水平较低,提示这些器官是继发性而非原发性受累。
7.17 抗凝治疗
COVID-19可以引起高凝状态,尽管使用低分子肝素(low molecular weight heparin,LMWH)或普通肝素预防血栓形成,但ICU和病房患者的静脉血栓栓塞(venous thromboembolism,VTE)形成率仍较预期高出2~4倍。慢阻肺患者发生VTE的风险增加,因COVID-19住院的患者应接受抗凝治疗来预防血栓形成。LMWH较普通肝素更有利于减少工作人员暴露,临床医生应遵循当地的药物指南。
7.18 慢阻肺和COVID-19患者的呼吸支持
COVID-19患者低氧性呼吸衰竭的发生率约为19%,有20%的患者因严重低氧血症需要呼吸支持,约5%的患者需要住ICU。需要呼吸支持的患者死亡率高,慢阻肺增加呼吸衰竭和ICU住院的风险。在COVID-19导致的中重度低氧性呼吸衰竭住院患者中,IMV使用率存在较大差异(2.3%~33.0%)。HFNT显著降低了插管率和IMV使用率,对死亡率有不同的影响。对于急性低氧性呼吸衰竭,应优先考虑HFNT而非NIV,俯卧位通气建议用于清醒的非插管低氧血症患者。慢阻肺急性加重出现呼吸衰竭的患者常用NIV,NIV可能有利于治疗合并COVID-19肺炎的慢阻肺患者的呼吸性高碳酸血症,但其也有可能由于高跨肺压和潮气量而加重肺损伤。应密切监测HFNT或NIV患者的病情变化,根据需要及早插管行IMV,并采取保护性肺通气策略。氧合指数<150 mmHg可能是NIV失败和死亡风险增加的有用指标。只有在其他策略未能达到氧合或通气目标时,才应考虑体外膜氧合(extracorporeal membrane oxygenation,ECMO)。工作人员应该使用合适的个人防护装备,病毒过滤器安装在有创或无创通气设备的呼气口,建议使用隔离罩来进一步减少工作人员的接触。
7.19 康复
患有COVID-19的慢阻肺患者尤其容易发生营养不良和骨骼肌减少。因此,医院治疗应包括饮食支持和早期活动。机械通气、镇静、长时间卧床休息可导致创伤后应激障碍,以及呼吸功能下降、认知和精神障碍。老年人和慢阻肺患者更易受到影响。对所有合并COVID-19的慢阻肺患者,特别是病情较重或需要ICU住院的患者,均应进行早期康复,并在出院时、出院后6~8周筛查可康复治疗的特征。
7.20 发生COVID-19的慢阻肺患者的随访
轻度COVID-19患者应遵循与慢阻肺患者相同的常规管理方案,中度COVID-19患者需要更频繁、更准确地监测,并特别注意氧疗管理。如果胸部X线异常,在6个月至1年应考虑复查胸部X线或CT。监测COVID-19发病期间/之后发生的并发症。慢阻肺患者发展为重症COVID-19的风险更高,可能为「危重疾病」或「慢性危重疾病」的高风险人群。
7.21 在COVID-19暴发流行限制期间对慢阻肺患者进行远程随访
在COVID-19暴发流行限制期间,远程会诊是降低冠状病毒传播风险的非常好的方式,推动远程会诊而建立的系统有助于提高未来卫生保健系统的效率和能力。GOLD 2021提供了指导文件,支持在一级或二级医疗机构中就诊的慢阻肺患者进行远程交流。该工具包括:①准备远程访视;②与患者制订访视日程;③无论是面对面访视,还是通过电话、虚拟/在线访视,提供一个标准化的慢阻肺患者随访清单。应始终遵循良好记录和临床实践的原则:①有尊严地对待患者;②尊重他人的隐私权和保密权;③倾听患者的需求,并以患者的最佳利益为出发点;④将建议建立在现有的最佳证据之上。
7.22 分类和优先顺序
下列情况可考虑远程随访:①患者或护理人员可以清楚地了解病情并提供信息;②定期慢阻肺随访或已知疾病随访;③医疗保健专业人员可查阅医疗记录和实验室检查结果;④可以获得处方和药物,需要时可以安排随访期处方药物。
下列情况应优先考虑面对面访视:①患者和护理人员提供信息有困难;②由于病情严重,患者需要立即治疗;③患者症状变化需要进行鉴别诊断,需要进行体格检查和/或实验室检查;④患者治疗必须到医院,不能在家治疗。
就诊的优先顺序应考虑慢阻肺患者疾病的严重程度(症状负担和加重风险)、最近急诊和/或入院史、共病、年龄和/或是否独自在家生活。
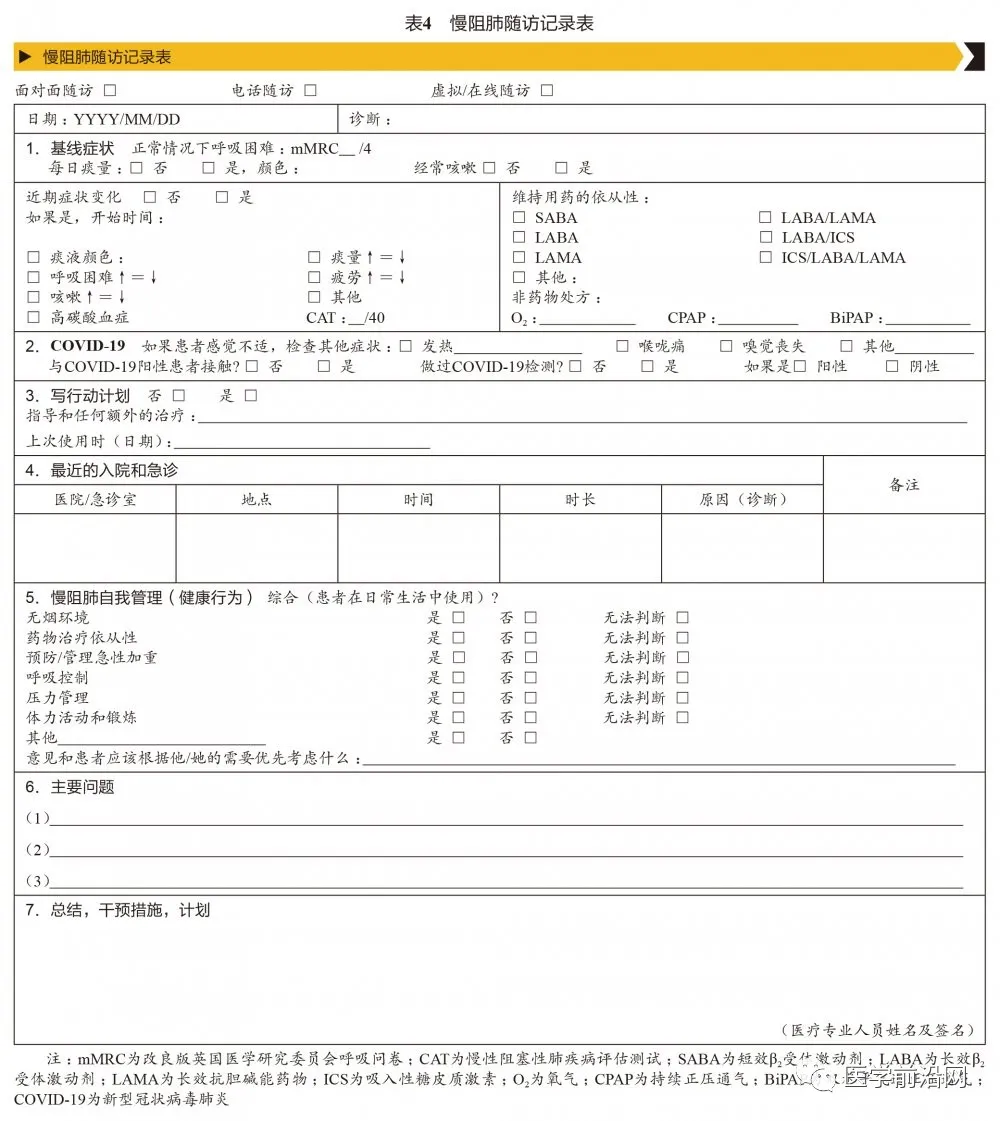
7.23 慢阻肺随访清单 GOLD 2021第七章列出了慢阻肺随访记录表(表4)。
小结
GOLD 2021更新解读中,笔者有几点体会:
(1)GOLD关注基层慢阻肺的筛查和基本干预措施:2020年9月7日WHO发布了《用于初级保健的非传染性疾病基本干预措施》。非传染性疾病,又称慢性病,往往持续时间较长,是遗传、生理、环境和行为因素共同作用的结果。非传染性疾病主要包括心血管疾病、癌症、慢性呼吸道疾病(如慢阻肺和哮喘)和糖尿病。非传染性疾病每年导致4100万人死亡,相当于全球所有死亡人数的71%。WHO的基本干预措施将有助于提高非传染性疾病适当医疗照护的普及。在这份文件中,WHO给出了慢性呼吸道疾病的基本干预措施,旨在为资源有限的中低收入国家提供一个具备性价比和可行性的方案,以便为民众提供基本的健康相关服务,从而减轻疾病负担。全球有高达19.5亿人口没有当地慢阻肺诊疗指南,需要推广普及慢阻肺基本筛查干预措施。根据《关于下达2020年公共卫生体系建设和重大疫情防控救治体系建设补助资金预算的通知》(财社﹝2020﹞99号)和《关于印发中央抗疫国债疾控类项目管理工作方案的通知》(国卫疾控综合便函﹝2020﹞91号)的要求,在国家卫生健康委员会疾病预防控制局的组织领导下,在国家呼吸医学中心和中国疾病预防控制中心的技术支持下,由中国基层呼吸疾病防治联盟牵头,基层呼吸系统疾病早期筛查干预能力提升项目目前正在全国31省(直辖市、自治区)、新疆生产建设兵团开展,以使基层医疗机构能够提供慢阻肺等常见慢性呼吸疾病的早期筛查、干预和健康管理服务,促进健康中国行动中慢性呼吸疾病防治专项行动目标的实现。
(2)循证医学与个体化治疗相结合:随着对慢阻肺发病机制研究的深入,慢阻肺治疗取得了很大进展,临床医生对于慢阻肺管理的信心增强,GOLD慢阻肺治疗目标已从过去仅关注改善慢阻肺患者的症状转至同时兼顾短期和长期目标,实现慢阻肺的全程管理。2020年4月,美国胸科学会发布了慢阻肺的药物治疗临床实践指南,以临床为导向,从证据出发,所解决的问题来源于临床实践,重点关注对临床实践有重要影响的干预与政策,并兼顾实际推荐意见的可行性。由慢阻肺临床专家、研究学者和方法学家组成的专家组归纳总结了慢阻肺药物治疗中最重要的6个问题,对所有相关研究进行了系统综述,并根据循证医学PICO(对象、干预、对照、结局)原则和方法,对证据进行GRADE评级和整合,给出了针对每个问题的推荐建议。2020年欧洲呼吸学会发布关于慢阻肺ICS撤除指南,建议根据外周血嗜酸性粒细胞和急性加重史判断。在慢阻肺治疗的新时代,临床医生可选择的药物治疗方案愈来愈多。通过真实世界的临床应用研究,使RCT得到进一步验证,在临床上为合适的患者选择合适的药物提供更多参考依据。中国慢阻肺指南将进一步结合临床尤其是基层医疗实践,修订具有中国特色的指南。
(3)新冠病毒疫情防控常态化与慢阻肺管理:慢阻肺人群是SARS-CoV-2的易感人群之一,而合并慢阻肺也是COVID-19患者进展为重症的危险因素之一,慢阻肺等多种慢性共病也增加了老年COVID-19患者的死亡风险,慢阻肺患者如何避免感染SARS-CoV-2则显得尤为重要。慢阻肺患者肺组织表达血管紧张素转换酶2(angiotensin converting enzyme 2,ACE2)(SARS-CoV-2受体)增加,这为慢阻肺患者可能更容易感染SARS-CoV-2提供了一种机制。慢阻肺患者还表现出内皮细胞功能障碍和凝血功能增高的特征,这可能导致COVID-19不良预后的风险增加。在疫情初期制定了《新型冠状病毒肺炎疫情期间慢性阻塞性肺疾病医疗和防范须知》《新型冠状病毒肺炎疫情防控期间开展肺功能检查的专家共识》《新型冠状病毒感染基层防控指导意见(第一版)》等指导文件。疫情期间慢阻肺的管理现状调查亦为我们带来启示:在未来的慢病管理中将进一步推动包括互联网医疗在内的创新管理模式,降低慢阻肺急性加重频率和住院次数,从而减轻社会经济负担。

专家介绍

陈亚红
主任医师,教授,博士研究生导师。北京大学第三医院呼吸与危重症医学科副主任、科研伦理综合办公室主任。研究方向:慢性气道疾病。担任第11届中华医学会呼吸病学分会肺功能学组副组长,第8~10届中华医学会呼吸病学分会慢性阻塞性肺疾病学组委员,中国医师协会呼吸医师分会慢性阻塞性肺疾病工作委员会委员,中国基层呼吸疾病联盟副主席,《中国医学前沿杂志(电子版)》编委。承担多项国家级和省部级科研基金,获得北京市科技新星计划支持和教育部新世纪优秀人才支持计划。研究结果获得北京市科技进步三等奖和中华医学科技奖三等奖。
陈亚红(北京大学第三医院 呼吸与危重症医学科,北京 100191)
基金项目:国家重点研发计划「重大慢性非传染性疾病防控研究」专项课题(2016YFC1304301);精准医学研究专项(2016YFC0903601,2016YFC0901102)
通信作者:陈亚红 E-mail :chenyahong@vip.sina.com
本文转载自订阅号「医学前沿网」(ID:yixueqianyan)
原链接戳:2021年GOLD慢性阻塞性肺疾病诊断、治疗及预防全球策略解读
本文完
排版:Jerry



