
摘要
本文报道1例28岁女性患者,临床以间断咯血、咳嗽、咳痰起病。实验室检查未见血象及炎症指标的升高,痰病原学无阳性发现。胸部影像学示右肺中叶及下叶支气管扩张伴感染,右侧胸膜增厚。右下叶背段于支气管镜下行肺泡灌洗,支气管肺泡灌洗液二代测序提示鸟胞内分枝杆菌。抗分枝杆菌治疗后患者症状较前好转,影像学可见炎症范围较前缩小。进一步寻找支气管扩张原因,患者体型高瘦,四肢细长,心脏彩超提示主动脉窦增宽,完善外周血基因检测发现FBN1基因变异,变异位点为c.4349G>A,综上考虑马凡综合征。
患者女,28岁,主因“间断咯血半年,咳嗽3个月”于2021年6月28日入院。
患者半年前(2021年1月)劳累后出现咯血,咯鲜红色血块约15 ml,无发热,经止血、抗感染治疗1周后(具体不详),未再咯血。4个月余前(2021年2月)无明显诱因再次出现咯血,初始为痰中带血,量约10 ml/d,2 d后咯血加重,为鲜红色血液,量约300 ml,伴胸闷、气短、头晕、心悸,无发热、恶心、呕吐,当地医院胸部CT示:右肺中下叶片状渗出影伴右肺中叶部分不张(图1~3),给予垂体后叶素止血、抗生素(具体不详)抗感染等治疗3 d,效果不佳,仍有咯血,平均30~50 ml/d。遂转至某市级医院介入科住院治疗,支气管动脉造影未见明确罪犯血管,故未行介入治疗,痰培养提示肺炎克雷伯杆菌,给予抗感染、化痰及巴曲亭等治疗,患者未再出现咯血,好转出院。出院后(2021年3月下旬)患者开始出现阵发性咳嗽、咳痰,为黄、绿及褐色痰,晨起及活动后明显,无胸痛、胸闷、气短,间断服用化痰、头孢类、左氧氟沙星等药物(具体不详),上述症状无明显缓解。
4 d前无明显诱因再次出现咯血,量约5 ml,伴咳嗽、咳痰加重,于我院急诊就诊,外院胸部CT(2021年 6月24日)示:右肺中叶及下叶支气管扩张伴感染,右侧胸膜增厚(图4~6),给予头孢曲松抗感染、巴曲亭止血治疗后,患者仍有咳嗽、咳痰,痰中带有少量鲜红色血丝。既往有多囊卵巢综合征病史5年。
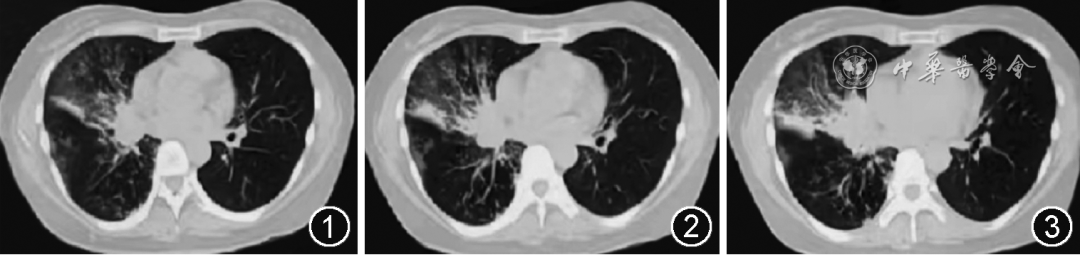
图1~3 2021年2月13日胸部CT示右肺中下叶片状高密度影

图4~6 2021年6月24日胸部CT示右肺中叶及下叶支气管扩张伴感染
体格检查:身高174 cm,体重65 kg,体重指数为20.48 kg/m2,体温 36.1 ℃,呼吸频率 20次/min,心率 80次/min,血压 116/70 mmHg,体型瘦长、肌肉发育欠佳、四肢细长、蜘蛛指(趾)(图7,8),无皮疹和关节红肿畸形,浅表淋巴结未触及肿大。胸廓视诊未见明显鸡胸、漏斗胸,双肺未闻及干湿性啰音及胸膜摩擦音。心率为86次/min,P2=A2,各瓣膜区未闻及杂音。腹平软,无压痛,肝脾肋下未触及,双下肢无水肿。四肢关节活动良好,未见脊柱侧弯或后突。

图7,8 入院后体检可见患者手指脚趾细长(蜘蛛指/趾)
实验室检查:血常规:白细胞3.99×109/L,中性粒细胞为1.84×109/L,血红蛋白为113 g/L,血小板为290×109/L;尿常规、便常规未见异常,肝肾功能、电解质、血糖、凝血4项、ESR、D-二聚体均正常;血清支原体、衣原体IgM、IgG抗体均阴性。入院初步诊断:支气管扩张伴咯血,支气管扩张伴感染。
入院后完善相关检查,血清抗核抗体(ANA)、ENA抗体谱、抗中性粒细胞胞质抗体(ANCA),类风湿因子、体液免疫IgG、IgM、IgA、补体C3、C4检查均正常;T细胞亚群:CD3+T细胞为74.3%(正常参考值:71.5%±6.2%),CD4+T细胞为41.6%(正常参考值:45.7%±5.3%),CD8+T细胞为29.4%(正常参考值:27.9%±5.0%),CD3+CD4+/CD3+CD8+为1.41(正常参考值:0.9~2.0),NK细胞为7.2%(正常参考值:7%~40%);过敏原总IgE检测、吸入物过敏原过筛实验、专项变应原筛查(烟曲霉)、特殊变应原筛查(多价霉菌)均阴性;完善心脏超声示主动脉瓣轻度反流,主动脉窦增宽,心包积液微量;腹部超声示肝内稍高回声(血管瘤?),胆囊泥沙样结石;下肢血管超声示双下肢静脉未见明显血栓。给予头孢哌酮舒巴坦(3 g/次,2次/d)联合依替米星(0.3 g/次,1次/d)抗感染治疗10 d,同时完善病原学检查,痰涂片,痰抗酸染色均阴性,痰GeneXpert MTB/RIF(Xpert)未见明显异常;结核感染T细胞斑点试验(T-SPOT.TB)阴性;1,3-β-D-葡聚糖(G试验)、曲霉半乳甘露聚糖抗原(GM试验)和曲霉抗体IgG均阴性。于2021年7月5日行支气管镜检查,镜下示正常气道,右下叶背段少量白色泡沫样分泌物。右下叶背段行支气管肺泡灌洗,BALF示白色浑浊,病理可见上皮细胞、巨噬细胞、淋巴细胞及中性粒细胞,BALF二代测序提示鸟胞内分枝杆菌复合群,故停头孢哌酮舒巴坦及依替米星,改为克拉霉素(0.25 g/次,2次/d)、利福平(0.6 g/次,1次/d)联合乙胺丁醇(0.75 g/次,1次/d)口服治疗5 d后出院。
患者出院1个月后于某市级胸科医院门诊治疗,并调整抗非结核分枝杆菌(NTM)治疗方案,改克拉霉素为阿奇霉素,联合利福平、乙胺丁醇、氯法齐明四联抗NTM治疗14个月。后未再咯血,间断咳嗽,咳痰少量,晨起为著,常规体检血、尿化验未见异常。2021年 8月3日、2022年6 月20日、2022年8 月5 日查痰分枝杆菌培养均阴性。2022年2月17日复查胸部CT示右肺中叶及下叶支气管管壁增厚,管腔柱状增宽,周围及远端多发结节状、斑片状高密度,病灶范围较2021年6月24日缩小(图9~11)。2023年1月27日复查胸部CT示右肺多发片结影,右肺中叶部分支气管扩张,心脏不大,心包未见明显增厚及积液,主、肺动脉无增粗(图12~14)。
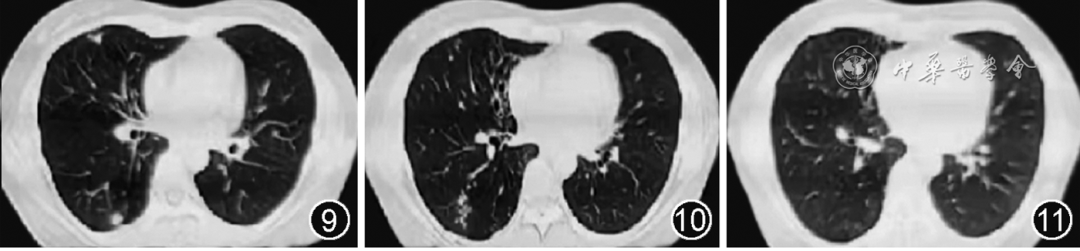
图9~11 2022年2月17日胸部CT示右肺中叶及下叶支气管管壁增厚,管腔柱状增宽,周围及远端多发结节状、斑片状高密度影,病灶范围较2021年6月24日缩小

图12~14 2023年1月27日胸部CT示右肺多发片结影,右肺中叶部分支气管扩张
讨论
李静(呼吸与危重症医学科):本例患者为青年女性,慢性起病。临床表现为间断咯血伴咳嗽、咳痰,外周血白细胞及中性粒细胞正常,影像学表现为右肺中叶及下叶支气管扩张伴感染,右侧胸膜增厚。入院初步诊断为支气管扩张伴感染、支气管扩张伴咯血,经验性给予头孢哌酮舒巴坦联合依替米星抗感染治疗,效果不佳。因此需考虑是否为目前应用的抗生素不能覆盖的特殊病原体感染,如结核分枝杆菌、奴卡菌等。故在经验性治疗的同时,要积极地进行病原学查找。因患者入院后留取的痰标本未能获得明确的阳性病原学结果,于入院第7天行支气管镜检查,镜下示正常气道,右下叶背段少量白色泡沫样分泌物,右下叶背段行支气管肺泡灌洗,BALF呈白色浑浊,病理可见上皮细胞、巨噬细胞、淋巴细胞及中性粒细胞,BALF二代测序提示鸟胞内分枝杆菌复合群,序列数11。
高燕莉(放射科):患者入院前胸部CT(2021年6月24日)于右肺中叶内侧段可见部分支气管扩张,管壁增厚,周围片状高密度影,考虑右肺中叶局部支气管扩张及周围炎性改变可能,右肺下叶多发结节状、斑片状高密度影,经验性抗细菌治疗效果差,从影像学角度需要与结核和NTM感染相鉴别,其中NTM肺病影像学上主要分为4型[1],分别为纤维空洞型、结节性支气管扩张型、孤立的肺结节型和过敏性肺炎型,不同类型之间的影像学表现可相互重叠。NTM肺病的胸部CT主要表现为结节影、斑片及小斑片样实变影、空洞影、支气管扩张影、树丫征、磨玻璃影等,胸膜肥厚粘连、心包受累、纵隔淋巴结肿大少见[2],且通常多种病变形态混杂存在。结节影以小叶中心小结节为主,结节边缘模糊。支气管扩张可呈柱状及囊状,以右肺中叶、左肺舌叶多见。小叶中心结节影和支气管扩张影混合存在是NTM肺病较为常见的影像学表现[3]。
谷丽(感染和微生物科):鸟分枝杆菌属于NTM中的一种,与胞内分枝杆菌统称为鸟分枝杆菌复合群(MAC)[4]。MAC广泛存在于自然环境中,是NTM病中的常见致病菌,临床上多表现为与结核感染相似的肺内及肺外病变[5]。有研究表明,NTM感染在支气管扩张症(简称支扩)患者中较为常见,约30%的支扩患者痰或BALF标本中可分离出NTM,以MAC最为常见[6]。目前指南推荐[7]MAC肺病的标准治疗方案是以大环内酯类药物(克拉霉素或阿奇霉素)为核心,联合利福平(或利福布汀)、乙胺丁醇和阿米卡星等。有研究证实[8],大环内酯类药物联合乙胺丁醇、利福平、氨基糖苷类药物治疗MAC肺病,可大大降低大环内酯类药物治疗过程中的耐药率。
王慧娟(呼吸与危重症医学科):经过一系列病原学检查,最终明确患者为鸟胞内分枝杆菌感染,并调整了治疗方案。然而关于患者罹患支气管扩张的病因目前尚不明确,《成人支气管扩张症诊治专家共识》2021版指出[9],支扩的主要已知病因如下:既往下呼吸道感染、免疫功能缺陷、遗传因素、气道阻塞和反复误吸、变应性支气管肺曲霉病(ABPA)、慢性阻塞性肺疾病、支气管哮喘、NTM肺病、炎症性肠病、类风湿性关节炎等,综合考虑患者症状、体征、病史、实验室检查、胸部CT表现等,该患者儿童时期无明确下呼吸道感染,如麻疹、百日咳,故不考虑感染后支扩。完善T淋巴细胞亚群及体液免疫功能检测,未见明显免疫功能缺陷。进一步追问病史,患者无气道阻塞和反复误吸史、无ABPA、慢性阻塞性肺疾病、支气管哮喘等肺部疾病,完善血清ANA、ANCA相关抗体、类风湿因子等检查均正常,故不考虑结缔组织病所致支扩。患者四肢细长,心脏超声示主动脉窦部增宽,要除外马凡综合征(MFS),目前不除外MFS所致支扩。
方秋红(呼吸与危重症医学科):2010年英国胸科协会的《非囊性纤维化支气管扩张指南》[10]中指出大气道先天性异常是支气管扩张的病因之一,包括先天性支气管软骨发育不全、巨大气管-支气管症、马凡综合征等。入院后患者体检可见体型高瘦、肌肉发育欠佳、四肢细长、蜘蛛指(趾),完善超声心动图示主动脉瓣轻度反流,主动脉窦增宽,心包微量积液。根据Ghent标准[11]及评分细则,该患者无MFS家族史,体型瘦长,蜘蛛指(趾),心脏超声示主动脉窦部增宽,疑诊为MFS。为确诊MFS,完善全外显子组测序示FBN1基因c.4349G>A(p.Cys1450Tyr)位点基因变异,其编码的蛋白第1450位氨基酸由半胱氨酸突变为酪氨酸,与文献报道的MFS患者基因变异位点相同[12]。检测父母该位点基因型正常。通过基因检测证实存在FBN1基因变异,且Ghent标准系统评分≥7分,因此可确诊为MFS。
卜小宁(呼吸与危重症医学科):MFS是一种少见的常染色体显性遗传疾病[13],主要为第15号染色体上的FBN1基因缺陷引起[14]。根据修订版Ghent标准,MFS患病率约为6.5/100 000[15]。MFS常有家族史,以青壮年多见,主要累及骨骼、眼和心血管系统,表现为体型瘦长、肌肉发育不良、蜘蛛指(趾)、脊柱侧弯或后突、漏斗胸或鸡胸、晶状体脱位、主动脉根部扩张和主动脉夹层等[16]。约10%的MFS并发呼吸系统疾病。如慢性阻塞性肺疾病/肺气肿、自发性气胸、支气管扩张以及睡眠呼吸紊乱等[17]。其中支气管扩张与MFS的关系并不少见,韩国学者通过胸部高分辨率CT(HRCT)评估了79例成年MFS患者的支气管扩张患病率,结果发现22例(28%)患者出现支气管扩张,10例(13%)患者有细支气管扩张[18]。尽管这一结果可能归因于近十年来HRCT的普及,但马凡综合征导致的支扩仍要引起足够重视。支气管扩张是NTM肺病的一个公认的危险因素,合并支气管扩张的NTM肺病患者,其肺部影像学表现更为严重,临床上需与肺结核相鉴别[19]。
目前研究表明,关于MFS合并心血管异常的患者,联合使用氯沙坦与β受体阻滞剂能够减缓MFS患者主动脉根部扩张的进展[20]。但对于MFS引起的支气管扩张症,目前尚无特异治疗。支气管扩张继发NTM感染,以MAC感染最为多见。虽然指南推荐了MAC感染的标准治疗方案[7],但Meta分析显示其治愈率不足70%[21, 22],可能归因于MAC的细胞壁为疏水性,药物不易透过,因此MAC对多数抗分枝杆菌药物均耐药。近年来,氯法齐明(CFZ)[23]、贝达喹啉(BDQ)[24]和德拉马尼(DLM)[25]这3种药物对NTM展现出了较好的抑菌活性。其中氯法齐明为亲脂性化合物,可以自由透过MAC的细胞壁并将其破坏[26],对MAC有良好抑菌效果。英国胸科协会的NTM治疗指南[27]中提到,建议在抗NTM治疗初期应用CFZ,持续治疗30 d以上可达到稳定的血清浓度,但仍需监测其体外敏感性。
这是一例临床少见病例,从支气管扩张伴感染的诊断,到寻找支气管扩张感染的病原学(痰、BALF),最后追根溯源,明确支气管扩张的病因,抽丝剥茧,层层递进,体现了良好的临床思维。总结本病例的特殊之处:(1)对于反复发生的以咯血、支气管肺部感染为主要症状的支扩患者,明确支扩感染的病原学对指导治疗至关重要,尤其是经验性抗生素治疗效果不佳时。(2)对于体型高瘦、指(趾)细长的支气管扩张症患者,应重点关注心脏超声表现,积极寻找病因,警惕MFS,必要时完善基因检测进一步明确。经过积极的病原学查找,该患者最终诊断为MAC感染,并给予相应治疗后症状好转。最终诊断:支气管扩张伴鸟胞内分枝杆菌感染、支气管扩张伴咯血、马凡综合征。
参考文献(略)
作者:李静 陈潇婷 高燕莉 王慧娟 谷丽 方秋红 卜小宁;单位:首都医科大学附属北京天坛医院呼吸与危重症医学科;首都医科大学附属北京朝阳医院呼吸与危重症医学科
引用本文: 李静, 陈潇婷, 高燕莉, 等. 马凡综合征导致支气管扩张症患者继发非结核分枝杆菌感染 [J] . 中华结核和呼吸杂志, 2024, 47(1) : 31-35. DOI: 10.3760/cma.j.cn112147-20230928-00203.
本文转载自订阅号「中华结核和呼吸杂志」
原链接戳:【临床病例(理)讨论】马凡综合征导致支气管扩张症患者继发非结核分枝杆菌感染
* 文章仅供医疗卫生相关从业者阅读参考
本文完
责编:Jerry



