病例汇报
患者46岁男性,2020年9月10日入院
主诉: 反复发热伴咳嗽、咳痰11天
现病史: 患者于2020-08-31号无明显诱因下出现发热,体温高达38.5℃,当地诊所予头孢治疗4天后体温稍有缓解,09-07再次出现发热,热度高达40℃,经治疗后症状持续不缓解,09-09至当地上级医院就诊,胸部CT示:左下肺胸主动脉旁感染可能,建议治疗后复查,右肺胸膜下及左肺多发小结节,建议随访。血常规:白细胞计数16.39ⅹ10 9 /L;中性粒细胞计数:15.93ⅹ10 9 /L;淋巴细胞百分比:1.9%。患者入院时仍高热,持续性干咳,咳嗽剧烈时稍有血丝,胸闷气急明显,急性病面容,病程中患者神志清,稍有头晕头痛,睡眠尚可,食纳正常,大小便正常。
既往史: 患者既往体健。否认高血压、糖尿病、肾病病史,否认肝炎、结核等传染病史。3年前曾因外伤引起胸腔积液,进行胸腔闭式引流手术史。无输血史。否认药物、食物过敏史。
个人史: 生于原籍,久居当地。否认疫区、疫水接触史。否认毒物、放射性物质接触史。吸烟20余年,11支/每天,平日少量饮酒。
婚育史:适龄结婚,配偶及子女体健。
家族遗传史:否认家族遗传病史及类似疾病史。
体格检查:神志清,精神可,急性发热面容,颈静脉无怒张。胸廓无畸形,无胸壁静脉曲张,双侧胸廓活动度对称,双侧语音震颤对称,叩诊清音,两下肺可闻及少许湿啰音。心尖搏动范围正常,HR102次/分,律齐,各瓣膜区未闻及病理性杂音。腹平软,无压痛,无反跳痛,肝脾肋缘下未触及,双肾区及肝区无叩击痛,肠鸣音可及,移动性浊音阴性,双下肢无水肿,病理征未引出。
辅助检查:2020-09-09胸部CT示:左下肺胸主动脉旁感染可能,建议治疗后复查,右肺胸膜下及左肺多发小结节,建议随访。09-09血常规:白细胞计数16.39ⅹ109/L;中性粒细胞计数:15.93ⅹ109/L;淋巴细胞百分比:1.9%。
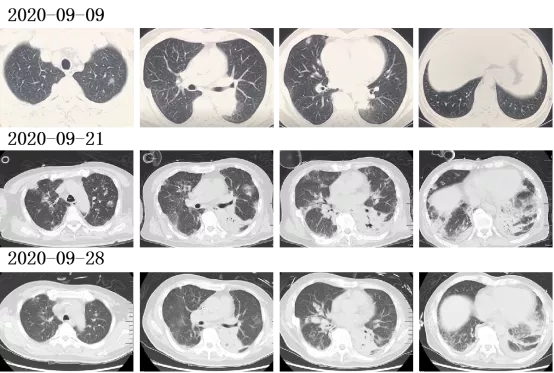
2020-09-09胸部CT
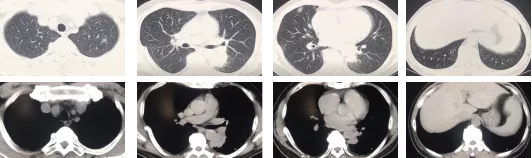
初步诊断
社区获得性肺炎(初治失败)
Ⅰ型呼吸衰竭
治疗方案:
鼻导管吸氧
比阿培南抗感染
入院后辅助检查:
动脉血气(鼻导管吸氧,FiO2 29%):PaO2 73.4 mmHg,氧合指数 253mmHg
血常规:WBC 18.85ⅹ109/L,LY 0.17ⅹ109/L,NE 18.44ⅹ109/L,PLT:227ⅹ109/L,HGB:114g/L
生化全套:TBIL 24.7μmol/L,ALT 17.3U/L,ALB 27.5g/L,Cr 48.5μmol/L,Glu 9.76mmol/L,CK-MB 20 U/L,LDH 825U/L
PCT:2.07 ng/ml
CRP:290.51mg/L
血凝指标:D-二聚体 1.78 mg/L
病情变化及评估
患者入院第二天,高热不退,胸闷气急逐渐加重,伴随血压下降,83/58mmHg,考虑感染性休克,积极扩容后纠正(未使用血管活性药物),同时加用莫西沙星注射液加强抗感染,完善胸痛组套:肌钙蛋白 5.74 pg/mL,BNP 2070 pg/mL,血常规:Ly 0ⅹ109/L,复查血气分析(面罩吸氧,FiO2 50%) :PaO2 64.44mmHg,氧合指数:129mmHg。评估病情:患者持续高热,最高达40℃,呼吸窘迫进行性加重,RR>30次/分,氧合指数自253mmHg降至129mmHg,血压出现一过性降低,CURB-65评分由1分上升至2分,病情快速恶化,紧急转入呼吸科ICU(RICU)。
第一次RICU
杨雯医师(PCCM学员)总结前期诊疗特点及后续诊疗计划:
这是一个中年男性,咳嗽、发热,CT示左下肺实变,双肺多发浸润影,伴多项感染相关指标的升高,RR大于30次/分,诊断为CAP、CURB-65评分1分。由于头孢初治失败,入院后升级为比阿培南、莫西沙星抗感染治疗,但病程中依然出现了进展,持续的发热、呼吸窘迫加剧、氧合指数降低,同时有血压的下降,基于目前表现,诊断修改为SCAP、Ⅰ型呼吸衰竭、CURB-65评分2分,同时合并不明原因的淋巴细胞降低,可能存在的心功能不全。鉴别诊断上,在感染方面,需要考虑是否存在耐药细菌的感染及曲霉、念珠菌、隐球菌、非典型病原体的感染。非感染性疾病方面,需要鉴别风湿免疫系统疾病、以肺炎为表现的肿瘤及血液系统疾病。目前治疗上主要需要完善血培养、明确是否存在脓毒症,尽快寻找病原体,指导抗生素的调整,尽快评估是否合并其他系统的疾病。
RICU床旁影像学评估:
床边胸片:两肺病变较前明显进展
肺部超声:两肺均可见大量B线,左下肺可见低回声区,内有散在点状强回声
心超:心室收缩功能减弱,EF:52%,主动脉瓣、二尖瓣轻度返流,三尖瓣最大返流压差25mmHg
下腔静脉内径27mm,吸气末塌陷<50%

汪泱医师(PCCM学员)RICU床旁影像学评估要点,及指导意义
从前面的病例汇报可以看出陈澄医生已经对患者进行了十分完善的床边影像学评估,包括床边胸片、肺脏超声、床边心超,这些其实也是ICU十分常见的快速床旁影像学评估的手段。
床边胸片发现肺部病变快速进展通常提示感染、ARDS、心功能不全等,如果快速吸收,那么肺水肿可能性更大一些。肺脏超声对于各种急慢性心肺疾病都有比较高的诊断价值,除了常规评估胸腔积液,对于气胸、肺实变、ARDS都有鉴别作用,且敏感性和特异性都比较高。如果再结合心超,更加直观的评估患者的容量、心功能,能够进一步提高诊断的准确性。
这名患者床边胸片24h内快速进展,肺脏超声可以探及大量B线,心脏超声可见下腔静脉明显增宽,塌陷度<50%,综合评估,考虑肺水肿可能性大,至于是ARDS还是心功能不全,还需要其他快速床旁检查辅助鉴别。但不管是哪一种可能,都需要加强对患者的液体管理。
第一次入RICU诊疗过程:
病情评估:APACHE-Ⅱ评分:14,住院病死率:18.6%,SOFA评分:3分。
修正诊断:SCAP,Ⅰ型呼吸衰竭,脓毒症?心功能不全
治疗调整:NIPPV,抗感,比阿培南+莫西沙星,低分子肝素抗凝,改善心功能
血培养(入院当日留取,三日后报告):人葡萄球菌(耐苯唑西林)
风湿抗体:Ro-52(+),余阴性(含肌炎、血管炎、类风湿)
肿瘤全套、输血全套、尿粪常规、G/GM试验、疟原虫、肥达氏反应、冷凝集试验:阴性
细胞免疫:CD4+T:34.57%,CD8+T:45.3%,CD4+T/CD8+T 0.76
患者持续高热,BNP 34608pg/ml;ALT,163.7U/L,肌酐62.0umol/L;血常规:WBC 5.72ⅹ109/L,LY 0.08ⅹ109/L,NE 5.6ⅹ109/L;动脉血气(NIPPV,FiO2 60%):PaO2 61.0mmHg,氧合指数:100mmHg。患者呼吸窘迫逐渐加重,加用利奈唑胺加强抗感染(患者病情进展迅速,予抗G+球菌),09-15气管插管呼吸机辅助通气,复查胸片两肺感染较前进展,再次床旁心超示心室收缩功能减弱,EF:55%,主动脉瓣、二尖瓣轻度返流,三尖瓣最大返流压差34mmHg,下腔静脉内径24mm,吸气末塌陷<50%,床边气管镜检查示左右支气管内少许脓性分泌物,粘膜充血水肿明显。

讨论1:患者病情恶化原因?
A.病原体未覆盖
B.心源性疾病
C.ARDS
D.存在未知基础病
杨丽敏医师(PCCM学员)分析:
该患者中年男性,并无基础疾病,初步诊断:CAP。但患者的病情几天内快速进展,超声:肺水肿,容量负荷增加,心肌收缩力下降,肺动脉压力增高,BNP从两千增到三万五,呼衰加重,氧合指数快速下降,这个时候已经不能用常见的CAP解释了。患者病情进展迅猛,首先考虑心衰肺水肿,但心衰的原因尚不清楚。既往无心脏疾病的中年男性,淋巴细胞计数为零。如果考虑病毒性心肌炎的话,心衰致肺水肿,病毒本身也可能引起间质性肺炎,这2点都符合肺超声的大量B线。然而患者肌钙蛋白不高,EF值在0.52到0.55之间,又不太符合病毒性肺炎。如果后续容量得到控制、心功能改善后仍有双肺浸润影,要考虑合并重度ARDS。但是ARDS的病因还有待进一步探寻,血培养的耐药人葡,是不是污染可能大?这个时候患者并无深静脉等置管,还有什么致病菌未找到,抗感染未覆盖到。肺栓塞的话,患者的三尖瓣返流压差从25mmHg增到34mmHg,这时患者下腔静脉大于21mm,塌陷率小于50%,要加15mmHg得出肺动脉压力49mmHg,已接近中度肺动脉高压的50mmHg标准,但患者D-D二聚体是阴性的,D-D二聚体阴性的肺栓塞也有但很少见,患者现在无法行CTPA明确。综上,患者NE、CRP、PCT都很高,持续高热,还是首先考虑感染合并心衰。
衡伟主任医师(呼吸与危重症医学科)点评:
刚才各位专培学员都对这个病例进行了较为全面和细致的分析,这样一个中年男性患者,以往没有基础疾病,根据其急性发病,血常规的异常,以及肺部影像学的改变,再结合重症肺炎的主要标准和次要标准,均符合重症社区获得性肺炎(重症)的诊断。关键问题在于从起病到住院再到入住ICU病房,虽然表皮葡萄球菌并不是社区获得性肺炎的常见致病菌,但即使根据药敏试验给予针对性的抗感染和对症治疗,病情仍快速持续进展,这其中的原因是什么?除了同学们前面的分析,可能需要关注该患者多次血常规提示淋巴细胞数极低、甚至为零,而中性粒细胞比例非常高,这背后究竟有没有隐藏着其它的合并疾病?第二,患者的BNP指标从两千多迅速上升到3万多,提示我们必须加强液体的管理。未来患者入住ICU后除了给予全面的生命支持和液体管理,在给病人赢得治疗时间后需要花时间来探寻这背后究竟有没有其它的疾病,虽然目前还没有充分的证据。
诊疗调整
继续机械通气,CRRT,激素减轻炎症反应,抗感染,脏器功能保护,低分子肝素抗凝,营养支持。
动脉血气(FiO2 45%):PaO2 96.4mmHg,氧合指数 214mmHg,BNP下降至1044pg/mL,影像学改善。
2020-09-21胸部CT:

病原体检查:
9.12 血培养:人葡萄球菌(耐苯唑西林)
9.17 BALF(mNGS):人葡萄球菌,肺炎克雷伯杆菌
9.17 BALF(培养):草绿色链球菌
9.19 血(mNGS):近平滑念珠菌
9.23 BALF(真菌培养):黄曲霉菌
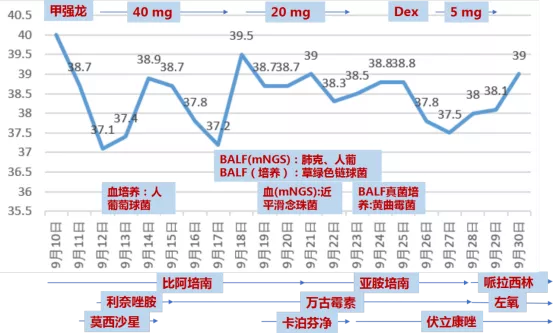
根据检查结果调整治疗方案,给予小剂量激素抗炎,加用科赛斯和万古霉素加强抗感染,经过综合治疗,一周后患者病情明显改善,动脉血气(FiO2 30%)PaO2 93.9 mmHg,2020-09-26顺利脱机拔管,复查动脉血气(鼻导管吸氧,FiO2 40%) PaO2 126mmHg,09-28复查CT较前改善,09-30转入普通病房继续治疗。
血培养(9.12)
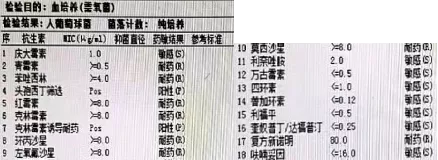
mNGS(BALF)
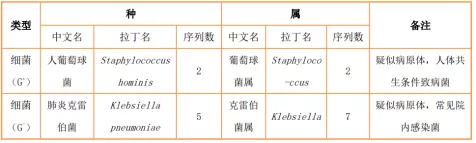
mNGS(外周血)
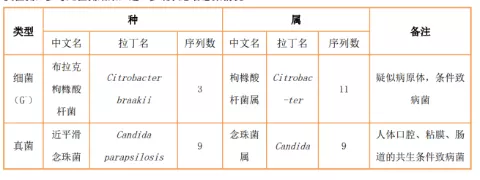
徐杰主任医师(检验科)点评:
患者入院第一天送检血培养检出人葡萄球菌,可能具有一定的临床意义,污染的可能性较小,凝固酶阴性葡萄球菌在抗生素使用方面要注意苯唑西林耐药问题,即MRS;随着住院时间的增加,肺部病情在加重没有好转,BALF(mNGS)检出肺炎克雷伯菌,可能是有一定临床意义的条件致病菌;外周血(mNGS)检出近平滑念珠菌,结合临床看是否为血流感染菌,积极抗真菌治疗;住院10~14天BALF真菌培养出黄曲霉菌,可能与气管切开或辅助呼吸有关,长时间辅助呼吸患者已发生院内曲霉菌感染。
治疗调整:
王佳佳副主任医师(PCCM学员)关于激素在肺炎中的应用分析:
通过RICU的综合治疗和管理,患者的病情总体有改善,这种改善主要得益于抗生素的及时使用以及机械通气和CRRT的综合应用。但是我们也注意到,患者从入院后不久就给予了糖皮质激素治疗。目前糖皮质激素在重症社区获得性肺炎患者中使用有效性和安全性存在争议。但是重症社区获得性肺炎合并脓毒症和脓毒症休克的患者,大多数专家认为短疗程低剂量的糖皮质激素治疗是可以获益的。
重症社区获得性肺炎合并ARDS以及肺外多器官功能损伤,它往往并不是病原体直接侵入器官引起的损伤,而是由于病原体侵入我们的人体,引起了过度的免疫反应,激发的炎症因子风暴,导致体内的促炎因子和抗炎因子的比例失衡,继发的多器官功能损伤。既往我们一项回顾性的临床研究也证实,在新冠肺炎合并ARDS以及肺外多器官功能损伤的患者中,有些炎症因子与特定的器官功能损伤是密切相关的。
糖皮质激素是大家公认的具有强大的抗炎作用,那么它为什么在重症肺炎当中的使用一直存在争议?我想主要存在以下两个方面:第一,目前我们还不能准确的识别出哪些患者可以从糖皮质激素的使用中获益;第二,我们还不能对糖皮质激素干预的时机很好的把握。上述问题未来需要更多多中心前瞻性的临床研究去证实。
我们再回到这个病例。这个患者从糖皮质激素开始使用到现在已经有三周。针对重症社区获得性肺炎,这个患者糖皮质激素使用的疗程已经足够,应该果断停止。否则因为糖皮质激素较长时间的使用所带来的各种不良反应,或者并发症发生的风险将大大的增加。
王希明主任医师(影像科)点评分析:
这个病例非常复杂,我就患者第一阶段的影像学检查做一下分析,主要谈一下影像学检查对于本病的鉴别诊断价值。患者2020-09-09细胞CT显示左肺下叶脊柱旁球形病变,病变边界相对清楚,周围肺野清晰,右肺中叶及左肺上叶结节样病变。左下肺病变需要与肿瘤、球形肺炎、炎性假瘤及球形肺不张鉴别,因为胸部CT是在发病10天之后检查的,也可能是肺内炎症吸收局限后所形成。患者入院后的9-11的床边胸片提示病变进展较快,左肺中下肺野出现大片实变,结合临床症状及实验室检查结果,肺肿瘤可以排除,球形肺炎进展的可能性大。9-15床边胸片较9-11明显进展,右肺出现大片实变影,与左肺病变形成蝶翼状表现,结合患者心脏功能情况,考虑两肺感染的基础上合并肺泡型肺水肿,超声也提示两肺并存间质性肺水肿。9-21胸部CT是患者经综合治疗、患者病情好转后做的,CT显示左肺下叶实变影,其内可见一空洞样病变,左下肺病变较12天前的外院CT进展,另于两肺散在斑片状、斑点状高密度影及纤维索条影,呈慢性炎症改变。不同病原体的肺内感染,具有相对特征性的影像学表现,通过患者肺部影像学表现可以对病原体的类型做一个大体诊断。如肺炎链球菌肺炎典型表现为大叶性肺炎的实变影,很少出现空洞,相对病变局限,治疗后吸收消散快,本病左下肺病变在逐渐进展,且两肺散在多发病变,不符合典型大叶性肺炎表现;金黄色葡萄球菌肺炎和厌氧菌肺炎容易形成多发空洞及肺脓肿,与该患者影像学表现不符;肺炎克雷伯杆菌肺炎常表现为肺叶或肺段实变,可出现多个小空洞,呈蜂窝状脓肿,并迅速融合为大空洞,出现叶间裂下坠,也与该患者影像学表现不同;军团菌肺炎病变分布广泛,形态多样,可表现为实变、空洞、纤维化等改变,与本病鉴别困难;病毒感染及支原体感染多表现为间质性肺炎,以磨玻璃影或网格状影为主,与本病不同;肺真菌感染的晕征、反晕征、霉菌球、多发不规则空洞、多发结节等征象该患者均未出现;肺结核各型影像学表现也与该病例不符。但肺内不同病原体感染异病同影的现象比较突出,尤其在系统抗炎治疗后,表现可能更不典型,因此该病例单纯从影像学表现来推测病原体类型,还是非常困难,还是需要结合临床及病原体实验室检查进行分析诊断。
陈延斌主任医师(呼吸与危重症医学科)RICU第一阶段诊疗总结分析:
肺炎的诊断程序包括确定肺炎诊断、评估严重程度、确定病原体三个环节;在该阶段,我们围绕这三个问题作了大量工作,也获得了相应的依据,诊断SCAP应该没有问题,治疗也初见成效;但患者的体温再次飙升到39℃,且CT显示左下肺病变吸收并不理想,是单纯的SCAP治疗还没有到位,还是合并存在其他隐匿的问题,抑或这所谓的「SCAP」只是一个假象,仍值得后续进一步探究。
转入普通病房依然存在的问题:
体温未获控制
左下肺病灶无明显吸收
在ICU期间发生的心功能不全是什么病因?
实验室检查:
血常规:WBC 17.25ⅹ109/L,LY 0.14ⅹ109/L,NE 17.03ⅹ109/L,PLT 275ⅹ109/L,HGB 77g/L
降钙素原:0.41 ng/ml
血培养(连续25天):阴性
深部痰培养:其它奈瑟菌
风湿抗体:Ro-52(+),余阴性(含肌炎、血管炎、类风湿)
肿瘤全套:阴性
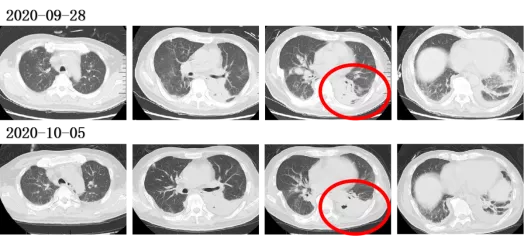
抗感染治疗方案不调整,激素减量的过程中体温反复,2020-10-05复查胸部CT:左下肺病灶较前略有进展。

讨论2:发热原因?
A.真菌感染
B.结核感染
C.多重耐药菌感染
D.结缔组织疾病
E.血液系统疾病
F.机化性肺炎
张晓辉主治医师(PCCM学员)分析:
这个患者经过这一阶段的治疗,咳嗽,呼吸困难等临床症状明显改善,胸部影像学大部吸收,但仍然还有发热,左下肺病灶不吸收,他的发热要从三个方面考虑:
第一个是感染性发热。首先想到的导管相关性感染,因为我们对这个患者做了很多侵入性操作,比如血透置管、深静脉置管,不排除导管相关性感染,可以继续完善血培养及导管相关培养;患者经历了气管插管有创呼吸机辅助通气,反复的广谱抗生素使用,皮肤黏膜屏障破坏等MDR感染的高危因素,反复发热要考虑继发MDR感染导致;同样的,这个患者也是有多种真菌感染高危因素,尤其是侵袭性肺曲霉菌病IPA感染(静脉使用抗生素,糖皮质激素使用等等),反复发热需要明确有无IPA;
第二个就是非感染性发热,首先需要鉴别的就是机化性肺炎,以反复发热,咳嗽,呼吸困难为主要表现,影像学表现为两肺多发的磨玻璃影或实变影,抗感染无效,这个患者始发病灶为左下肺实变,伴发热,随着激素减量过程中出现发热,需要鉴别,需气管镜或经皮肺穿刺活检病理明确;其次是风湿结缔组织疾病引起的发热,多伴有多系统损害,如系统性红斑狼疮,干燥综合征,血管炎等等,完善风湿相关抗体检查往往可以明确;
第三个就是恶性肿瘤,如淋巴瘤,也可以表现为反复发热,伴肺部浸润表现,这个患者反复出现淋巴细胞低下,甚至为0,需高度怀疑血液系统疾病,需行肺穿刺活检或骨穿检查病理明确。
发热可能的原因:
感染性发热:血流感染?MDR-HAP?IPA?
非感染性发热:机化性肺炎?结缔组织疾病?血液系统疾病?恶性肿瘤?其它?
气管镜检查:
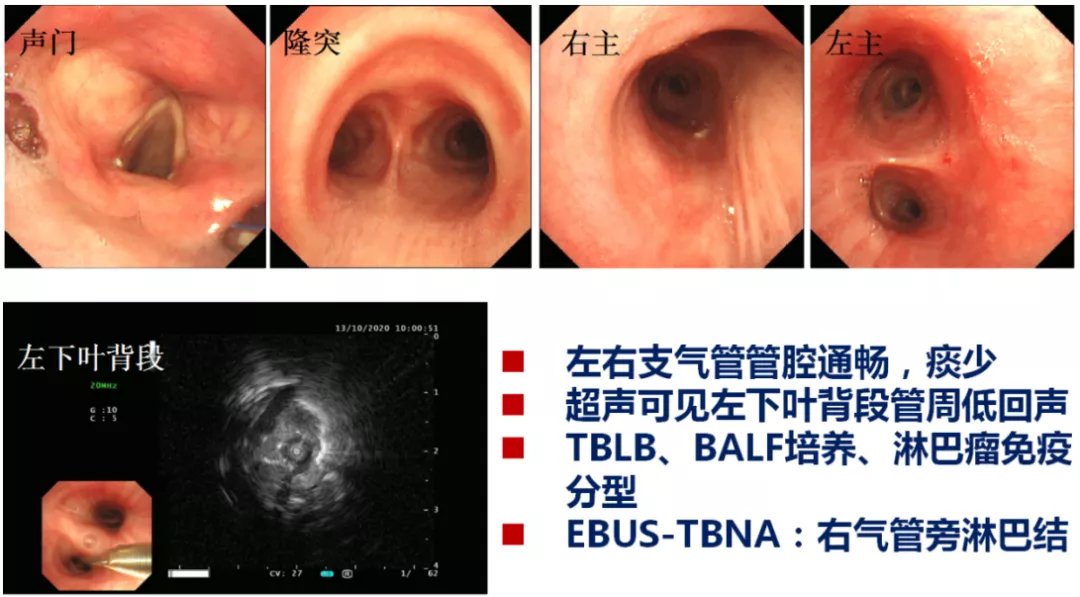
气管镜检查结果:

骨穿检查结果:
我们继续给予患者激素抗炎治疗,并逐渐减少剂量(80毫克-60毫克-40毫克),患者连续13天体温正常,患者饮食可自理,可下床站立,FiO2 30%,氧饱和度可稳定在95%以上,血常规:WBC 13.1ⅹ109/L,LY 0.42ⅹ109/L,NE 12.52ⅹ109/L,CRP 6.41mg/L,降钙素原 0.13 ng/ml,BNP 53.59pg/ml,痰培养结果为碳青霉烯类敏感的肺炎克雷伯杆菌,调整治疗方案为比阿培南联合伏立康唑抗感染治疗,但10-25患者再次出现高热,复查CT影像学再次进展,PET-CT示两肺斑片、结节灶,两下肺膨胀不全均伴葡萄糖代谢不同程度增高(SUVmax:3.1)考虑感染可能大,两侧胸腔、心包积液;右侧第5-9肋陈旧性骨折;脾大;右上颌窦炎。

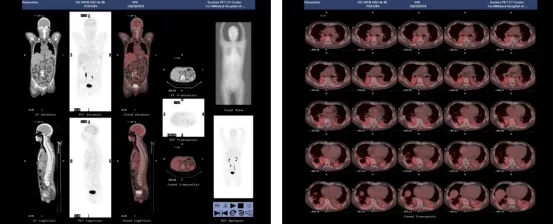
王希明主任医师(影像科)讨论:
患者经系统抗微生物、抗炎治疗后,9-28胸部CT与9-21胸部CT相比,左肺下叶病变有所吸收,10-05胸部CT显示左肺下叶病变增大,呈实性病变,除了一不规则空洞样外,病变密度较均匀,支气管充气征不明显,与常见大叶性肺炎不同,提示肺泡及小支气管均有炎性渗出或其他病理组织充填。应用激素冲击治疗后,10-16复查CT显示左下肺病变较前有所吸收,提示病变对激素治疗敏感。但10-28胸部CT显示左下肺病变又有进展,且右肺下叶出现团状实变病灶,与9-09外院CT所示左肺下叶病变相似,提示右肺下叶病变可能与左肺下叶病变同源。
综合上述影像学表现,左肺下叶实变病灶在短期内出现反复变化,但始终未完全吸收,且于10-28又出现右肺实变病灶,因此该患者需要与肿瘤、风湿免疫相关疾病及少见的病变进行鉴别。需要与肺炎性实变相鉴别的肿瘤包括淋巴瘤及炎性肺癌。肺内原发淋巴瘤的病理类型为粘膜相关淋巴瘤,可以表现为结节、肿块型、肺炎型、淋巴管型及粟粒型,肿块或肺炎型多表现为边界模糊的实变影,支气管充气征多见,病变可跨叶生长,CT增强后可见血管征表现,与该病例影像学表现有所差异,且肺MALT淋巴瘤属于惰性淋巴瘤,好转及进展均较缓慢,临床症状较轻,也与本病不符。炎性肺癌又称作「实变性」肺癌,实性病变多分布在肺外周,呈膨胀性生长特点,其内可见多发小囊腔类似蜂窝征,也可见支气管充气征,实性病变周围呈磨玻璃影,周边多有结节灶,也可见CT血管征,与该病例表现不同,炎性肺癌很少在短期内出现明显变化。另外,PET-CT显示两肺病变SUV值稍高,也可排除肺肿瘤的可能。风湿免疫相关疾病对激素治疗较敏感,但影像学上主要表现为弥漫间质性病变或肉芽肿性病变,与该病例影像学表现不同,且该患者的实验室检查指标也不支持该类疾病诊断。隐源性机化性肺炎对激素治疗敏感,影像学科表现为多样性、多变性,也可表现为实变影,与该病例影像学表现相似,但COP多伴发间质纤维化表现,该病例间质纤维化表现不明显。综上所述,该病例虽可以基本排除肿瘤性病变,但具体病因诊断通过影像学较难判断,因此,建议对病变穿刺活检,以进一步明确诊断。
武剑主任医师(风湿免疫科)讨论:
该患者中年男性,起病急,表现为重症肺炎,抗感染治疗疗效不佳,激素有反应,但减量后反复。从风湿免疫科角度,需要鉴别的疾病包括:肌炎相关间质性肺病,包括皮肌炎尤其是抗MDA5阳性皮肌炎、抗合成酶综合征,前者有典型皮肤表现如向阳疹、Gottron征等,后者有技工手、肌炎、雷诺现象等,目前患者体检及相关检查均不支持,但临床也有以肺部病变为首发表现的皮肌炎、抗合成酶综合征,相关抗体检测也有一定的漏诊率,建议送不同实验室复测肌炎抗体谱进一步明确。其他结缔组织病如SLE、RA、干燥综合征、ANCA相关性血管炎等目前均无依据。
患者有两次抗Ro52抗体阳性,但该抗体无特异性,可见于多种结缔组织病、其他自身免疫病、肿瘤等,此外,在CTD-ILD中,出现抗Ro52抗体常提示ILD病情更重。
总之,该患者重症肺炎如此凶险难治,高度提示其存在潜在基础病,重点需复查相关抗体排除皮肌炎、抗合成酶综合征,此外,恶性肿瘤尤其是淋巴瘤也需行进一步检查包括肺活检寻找依据。
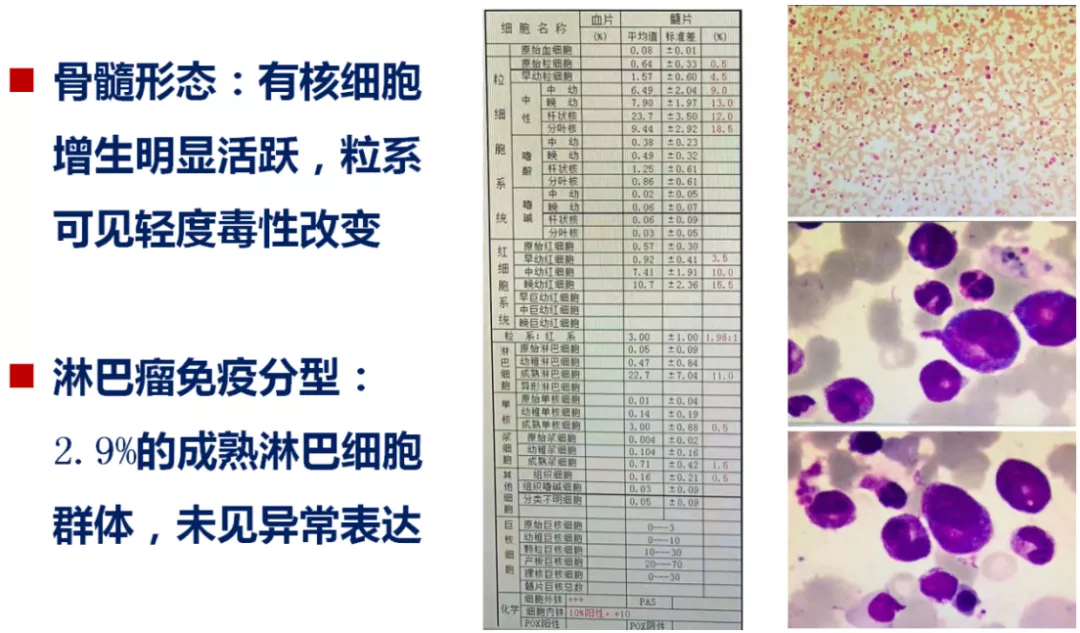
孙爱宁主任医师(血液科)讨论:
病例特点:1、患者中年,男性,急性起病;反复发热,有反复肺部感染征象。2、外周血白细胞升高,中性粒细胞明显升高,淋巴细胞比例明显下降;骨髓检查:粒系增生活跃,形态正常。3、炎症指标(PCT、CRP、IL-6)升高,细胞因子风暴引发多脏器受损。4、多种微生物混合感染或定植,抗生素治疗疗效欠佳。5、糖皮质激素反应(+)。
针对以上特点,从血液科角度分析:
1、感染引起的类白血病反应 患者发热感染,但无NAP强阳性,外周血中无中幼粒、晚幼粒及核左移现象。不是多药耐药、泛耐药菌感染,宿主也无免疫功能缺陷,为何抗感染疗效不佳?
2、慢性中性粒细胞白血病 属于非常少见类型的慢性白血病。起病缓慢,乏力低热,肝脾肿大,无淋巴结肿大。外周血白细胞升高,一般大于25x109;中性粒细胞升高,原始细胞小于10%,流式细胞术检查提示:有异常中幼粒表型。此病人流式无异常,染色体正常,BCR/ABL融合基因阴性,可排除慢性白血病。
3、急性发热性嗜中性粒细胞性皮肤病( Sweet 综合征) 发病机制尚不明确,可能与感染、药物及肿瘤等因素有关。20%的病人合并恶性肿瘤,其中血液系统恶性疾病占80%,主要有急、慢性白血病、骨髓增生异常综合征等;也可见于一些实体瘤。主要表现:特征性皮损,真皮内中性粒细胞侵润;发热,中性粒细胞升高,糖皮质激素反应非常好。文献报道:急性白血病合并Sweet综合征,治疗后不易缓解,反复发热、皮损,预后差。两者可同时发病,也可先后出现临床表现。本病例有急性发热,中性粒细胞明显升高,但无特异性皮疹。需继续随访,进一步检查,以明确诊断。
张秀琴主任医师(呼吸与危重症医学科)讨论:
这个病例确实比较复杂,可以说集中了我院多个学科的专业力量对这个患者实施了救治。从诊断思路上来讲,该患者确实有顽固性发热,但是他不是一般意义上的发热待查。这个患者入院时除了发热,影像学肺部有渗出性的病灶,所以入院时 CAP的诊断是可以确立的。但是在后续的诊疗过程当中,虽有多次找到病原学的证据,比如找到肺炎克雷伯菌,找到葡萄球菌以及真菌感染的证据,但是相对应的一些抗感染治疗并没有拿到非常好的疗效。
该患者从入院到现在已经大约三周了,除了顽固性的发热,有几个重要的临床特征需要关注:第一,肺部病灶进展迅速,来的快,去的也快。第二,对激素敏感。第三,同时合并心功能不全。
基于上述这些特征,我们对病因的探寻有如下思考:1、这个患者,不是一般意义上的 CAP,因为一般 CAP 影像学的病灶不可能在 48 小时左右有明显消散吸收。2、根据以往经验,肺部有渗出性病灶、有发热,同时又对激素敏感,我们可能会考虑到一些少见病,比如说隐源性机化性肺炎、粘膜相关性淋巴瘤等等。3、检验结果两次提示 RO-52 抗体阳性,我们也考虑是否存在风湿免疫性疾病。因为一些免疫相关疾病,比如说皮肌炎,诊断上也是有一定难度的。另外,这个患者心功能不全的病因始终是个谜团。当疾病病因探寻之路陷入僵局时,常规的诊断思路是去争取获得病理诊断。所以我们此时建议患者,接受一些有创的操作,获取病理组织,拿到病理诊断,从而为该患者后续的诊疗打开局面。
经皮肺穿刺病理结果:
1、左肺原发病灶:慢性炎伴肺泡上皮增生、间质纤维化,局灶见凝固性坏死。

2、右肺新发病灶:镜下见肺泡腔内大量纤维素及以中性粒细胞为主炎细胞渗出,肺泡间隔毛细血管受压。
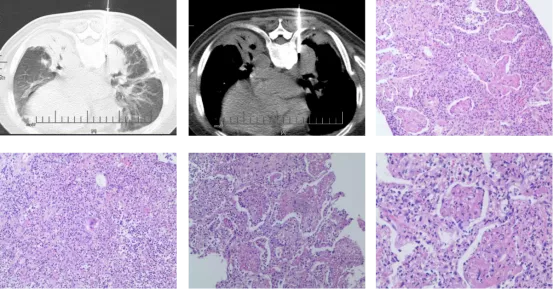
郑玉双博士(病理科)分析:
穿刺镜下表现:弥漫性的肺泡腔内充满以中性粒细胞为主的渗出,肺泡壁结构没有明显破坏,整体符合大叶性肺炎灰色肝样变期表现,引起大叶性肺炎的原因很多,此次穿刺病理并不具有特异性,还需结合临床其它检查寻找病因。
穆传勇主任医师(呼吸与危重症医学科)总结分析:
患者两侧肺穿病理诊断均考虑大叶性肺炎,但是这个患者真的就是普通的大叶性肺炎吗?病理诊断显然和我们的临床需求还有一定差距。由于前面的两次气管镜TBLB和EBUS-TBNA标本均没有明确诊断,所以我们在完善PET-CT的前提下先后两次给予经皮肺穿刺活检,第一次穿刺点为左下肺病灶,其病灶特点是最早出现,多次检查变化不大,相对稳定,经皮最近,穿刺风险小,但是病理是上皮增生,部分凝固型坏死,显然与临床需求有差距。组内经过充分讨论,充分准备,充分沟通,第二次选择了右下肺穿刺活检,其特点是新发,病理更贴近诊断,但是病理依然是大量中性粒细胞的渗出,这显然也不能满足我们临床的需求。虽然两次病理没有给我们明确诊断,但是结合患者临床特点,诊疗过程,也可以发现其对激素治疗相对敏感,对后续的诊断和治疗应该可以给出很好的参考。当然穿刺过程也不是一帆风顺,第二次穿刺过程出现了血胸,也提示我们学员在进行任何操作前应该进行充分的沟通、准备以及抢救预案。
随着体温再次升高,影像学快速进展,患者胸闷气喘症状进行性加重,呼吸频率大于30次/分,痰鸣音明显,并出现意识障碍和血液动力学不稳定,动脉血气,氧合指数小于200mmHg。BNP再次升高到13558pg/mL,淋巴细胞计数为0*109/L,血小板为27*109/L,CRP为269.24mg/L,2020-11-02再次气管插管呼吸机辅助通气转入RICU。
第二次RICU
诊疗方案
机械通气,强心利尿,改善心功能,营养支持,人免疫球蛋白、人血白蛋白支持治疗
激素治疗:120毫克-80毫克-40毫克
抗感染:美罗培南+伏立康唑片剂+利奈唑胺片剂+SMZ
动脉血气( FiO2 30% ):PaO2 86.0 mmHg,氧合指数:287mmHg
血常规:WBC 11.8ⅹ109/L,LY 0.4ⅹ109/L,PLT:81ⅹ109/L
CRP:46.64mg/L
降钙素原:0.14 ng/ml
BNP:3435pg/ml
气管插管第八天,成功撤机,续贯鼻导管吸氧,复查动脉血气(鼻导管吸氧FiO2 29%):PaO2 87.4mmHg。2020-11-13复查CTPA示:胸部右下肺动脉部分分支内血栓形成,左下肺动脉局部分支充盈欠佳,少许血栓。后患者甲强龙逐渐减量,抗感染降级,低分子肝素抗凝,患者恢复良好,精神佳,呼吸平稳,体温正常,仍有咳痰,稀薄,2020-11-17转入普通病房。
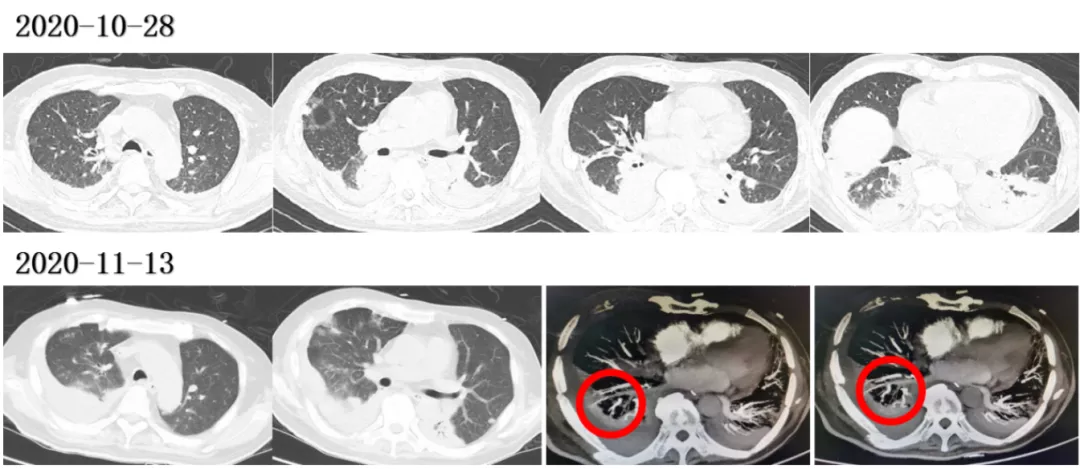
刘超主治医师(PCCM学员)两次气管插管脱机成功的经验分析:
该患者两次病情恶化入RICU,救治的过程是成功的,我们都参与了其中,个人有几下几点体会。一是患者出现氧合恶化,呼吸窘迫,达到气管插管指征,需要及时的插管,以避免呼吸失代偿加重脏器功能损伤。二是治疗期间做好脏器功能的支持和内环境的管理,必要时CRRT支持。三是,病情好转符合撤机拔管指征,则及时撤机拔管,以减少院感的发生。
目前,患者病情阶段性好转,留给我们很大的困惑是诊断未充分明确。患者第二次有创机械通气时间在一周左右,病程较一般重症肺炎短,获取的病原学依据不能充分解释病程;CTPA发现局部肺动脉分支血栓,但不能解释反复高热呼衰及快速变化的特点。EBUS-TBNA及肺穿刺活检的病理结果也没有指向特异性的诊断。所以这个病人的诊断非常困难。
但是要说有什么启示的话,就是我们发现该患者的病情恶化是出现在激素减量过程中,两次成功的救治都伴随着激素加量,反映该疾病可能对激素敏感。可能是一个线索。在发热伴肺部阴影的疾病谱中,对激素较敏感的疾病主要有结节病,机化性肺炎,过敏性疾病,自身免疫性疾病,以及淋巴瘤等,但目前都不能建立诊断,会不会是其他比较少见的疾病,还需要继续寻找依据。
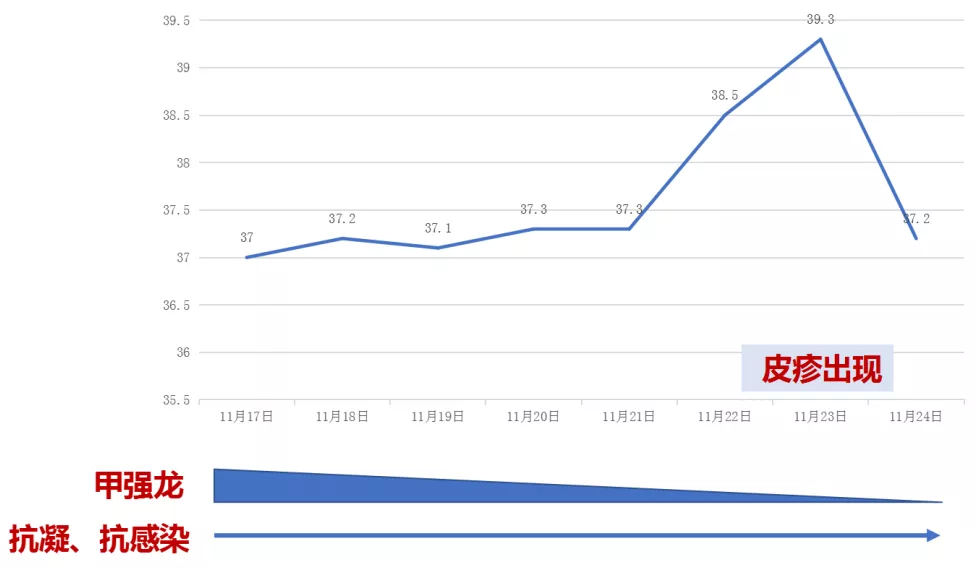

随着激素减量和抗生素降级患者再次出现体温复升,同时四肢出现皮损。
讨论3:皮损原因?
A.皮肤感染
B.药物相关性皮损
C.其他疾病的皮肤表现
D.皮肤相关原发病
邱冬主治医师(PCCM学员)分析:
首先,患者病程中长时间使用抗菌药物,此时出现皮损需警惕药物性皮炎。其次,患者淋巴细胞长期处于低水平状态,机体免疫功能低下,病程中伴随长时间的广谱抗菌药物及糖皮质激素使用,皮损还应鉴别继发的皮肤感染,比如真菌性皮肤病,皮肤结核等,后续可予以完善分泌物培养及组织培养予以鉴别。我们回顾患者整个病程可以发现患者的热峰与激素使用剂量相关,这提示我们患者有可能存在某种尚未明确的潜在基础疾病。比如结缔组织疾病中的白塞病,患者可表现为阴囊溃疡、结节红斑,少数患者还可以出现发热症状,再比如淋巴瘤的患者也可以出现红斑、丘疹、脓疱等皮肤表现。患者此时出现的皮损有可能是潜在疾病的皮肤表现,后续可以予以完善皮肤活检予以鉴别。最后患者的皮损还需要鉴别原发的皮肤疾病。
周乃慧主任医师(皮肤性病科)分析:
中年男性患者,在住院期间出现皮损,皮损主要分布在四肢,最初的皮损为散在分布的淡红色丘疹,粟粒至绿豆大小,部分丘疹的顶端有小脓疱;但2天后,这些小的丘疹就迅速进展为水肿性斑块,而且部分皮损中央出现了破溃。
可能原因有:(1)药物因素:患者住院期间使用了多种药物,需进一步排查药物过敏的可能,并密切观察皮疹有没有进一步加重的趋势,必要时需要停用可疑的致敏药物;(2)感染:患者一直有发热,住院期间系统使用了糖皮质激素,而且皮损有破溃,需要排除感染所致的皮损,感染包括真菌、细菌以及其他的特殊感染如分枝杆菌等;(3)肿瘤:患者进展后的皮损为水肿性斑块,伴有破溃,需要排除血液系统或者内脏肿瘤累及皮肤的的可能,另外也要排除原发于皮肤的肿瘤如皮肤淋巴瘤;(4)炎症性皮肤病或结缔组织病:包括了血管炎、脂膜炎等。为明确诊断,我们需要进一步完善皮肤病理检查和微生物学检查。
患者持续高热,胸闷气短进行性加重,痰鸣音明显,血常规:WBC 15.64ⅹ109/L,Ly 0.28ⅹ109/L,NE 15.28ⅹ109/L,CRP:281.91,降钙素原:1.21 ng/ml,BNP:5091pg/ml,动脉血气:鼻导管吸氧5L/min, PaO2 126mmHg,11-25复查胸片较前明显进展,第三次转入RICU。
第三次RICU

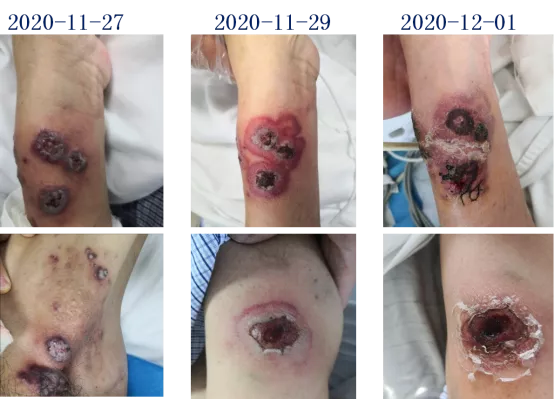
转入RICU后完善怕皮肤活检及分泌物培养,同时继续抗凝抗感染,呼吸支持,激素逐渐加量,营养支持等综合治疗,但患者病情无明显好转,炎症指标、氧合指数、心功能、乳酸、影像学等重要指标再次急剧恶化,于2020-12-02再次气管插管呼吸机辅助通气,俯卧位通气,以及床边持续血液净化治疗(CRRT)。


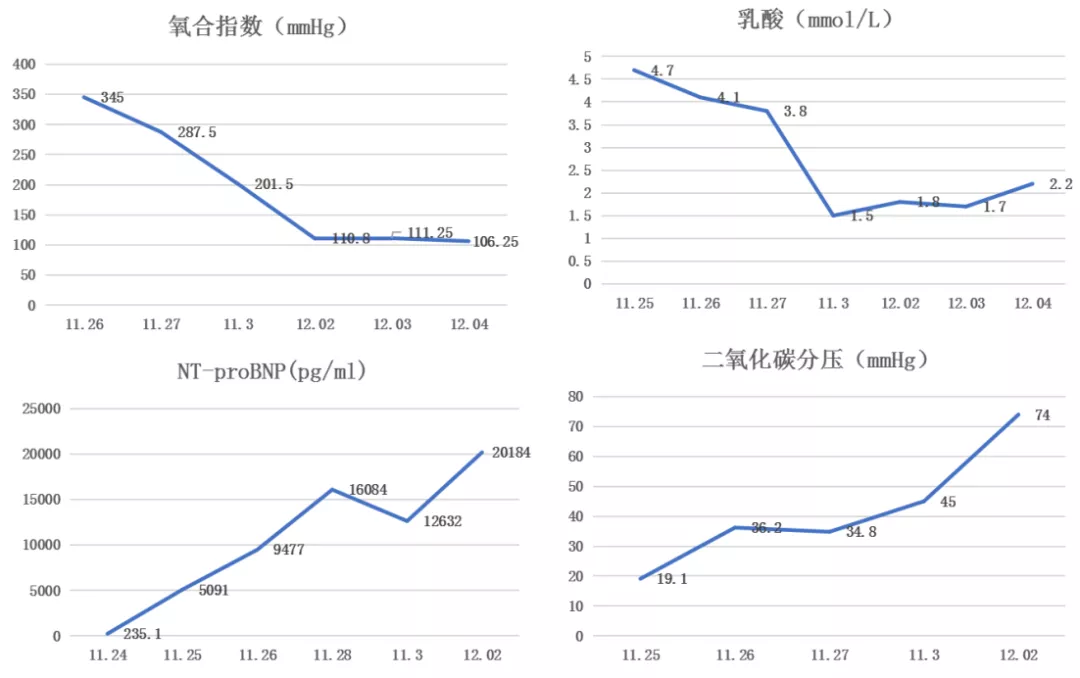
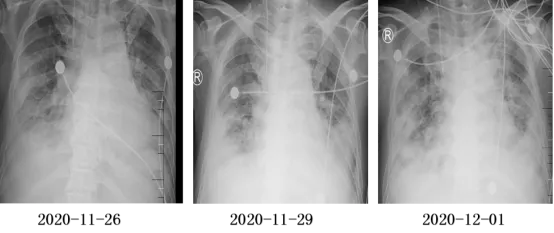
王晓飞副主任医师(PCCM学员)分析病情变化:
这个阶段患者出现皮疹,与患者发热、肺部病变是一元论还是疾病发展过程中的插曲,也是值得我们关注的。结合皮肤科周主任的分析,综合考虑患者疾病可能原因:首先患者广谱抗生素、激素的使用,可出现二重感染,如播散性细菌感染,分枝杆菌、真菌感染等。其次患者发热、肺部病变、皮疹,还是要再次考虑自身免疫性疾病,如皮肌炎、血管炎、白塞病等。第三患者病情变化、治疗一波三折,需考虑肿瘤性疾病、血液病、少见系统性疾病的可能。下一步希望通过皮肤分泌物、组织培养和病理结果,为我们诊断和治疗提供更多线索。
辅助检查
痰培养:鲍曼不动杆菌(CR-AB)
血培养:阴性
导管尖端培养:阴性
肺泡灌洗液常规培养:阴性
肺泡灌洗液真菌培养:阴性
皮损相关检查结果
涂片:找G-球菌(3次)未找到细菌;找结核杆菌(3次)未找到抗酸杆菌;找霉菌(3次)未找到霉菌
培养:热带念珠菌(少量)
细胞分类:大量中性粒细胞
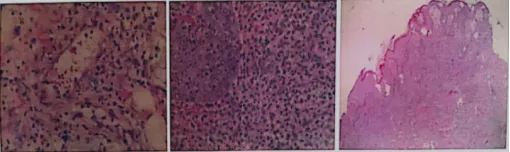
皮肤活检(左前臂,第一次)病理:真皮层见大量中性粒细胞浸润

皮肤活检(左腹股沟):急性化脓性炎,部分表皮剥脱,真皮层附件区脂肪层均见大量中性粒及脓细胞及炎性坏死,局灶中-小静脉壁破坏伴出血及炎细胞浸润。
特殊染色:PAS染色,六胺银染色,抗酸染色均(-)

皮肤活检(左前臂,第二次):表皮呈假上皮瘤样增生,海绵水肿,有大量中性粒细胞移入表皮,真皮乳头水肿,真皮内弥漫中性粒细胞浸润,血管内皮细胞肿胀,周围中性粒细胞浸润,考虑Sweet综合征(皮肤科病理)。
皮肤科周乃慧主任医师(皮肤性病科)分析解读:
患者的左前臂及左腹股沟皮损的组织病理结果类似:均表现为真皮乳头高度水肿,真皮内弥漫性中性粒细胞浸润,但没有感染性肉芽肿形成。结合微生物学相关的检查:PAS染色、抗酸染色、银染色阴性;分泌物涂片:真菌、G-球菌及抗酸杆菌阴性。排除感染及肿瘤外,结合皮损表现,Sweet综合征诊断明确。
宁卫卫主治医师(PCCM学员)分析:
该患者出现大片皮疹,皮损部位的活检病理报告考虑为Sweet 综合征,因此,给患者的诊断指出了一个方向。该患者皮损部位病理提示存在真皮内大量中性粒细胞浸润,是Sweet综合征的病理特征之一。而我们可以看到,之前的经皮肺穿刺病理也存在大量中性粒细胞浸润,虽然这样的病理结果一般首先考虑为大叶性肺炎表现,但结合上述各位专家的讨论与分析,更倾向于非感染性疾病,且对激素治疗有反应。因此,该患者的肺部表现是否可以用Sweet综合征累及肺部来解释呢?
郑玉双博士(病理科)分析:
患者两肺肺部穿刺活检标本均可见大量中性粒细胞浸润,肺泡壁结构没有明显破坏,整体符合大叶性肺炎灰色肝样变期表现,同样Sweet综合征也是以大量中性粒细胞浸润为主的炎症行疾病,这两者单纯从病理的角度很难区别,Sweet综合征以肺部病灶为首发表现的实属罕见。
王再亮住院医师(PCCM学员)分析:
病程中我们可以看到患者每次病情的加重都会伴随着心肌的损伤,这个心肌损伤可以用Sweet综合征解释吗?就这个问题请教一下心内科赵彩明主任。
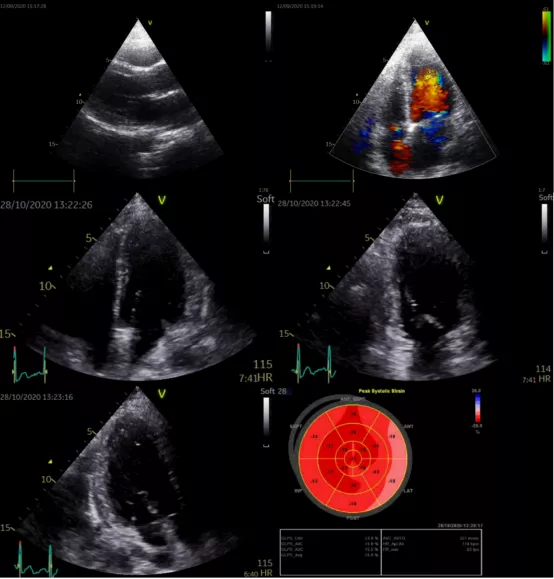
赵彩明主任医师(心血管内科)分析:
下面我从心血管科和心超方面谈一下Sweet综合征对心脏的影响。Sweet综合征是一种非常罕见而且复杂的疾病,据文献报道,除皮肤、肺和其他多种脏器外,也可以累及心脏,但相对少见,主要表现为左心室增大,左心室收缩功能减退,另外,也可能会有主动脉狭窄,主动脉炎、冠状动脉闭塞、心脏肥大等,这个病人的左室长轴切面、心尖四腔切面上肉眼观左房左室大小正常,主动脉瓣、二尖瓣没有明显反流,收缩活动看起来基本正常。前面曾经提及EF测值大概在0.52到0.55,处于正常和非正常的临界状态,我们用二维斑点追踪模式来测量左室的应变,从而观察左室的收缩功能,这种方法,要比常规方法敏感,颜色亮红表示收缩正常,亮红、淡红、粉红、白红,颜色变浅表示收缩逐步减弱,应变绝对值20左右正常,17-20属于临界状态,17以下认为有心肌损害。我们通过左室牛眼图可以观察到部分心肌呈现亮红色,部分呈淡红色,左室侧壁基底段的心肌呈粉红色,绝对值10左右,说明侧壁这部分心肌受到了损害,结合这个病人的肌钙蛋白以及NT-proBNP多次测值均明显升高,说明这个病人是有心脏损害的,但是在一般情况下,心衰表现并不严重,如果由于容量、感染,缺氧、毒素等因素影响,就有可能对心功能,特别是对舒张功能产生影响,从而会导致左室舒张末期压力增高,导致病人出现胸闷、气急等明显的心衰症状以及相关的指标比如NT-proBNP增高。
Sweet综合征
概述:一种急性发热性嗜中性粒细胞性皮肤病,特征是皮肤嗜中性浸润(表皮、真皮或真皮下),伴有或没有真正的血管炎。突然出现嫩斑块或结节,伴有发热、动脉痛、眼部炎症、头痛,很少出现口腔或生殖器病变。
病因:特发性(最常见),恶性肿瘤(特别是骨髓增生异常综合征),自身免疫性疾病,感染,药物,怀孕等。
发病机制:不确切。遗传因素: HLA-B54、MEFV基因突变、3q染色体异常,对细菌、病毒或肿瘤抗原过敏致中性粒细胞激活和浸润,细胞因子和趋化因子如IL-1和干扰素的作用。
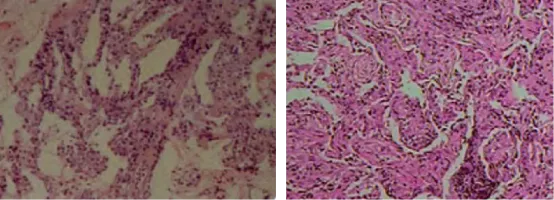
组织病理学:典型组织病理学模式包括网状真皮中弥漫性致密的嗜中性粒细胞浸润,白细胞碎屑核碎片呈间歇性表现,乳头状真皮水肿很常见。真正的血管性变化通常不存在,但可能会发生微血管变化,可能存在嗜酸性粒细胞和淋巴细胞,但以中性粒细胞为主。
肺或气管组织病理与皮肤改变相似,多见于肺实质、间质或气道黏膜有大量中性粒细胞浸润,肺泡灌洗液可见大量中性粒细胞, 或伴肺间质水肿少量淋巴、巨噬、嗜酸等细胞浸润, 纤维化等改变、肉芽组织形成,机化性肺炎甚至符合 COP或BOOP的病理改变。
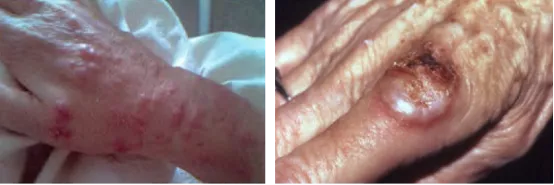
症状和体征:皮肤表现:突然发作、柔软的红斑斑块或不同大小的结节,分布不对称。病变最常见于上肢,也可出现于面部、颈部、胸部、背部和下肢。有文献报道,典型皮肤表现可晚于肺部表现数月。发热几乎总是存在的,其它包括关节痛、肌痛、疲劳、不适和头痛。
皮外表现:动脉硬化、非侵蚀性炎症性关节炎、眼部炎。嗜中性浸润可导致心肌受累、多灶性无菌性骨髓炎、肺泡炎、胸膜积液和无菌性脑膜炎。
诊断标准:2条主要+至少2条次要标准
主要标准:
柔软、疼痛的斑块或结节突然爆发
真皮嗜中性粒细胞浸润,没有血管炎
次要标准:
发热>38℃
起病前存在上呼吸道或胃肠道感染、典型炎症性疾病、恶性肿瘤、妊娠
白细胞数量升高,中性粒细胞优势和炎症标志物升高
皮质类固醇阳性反应
治疗:一定的自限性,对类固醇反应高度敏感。在皮质类固醇逐渐减少后疾病复发时,一些保留类固醇的药物据报道显示有效,包括碘化钾、秋水仙碱、氨苯砜、异维甲酸、甲氨蝶呤、强力霉素、消炎酸、氯胺霉素和环孢素。抗菌药物治疗无效。
预后:与基础病相关,预后因潜在原因而异,一旦在病程中出现呼吸衰竭,整体预后极差,死亡率约40%,高达69%的患者会在一年内复发。
朱晔涵主任医师(呼吸与危重症医学科)点评:
当皮疹出现及皮疹活检的病理出来后,我们恍然大悟,这是一例以肺部异常为首发表现和典型表现的Sweet综合征,也是一例晚发皮疹的Sweet综合征。我们简短回顾一下前面的诊治。治疗组医生不遗余力地做了多次支气管镜及两次肺活检。肺活检病理特点主要有三个:有中性粒细胞浸润,组织坏死以及大量纤维素形成,没有肉芽肿,没有机化,没有异性细胞,这可以用Sweet综合征来合理解释。Sweet综合征的典型特点就是组织大量中性粒细胞浸润;细胞释放溶酶体,导致组织坏死;修复与损失胶着一起,故出现大量纤维素沉积。心内科赵主任指出患者心衰好转很快,且EF值很快接近正常,这种心衰也可解释为Sweet综合征的心肌损害所致。治疗上,患者两次入住ICU,分别11及8天,就神奇地撤机拔管,可以认为是综合治疗的结果,特别是激素治疗及抗感染治疗。激素在整个病情好转中起了关键作用,Sweet综合征有免疫缺陷,抗感染,特别是针对免疫力低下患者易得的机会感染,如抗凝固酶阴性葡萄球菌及念珠菌,也起了重要作用。接下来的治疗还是要使用激素,甲强龙每天至少要120mg;抗感染要继续,特别是要关注机会感染病原体;呼吸支持及呼吸道管理应当继续做好;还有就是液体平衡及心衰问题,也要关注。
治疗方案调整:
12月4日,予激素冲击(甲强龙 500mg qdⅹ3d)治疗,继续加强抗感染,呼吸机辅助通气和CRRT治疗,但患者病情无明显改善,相关指标继续恶化。
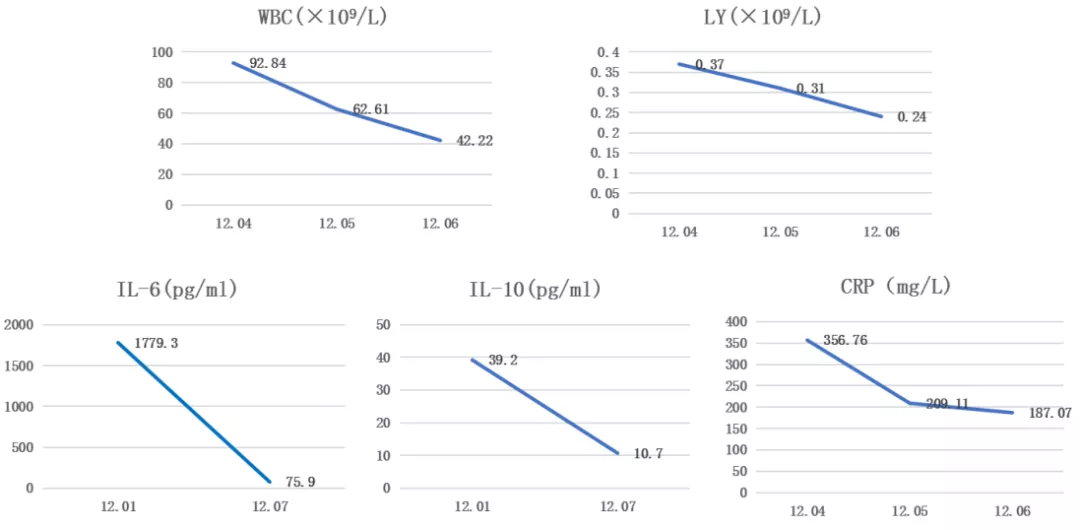
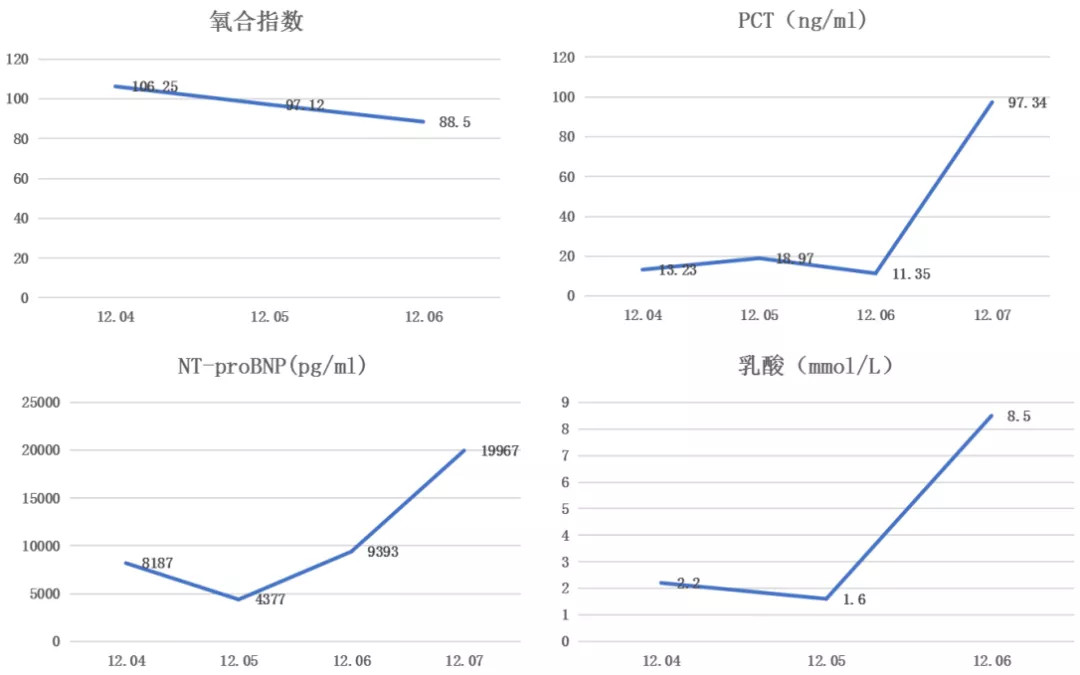
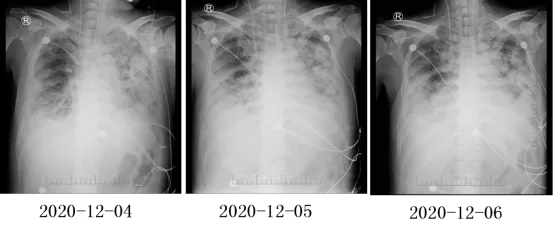
赵卫峰主任医师(感染科)点评:
这个患者发热待查入院,肺炎起病,伴有呼吸衰竭和心肌损伤,激素治疗有效,减量后病情反复,后来出现皮疹,经过肺部和皮肤活检证实是Sweet综合征,Sweet综合征是对激素治疗有效的,可以看到,开始的时候激素的冲击治疗炎症指标是改善的,但是其他的指标改善并不理想。感染指标PCT明显升高,说明除了Sweet综合炎症反应之外,再结合长期的发热,大量使用广谱抗生素及激素,淋巴细胞低至0,所以存在严重的免疫力低下,同时,皮肤分泌物培养到念珠菌,这是用Sweet综合征无法解释的,所以更要考虑二次感染,机会感染的可能,要重视病原学的检查,比如血培养、痰培养、G/GM试验、甚至肺泡灌洗等。
雷伟主任医师(呼吸与危重症医学科)点评:
这个病例很曲折,从这个患者的诊治过程我们可以看到倾注了床位医生和主管主任的大量心血,我们可以看到患者及其家属对我们的高度配合,医患关系的高度和谐。在前面的诊疗过程中,我注意到该患者进行了2次肺部组织的活检,一次经皮肺穿刺,一次TBLB+EBUS,病理结果一次为凝固性坏死,一次为大量中性粒细胞的浸润。两次皮肤活检,真皮内也可见大量中心粒细胞浸润。骨穿没有异常发现。PETCT提示肺组织和上颌窦有高代谢病灶。目前诊断上我也存在一些困惑,肺部的病灶是否可以用一元论解释,肺部的病灶是否可以和皮肤及心脏等其他部位的脏器受累用一元论来解释。因此接下来,诊断方面,我觉得,是否可以进一步行鼻窦和心肌组织的活检,进一步证实,或者就像刚才专培学员陈澄医师文献复习中介绍的,从HLAB54,MEFV,3q染色体等分子遗传学角度进行一些检测进一步证实。治疗方面,前面已经大剂量激素冲击治疗,效果不佳,接下来是否考虑免疫调节剂,丙球的冲击治疗,血浆置换等治疗手段。
陈成主任医师(呼吸与危重症医学科)点评:
这个病人很不容易,第三次进入RICU,肺部出现广泛改变,同时伴随感染、容量负荷相关指标的明显变化,临床期待采用大剂量激素的治疗能够减轻基础病相关的脏器损伤,但这个时候有两点需要注意,第一个是感染的问题,看到了皮肤组织培养到了念珠菌,而且PCT有了特别明显的升高,此时脓毒症休克应该存在了;第二个问题就是激素冲击治疗加重感染的风险。如果脓毒症休克进一步加重,出现血流感染、肺损伤、ARDS,肺部影像学就难以短期改善。
季成主任医师(呼吸与危重症医学科)点评:
这个病例非常「绕」,或者说复杂,干扰因素多。初始起病表现为大叶性肺炎,有典型的临床表现,影像学表现,病原体。但治疗坎坷,反复表现为发热,呼吸衰竭,肺部病变吸收不理想。最后出现皮肤表现,结合活检,考虑Sweet综合症。但这个病例复杂之处正如前面学员宁卫卫所说,在于肺部的病变是否能完全用Sweet综合症解释?我们来回顾一下肺部的穿刺病理,左下肺、右下肺的病变能否用肺炎的不同时期(机化期 灰肝变期)解释?如果这样,为什么积极的抗感染后肺部病灶吸收不明显?Sweet综合症尽管文献报告对激素比较敏感,但我们也注意到,使用激素后,第一次拔管,第二次拔管前后CT肺部病灶吸收都不理想,这也意味着该患者对激素并不敏感,提后预后差。激素冲击过程中出现病情变化,PCT跳升的时候,我同意刚才前面几位主任的意见,需要想到有没有败血症,条件致病菌的可能性。肺部病变那些Sweet综合症所致?那些是感染所致?对这个患者而言,恐怕临床要确认很困难,尤其是各种治疗效果都不好的情况。也许后续观察皮疹的演变有助于该例Sweet综合症患者对激素敏感性的判断。
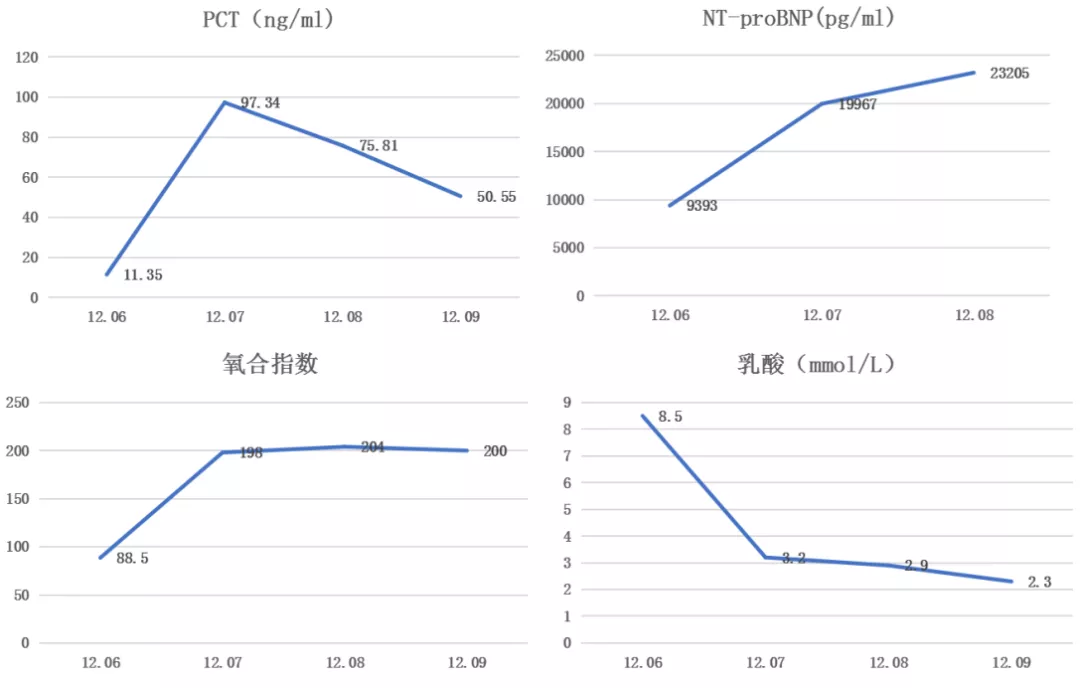
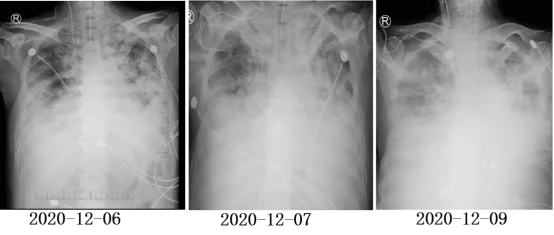
2020-12-06,患者氧合不能维持,机械通气和CRRT的同时使用了ECMO(模式VV-ECMO,FiO2 80%,气流速3.5L/min,血流量3.57L/min),调整甲强龙剂量为240mg QD,全血真菌培养(12.3标本):白色念珠菌(较多),加用两性霉素B抗念珠菌血症,患者病情始终无改善,2020-12-09自动出院。
最终诊断
Sweet综合征
多器官功能衰竭
念珠菌血症
吴巧珍主任医师(苏州市第九人民医院呼吸与危重症医学科)点评:
非常高兴参加苏州大学附属第一医院主办的PCCM疑难病例讨论会,这是一个非常好的病例,历时3月,三入ICU,诊治过程波澜曲折,我们的心情随着病史汇报跌宕起伏,最终的诊断「意料之外」,不良的预后却又在「情理之中」,为什么说是「意料之外」呢?作为非皮肤专科医生比较孤陋寡闻,Sweet综合征还是第一次听说,那为什么又是「情理之中」呢,反复呼吸衰竭入ICU,抗感染治疗无效,糖皮质激素的使用剂量越来越大,我想经治医生心中是很无奈的,作为参访单位成员,从中学习到很多。
一个既往无慢性疾病以及无提示存在免疫功能低下相关病史的壮年男性,发热、咳嗽、咳黄痰,肺部体征有湿罗音,血炎症指标WBC、N%、CRP、PCT等明显增高,胸部CT见左下肺实变影和两肺散在斑片影,根据这些病史特点,首先考虑CAP而且是细菌感染引起的CAP,我觉得诊断思路没有错,当病情出现恶化,及时进行评估、补充诊断、完善相关检查,调整治疗方案。在先后使用比阿培南、利奈唑胺、莫西沙星、亚胺培南、万古霉素、卡泊芬净、伏立康唑以及甲强龙抗炎治疗,病情反复,及时调整思路,从CAP调整到发热待查的诊断思路,那必然是感染性疾病和非感染性疾病这架天平的砝码的较量,在积极进行经皮肺穿、骨穿等有创检查以及PET-CT等一系列检查后,并没有获得可靠的诊断信息,一直到发病3个月后的皮损的出现,给诊断带来了新希望,皮肤活检明确为「急性发热性嗜中性粒细胞皮肤病(Sweet综合征)」。
那么是否可以用Sweet综合征一元论来解释呢?Sweet综合征是原发病因还是继发改变?毕竟在患者皮损出现前3个月已经肺部改变且严重至呼吸衰竭,病程长达3月余,有创机械通气,长时间的广谱抗菌药物以及糖皮质激素的使用,继发感染难以避免。该病人早期表现为发热、呼吸系统和心肌侵犯,并没有侵犯常见的部位骨髓,也并不是在发病初就表现出全部的临床特征,尤其是呼吸道症状先于皮肤症状出现,在今后的工作中我们该如何提高对这一疾病的认识,保持对Sweet综合征这一疾病的警惕性是十分重要的。
黄建安主任医师(呼吸与危重症医学科)总结:
第一点,这个病例最后诊断Sweet综合征,从整个诊治过程来讲,病人无免疫基础疾病,起病急,进展快,病情重,很快进展为呼吸衰竭,起病时的靶器官首先表现为肺,其次为心脏,后面才表现为皮肤损伤。右侧肺新发病灶穿刺在左侧肺穿刺后48小时后进行,病理报大叶性肺炎灰色肝样期表现,大量中性粒细胞浸润,但事实上大叶性肺炎灰色肝样期应该发生在疾病的第2-3周,这与临床不符,结合骨穿及气管镜淋巴结穿刺活检标本病理基本可以排除恶性疾病,如淋巴瘤、肺癌、肉瘤等。对于一个年轻又没有基础疾病的患者来讲,病情如此反复加重,临床常规检查手段并没有找到犯罪病原体,因此从感染的角度并不能完全解释患者的病情变化,后期的皮损及活检从疾病一元论的角度来看完全符合Sweet综合征的诊断。Sweet综合征尽管是皮肤科的常见病,但像该患者起病首先表现在内脏心和肺的应该十分罕见,该患者能够最终确诊得益于我们多学科的团队协作。
第二点,该患者的整个诊疗过程都是在我们PCCM学员的主导下完成的,包括呼吸机、CRRT、床旁影像学快速评估、ECMO、俯卧位通气、气管镜、经皮肺穿刺活检、深静脉置管等,这充分展示了PCCM制度的优势,学员的诊疗水平确实得到很大的提高,特别对于重症患者的诊断和管理更具有先天优势。
第三点,这个患者诊治过程近3个月,期间经历过那么多操作和治疗措施,充分显示了我们团队的沟通技巧,也感谢患者及其家属对我们工作的充分信任、理解和支持,才能让我们最终找到病因。
第四点,该患者整个疾病的诊疗过程得到医院兄弟科室和各位专家的大力支持,充分体现了多学科团结协作的优势,再次表示感谢,也感谢呼吸界给我们这样一个展示的机会。
作者简介

苏楠
PCCM学员;苏州大学附属第一医院,呼吸与危重症医学科,副主任医师,在读医学博士,贵州省铜仁市石阡县人民医院,呼吸科学科带头人,江苏省中西医结合学会呼吸系统专业委员会青年委员。

陈澄
PCCM学员,苏州大学附属第一医院呼吸与危重症医学科,主治医师,2007-2014就读于苏州大学临床七年制,2014年进入苏州大学附属第一医院呼吸与危重症医学科工作至今,熟练掌握呼吸系统相关诊疗操作如气管镜,肺功能,呼吸机等,熟练掌握呼吸系统常见病如肺癌,慢性阻塞性肺病,哮喘,肺炎的诊治,在核心期刊上发表论文数篇。



