抗中性粒细胞胞浆抗体(ANCA)相关性血管炎(AAV)是一类可累及全身多系统的自身免疫性疾病。此类疾病多见于中老年人,并常累及肾、肺、胃肠道、五官及神经系统等,当累及肺时易误诊为呼吸系统疾病,延误诊治。
临床资料
一般资料:
患者,男,32岁,因「咳嗽21 d,咳痰、气促、发热1周」于2018年3月13日入住我院RICU。
现病史:
患者于2018年2月20日无明显诱因出现间断咳嗽,每次咳1~2声,无痰,无畏寒发热,无胸痛,无气促等不适,因症状无缓解,先后辗转至当地诊所、县医院、市级医院完善胸部CT(图1)等检查后,予以抗感染、抗病毒等治疗,症状未得到有效控制,咳嗽症状明显加剧,以刺激性干咳为主,夜间症状明显。3月3日开始出现发热症状,体温高达38°C。3月7日出现咳白色黏液痰,并有痰中带血,量不多。于3月9日转入我院急诊科(图2),予以「利奈唑胺+伏立康唑片+莫西沙星针」治疗,但患者症状持续加重,血气分析提示低氧血症,于3月12日下午行无创呼吸机辅助通气治疗。因患者症状改善不明显,气促、发热症状未缓解,于3月13日转入RICU。
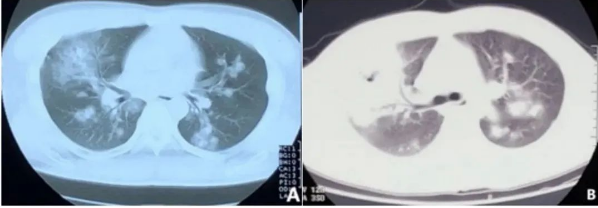
图1 患者外院CT
注:3月2日外院CT提示右肺可见大片高密影,左肺可见散在病灶;3月6日外院CT提示双肺多发斑片状影,右侧为甚。

图2 我院急诊CT(3月9日)
注:双肺多发病变,感染可能性大,其中右上肺可见空洞。
既往史及其他:
既往体健,2018年1月曾夜间在酒店地毯上睡觉,后有受凉症状,出现咳嗽,咳少许白色黏液痰,在诊所输液治疗后症状消失。从事金属机械加工行业8年,有金属粉尘及化学制剂气雾接触史。吸烟5年,日均3~6支,偶有饮酒。其母亲于2014年因「肠癌」过世。
入院查体:
T 36.5℃,P 100次/min,R 30次/min,BP 112/64 mmHg,无创呼吸机辅助通气(ST模式,IPAP 14 cmH2O, EPAP 7 cmH2O,氧浓度60%~80%)。神志清楚,急性危重面容,平车入病房。全身皮肤未见出血点、皮疹,浅表淋巴结未扪及肿大。口唇微发绀。胸廓无畸形,双侧语音震颤对称,呼吸运动度对称,双肺叩诊清音,双肺呼吸音低,未闻及干/湿啰音。心、腹未见异常。四肢肌力肌张力正常,双下肢不肿,病理征未引出。克布氏征反射阴性。
入院诊断
①双肺病变并发热查因:重症肺炎(金黄色葡萄球菌?诺卡菌?真菌待排?)血管炎并感染?Ⅰ型呼吸衰竭;②低蛋白血症;③肝功能不全;④轻度贫血。
治疗经过
入院后治疗暂予以「注射用盐酸万古霉素+注射用头孢哌酮舒巴坦+复方磺胺甲噁唑片」抗感染治疗。3月14日患者因无创呼吸机辅助通气不能维持氧合,改用经鼻气管插管接有创机械通气辅助。插管后查体:HR 158次/min,RR 48次/min,BP 105/50 mmHg,SpO2 82%。神志躁动,气管插管内可抽吸出血性分泌物,双肺可闻及干/湿啰音及哮鸣音。床旁支气管镜检查可见气道内血性分泌物。床旁重症超声示双下肺重力区肺实变明显。复查血气提示氧合差,于3月15日凌晨予以V-V ECMO生命支持,转机后1 h复查血气分析提示氧合改善。
3月16日接相关结果回报:①抗中性粒细胞胞浆抗体:pANCA阴性,cANCA阳性;②血管炎三项:抗蛋白酶3抗体IgG型阳性;③电镜下观察送检肺泡灌洗液沉淀:灌洗液沉淀中见少量球菌及杆菌。明确「ANCA相关性血管炎(GPA可能性大)」诊断。
于3月16日开始予以「甲强龙+血浆置换+环磷酰胺」治疗,并调整抗感染药物方案为「注射用头孢哌酮舒巴坦+伏立康唑片+注射用盐酸万古霉素」。患者血象下降,体温恢复正常,氧合稳定,查重症超声肺部情况稳定好转。3月27号撤除ECMO,3月28日撤除有创通气。分别于3月30日、4月6日复查胸部CT:双肺多发病变较前明显吸收,右上肺空洞性病变实变部分较前明显吸收,留有空洞(图3)。转风湿科普通病房巩固治疗后出院。
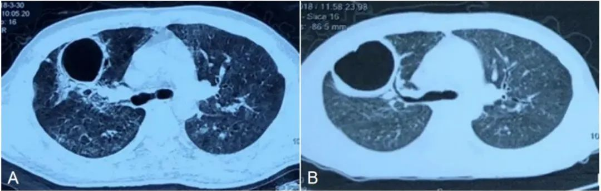
图3 两次复查胸部CT均可见右上肺空洞病灶
出院后继续口服甲泼尼龙片及间断静脉使用环磷酰胺治疗,甲泼尼龙片由出院时48 mg逐渐减量为12 mg(7个月随诊),随诊7个月后复查胸部CT可见右上肺空洞消失(图4),患者一般情况稳定。

图4 患者复查胸部CT
注:A、B、C分别为5月12日、6月26日、8月17日的胸部CT,可见右上肺空洞逐渐缩小;D为11月1日胸部CT,可见右上肺空洞消失。
讨论
AAV是一类与ANCA相关和小血管受累为主的系统性血管炎。根据2012年Chapel Hill分类标准分为:肉芽肿性多血管炎(GPA)、显微镜下多血管炎(MPA)和嗜酸性粒细胞性肉芽肿性多血管炎(EGPA)[1]。目前,随着对此类疾病认识的加深,检测手段及诊断标准不断完善,多学科均对此类疾病予以了重视。肾脏是AAV最常见的累及部位,其次是肺,因其临床症状与体征无特异性,与肺部疾病鉴别困难,导致不能得到及时有效的诊治而预后差。
针对本例患者的诊治经过,有下列表现可以帮助诊断:①有发热、咳嗽、咳痰、持续加重的低氧性呼吸困难、咯血,前期广覆盖抗感染和抗病毒等治疗无效,相关细菌培养、病毒、真菌等培养均未明确致病菌。②肺部CT可见结节或结节密度增高影,可有空洞形成;或可见肺实变和片状或弥漫性磨玻璃影。③有呼吸系统外脏器病变情况,如肾功能损害、血尿、鼻窦病变等。④排除结缔组织、肿瘤等相关疾病。如有上述情况则需尽快完善血管炎三项检查和抗中性粒细胞胞浆抗体检测,有肾损伤者可完善病理活检。研究指出,cANCA合并抗PR3抗体阳性和pANCA合并抗MPO抗体阳性用于诊断AAV的特异性可达99%[2]。本例患者通过肺部影像学表现、cANCA合并抗PR3抗体阳性确诊AAV,并及时采取了针对性治疗。
AAV分为诱导缓解和维持治疗,目前诱导缓解疗效肯定的方案为激素和环磷酰胺冲击治疗[3],同时根据病情可联合血浆置换或大剂量丙种球蛋白。AAV累及肺时,常因弥漫性肺泡出血引起Ⅰ型呼吸衰竭而危及生命。本病例早期即出现弥漫性肺泡出血,有严重的低氧血症,在积极予以V-V ECMO及有创呼吸机提供生命支持的同时,采取了甲强龙+环磷酰胺+血浆置换的治疗策略,迅速控制了病情[4],通过血浆置换清除体内高效价ANCA和其他致病因子,可迅速有效地缓解肺泡出血。
通过有效治疗,AAV患者目前的5年生存率可达70%左右[5]。其主要死因为感染[6],以肺部感染为主[7],此多与患者基础疾病及免疫抑制治疗有关。免疫抑制剂的合理使用是改善预后的重要因素,目前推荐激素起效后迅速减量,环磷酰胺使用静脉给药。本文报道的病例为青年男性,既往体健且病变仅累及肺,规律予以甲泼尼龙及环磷酰胺治疗。
总之,肺受累的AAV在临床上无特异性表现,误诊率高,需要增强对此类疾病的认识,尽早准确诊断、及时规律治疗是改善预后的关键。
参考文献
[1] Jennette J C, Falk R J, Bacon P A, et al. 2012 Revised International Chapel Hill Consensus Conference Nomenclature of Vasculitides[J]. Arthritis Rheum, 2013, 65(1):1-11.
[2] 陈凌舟,彭卫华.抗中性粒细胞胞质抗体相关性小血管炎发病机制研究进展[J].临床肾脏病杂志,2017,17(3):185-188.
[3] 李丽雅,左晓霞.抗中性粒细胞胞浆抗体相关性血管炎的诊治进展[J].临床内科杂志,2014,31(10):661-664.
[4] 夏正坤,何旭.血浆置换治疗抗中性粒细胞胞质抗体相关性血管炎专家共识解读[J].中华实用儿科临床杂志,2018,33(15):1136-1137.
[5] 戴青,鲍春德.ANCA相关性血管炎的治疗与预后[J].实用医院临床杂志,2011,8(2):5-7.
[6] 杨柳,谢红浪,刘正钊,等.抗中性粒细胞胞质抗体相关血管炎合并感染患者的临床特征[J].肾脏病与透析肾移植杂志,2015,24(4):331-336.
[7] 张清,周惠琼,郭娟,等.抗中性粒细胞胞质抗体相关性血管炎死亡危险因素的探讨[J].中华医学杂志,2017,97(43):3392-3395.
作者:李园园,杨文哲,潘频华;单位:中南大学湘雅医院呼吸与危重症医学科
本文转载自订阅号「重症肺言」
原链接戳:以肺脏受累为主的ANCA相关性血管炎



