第二部分:诊断篇
一、2019年《欧洲急性肺栓塞诊断和治疗指南》
诊断
随着人们对静脉血栓栓塞性疾病认识的提高以及无创性影像检查(主要是CTPA)的日益普及,临床医生对肺栓塞(PE)疑诊并进行确诊检查的频率较过去越来越高。在评估现代PE的无创诊断策略时,至关重要的问题是确保无创诊断策略能够在当前患者人群中安全地排除PE。因此,阳性检查应具有足够的特异性以确定抗凝治疗的适应证。
1、临床表现
急性PE的临床症状和体征缺乏特异性。如果患者出现呼吸困难、胸痛、先兆晕厥或晕厥、咯血时都可以疑诊PE。血液动力学不稳定是一种罕见但非常重要的临床表现,因为它经常提示中央型或广泛的PE和血流动力学储备能力严重降低。晕厥可能会发生,并与血液动力学不稳定和右心功能障碍的发生显著相关。
某些情况下,PE可能无症状,或者可能是在另一种疾病的诊断过程中偶然被发现。
在中央型PE中,呼吸困难可能急性发作且非常严重;在小的周围型PE中,呼吸困难通常比较轻微或短暂。在有心衰或肺病病史的患者中,呼吸困难加重可能是PE的唯一症状。
胸痛是PE的一种常见症状,常由远端血栓栓塞导致肺梗死引起的胸膜刺激所致(胸膜炎性胸痛)。中央型PE中,胸痛亦可有典型的心绞痛特征(心绞痛样胸痛),反映右心室心肌缺血,需要与急性冠状动脉综合征或主动脉夹层进行鉴别。
2、临床可能性评估
结合症状、体征及VTE的易患因素,可将疑诊PE的患者分为不同程度的临床可能性。这种预测评估可以通过临床经验判断或使用预测规则完成。PE的诊断后测试概率不仅取决于诊断检测本身的特点,还取决于临床可能性,这是PE诊断策略中的关键一步。
临床经验判断的价值已在几大系列研究中得到证实,通常包含常规检测,比如胸片、心电图以鉴别诊断。然而,由于临床判断缺乏标准化,因此制定出一些临床可能性评估工具。最常用的是修订版Geneva评分 (见下表)和Wells评分。为了增加其应用,这两个评估工具也已被简化。
无论所用的分数如何,确诊PE患者的比例可以预计为:低度可能10%,中度可能30%,高度可能65%。当采用二级分类时,在PE可能性低的类别中,确诊PE患者有12%,在PE可能性高的类别中,大约有30%确诊为PE。
Geneva临床预测评分表

PE:肺栓塞;DVT:深静脉血栓形成。
3、避免过度使用PE的确诊检查
肺栓塞排除标准(PERC)是为急诊病人制定的,临床上,PE可能性很低的患者不需要进行PE确诊检查。PERC中8个临床表现与无PE显著相关:年龄<50岁;脉搏<100次/分;SaO2>94%;无单侧腿肿胀;无咯血;无近期外伤或手术;无VTE病史;无口服激素。
4、D-二聚体检测
急性肺栓塞时,D-二聚体水平都会升高。D-二聚体检查阴性预测价值很高,其正常时急性PE或深静脉血栓形成(DVT)的可能性很小。而D-二聚体升高的阳性预测价值很小,所以不用于PE的确诊。D-二聚体升高常见于肿瘤、严重感染或炎症、妊娠期或在院患者。所以,急诊必须检测D-二聚体来排除急性PE。
D-二聚体检测的方法有很多,临床医生需要知道自己医院相关实验的诊断效能。ELISA诊断敏感度>95%,能用于排除检测前中低可能性患者发生PE。在急诊病房,ELISA阴性的D-二聚体结果联合临床可能性评估,能排除30%疑似PE的患者且避免继续检查。
5、根据年龄校正的D-二聚体界值
针对年龄>80岁的老人,疑似肺栓塞的D-二聚体特异性随年龄增加而降低约10%。根据年龄校正的D-二聚体界值能够提高老年人D-二聚体的检测效能。
6、CTPA
多排螺旋CTPA是疑诊PE患者肺血管成像的首选方法,能充分显示肺动脉至亚段水平。对于PE临床评估低或中度的患者,CTPA阴性对PE具有较高的阴性预测值,但如果临床评估高度可能,其阴性预测值较低。相反,对于临床评估中度或高度可能的患者,CTPA阳性对PE 的阳性预测值较高,但在临床评估低度可能的患者中,其阳性预测值较低。因此,如果临床判断和CTPA结果不一致,临床医生应考虑进一步检查。
7、核素肺通气/灌注(V/Q)显像
核素肺通气/灌注(V/Q)显像是一种对疑诊PE患者的重要诊断方法。通气显像的目的是提高特异性:在急性PE中,低灌注节段(不匹配)的通气预期是正常的。V/Q显像是一种低辐射和低造影剂滞留的方法,优先应用于临床可能性低、胸片正常的门诊患者、年轻(尤其是女性)患者、孕妇、造影剂过敏史或严重肾功能不全的患者。
为便于与临床医生交流,最好采用三种分类:常规扫描除外PE、高度可能PE(大多数患者考虑诊断为PE)和非诊断性扫描。对于胸片正常的患者,可只行灌注扫描;在这种情况下,任何灌注缺损都会被认为是不匹配的。尽量避免使用非诊断性扫描的报告结果,因为这一结果表明了进一步诊断性检查的必要性。为克服这一问题,人们提出了各种各样的策略,尤其是将临床可能性纳入其中。
此外,最佳的显像技术(灌注SPECT、V/Q SPECT、非增强CT灌注SPECT、或非增强CT V/Q SPECT)仍有待确定。
8、肺动脉造影
几十年来,肺动脉造影一直是诊断或排除急性PE的金标准,但由于侵入性较低的CTPA提供了类似的诊断准确性,现在很少进行这种操作。急性PE的诊断是基于血栓的两种形式的直接证据,要么是充盈缺损,要么是肺动脉分支的截断。
肺血管造影有风险,大多数发生在血流动力学不稳定或呼吸衰竭患者。对于血流动力学不稳定的患者,应减少造影剂的用量,避免非选择性注射。
肺栓塞诊断的影像学检查
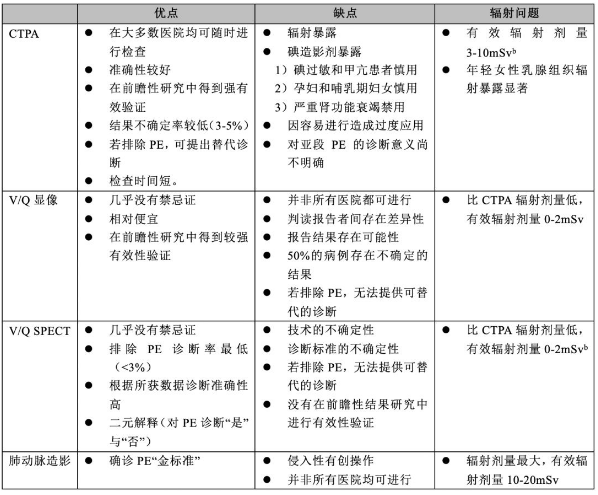
CTPA=CT肺动脉造影;mSv =毫西弗;PE=肺栓塞;SPECT=单光子发射计算机断层扫描;V/Q=核素肺通气/灌注显像
9、磁共振血管造影
磁共振肺动脉造影(MRPA)多年来一直被用来评估疑诊PE。然而,该技术灵敏度低、扫描不确定性很高,在大多数紧急情况下的可使用的价值很低,目前尚不能推广应用于临床实践。
10、超声心动图
急性PE可导致的右室压力超负荷和功能障碍,可通过超声心动图检测。其阴性结果不能排除PE。
经胸超声心动图(TTE)显示≥25%的PE患者右室扩大,可用于疾病的危险分层。即使之前已存在心肺疾病,超声心动图对PE仍有较高的阳性预测价值。因此,肺动脉射血加速时间(右室流出道切面)< 60 ms与收缩期三尖瓣峰值距离< 60毫米汞柱(60/60征)的组合,或与超声心动图的右室顶点相比,右室游离壁收缩力减低(麦康奈尔征),经常提示PE的发生。
超声心动图检查对于血流动力学稳定的疑诊PE患者不强制作为常规诊断工作的一部分。在血流动力学不稳定的疑似PE患者中,右室压力过负荷的明确征象,尤其是更加特异的超声心动图的发现 (60/60征,麦康奈尔征,或右心血栓),对于高度怀疑PE,而且临床上不能做CTPA检查,超声心动图提示无其他明显原因可以解释的右室压力过负荷,应考虑紧急溶栓治疗。
未筛选的PE患者中,<4%的患者可通过TTE或经食道超声心动图(TOE)或CTPA检测到可移动的右心血栓。右心移行血栓基本上证实了PE的诊断,并与早期高死亡率有关,尤其是在右室功能障碍患者中。
超声心动图可检测到部分疑似急性PE患者的右室壁增厚或三尖瓣功能不全射流速度超过与急性右室压力过负荷(>3.8 m/s或收缩期三尖瓣峰值距离>60 mmHg)相匹配的值。
【图3】经胸超声心动图评估右心室负荷过重参数特征

A’=组织多普勒成像显示三尖瓣环舒张晚期峰值速度;ACT=右室流出道加速时间;Ao=主动脉;E’=组织多普勒成像显示三尖瓣环舒张早期峰值速度;IVC=下腔静脉;LA=左心房;LV=左心室;RA=右心房;RiHTh=右心血栓(或血栓);RV=右心室(的);S’=组织多普勒成像显示三尖瓣环收缩期峰值速度;TAPSE=三尖瓣环收缩期位移;TRPG=三尖瓣峰值收缩梯度。
11、加压静脉超声(CUS)
PE起源于下肢DVT,极少起源于上肢DVT(多发生于静脉置管后)。现在,下肢加压超声在诊断DVT上已经基本取代了静脉造影。疑似肺栓塞的患者中发现近端DVT,这足以证明需要抗凝治疗,而无需进一步检查。如果PE患者被间接证实存在近端 DVT ,则应对肺栓塞严重程度和早期死亡风险进行风险评估。
疑诊PE时,CUS可局限于四点检查(双侧腹股沟和腘窝)。唯一证实DVT的诊断标准是静脉的不完全压缩率。近端CUS阳性对PE具有较高的阳性预测价值。对于CT禁忌证患者,CUS是一个可用的方法。与有与腿部静脉相关的症状和体征的可疑PE患者的近端CUS阳性的可能性较高。
PE诊断推荐意见

CT=计算机断层扫描;CTPA=CT肺动脉造影;CUS=加压静脉超声;DVT=深静脉血栓形成;MRA=磁共振血管造影;PE=肺栓塞;SPECT=单光子发射计算机断层扫描;UFH=普通肝素;V/Q=核素肺通气/灌注显像;VTE=静脉血栓栓塞症。
危险分层及早期死亡风险评估
1、PE严重程度的临床指标
急性右心衰竭是一种快速进展的综合征,是决定急性PE预后的关键因素。心动过速、低收缩压、呼吸功能不全、晕厥,无论单独或合并存在,均与急性PE短期预后不良有关。
2、右室大小和功能的影像学检查
① 超声心动图:RV/LV直径比≥1.0和TAPSE(三尖瓣瓣环收缩期位移)<16mm是最常被报道的与预后不良有关的参数。
超声心动图上右心功能障碍与血流动力学暂时稳定患者的短期死亡风险升高有关,但是它对PE相关死亡的总体阳性预测值较低。在临床实践中,超声心动图被认为是评估血压正常PE患者预后的重要工具。
除了右室功能障碍,超声心动图还能识别卵圆孔未闭导致的右向左分流和右心血栓的存在,两者均与PE患者死亡率升高有关。
② CTPA:CTPA四腔心切面可以检测右室扩大(横断面或者四腔心切面右室舒张末内径和RV/LV比值)作为右心功能不全的指标。
轻度右心室扩张(RV/LV略高于0.9)是一种常见的表现,可能对预后影响不大。然而,RV/LV比值升高与预后特异性提高有关,即使临床标准低风险的患者。因此,CTPA上RV/LV≥1.0(而不是0.9)可能更适合作为预后不良的指标。
除了右室大小和RV/LV比值,CT还可分析心腔容积提供预后信息,并对下腔静脉(IVC)造影剂反流进行评估。
3、实验室生物标志物
①心肌损伤标志物:入院时血浆肌钙蛋白浓度升高可能与PE急性期预后较差有关。
心脏肌钙蛋白水平升高本身对血压正常的急性PE患者的早期死亡风险有较低的特异性和阳性预测值。然而,当与临床和影像学表现结合起来时,有助于识别出升高的PE风险,进行进一步的预后分层。
心型脂肪酸结合蛋白(H-FABP)是心肌损伤的早期敏感指标,对未选择的和血压正常的急性PE患者均可提供预后信息。
②右室功能不全标志物:血浆利钠肽水平反应了急性PE患者右室功能不全和血流动力学损害的严重程度。
和肌钙蛋白相似,BNP或NT-proBNP浓度升高对血压正常的急性PE患者的早期死亡风险有较低的特异性和阳性预测值,但是低水平的BNP或NT-proBNP可排除早期的临床不良结局,具有较高的敏感性和阴性预测值。NT-proBNP>600pg/mL可能是一个合适的临界值。
4、PE严重程度的综合评价及评分
对于血流动力学稳定的PE患者来说,独立参数可能不足以确定PE严重程度及其相关风险,并对其进一步分层。因此,上述临床、影像、实验室参数的各种组合已被用于建立预后评分,从而对早期PE相关死亡风险进行(半)定量评估。
5、将进展性疾病和合并症共同纳入PE风险评估
临床、影像、实验室检查的结果与PE严重程度和PE早期死亡风险相关。除此之外,进展性疾病和合并症的基线参数对评估PE患者死亡风险和早期预后是必要的。
肺栓塞严重指数(PESI)是最广泛验证的一项临床评分其主要优势在于可靠地识别30天死亡风险较低的患者(PESI I级和II级)。鉴于原始PESI评分包括11个不同权重的变量,较为复杂,一项简化PESI评分(sPESI)已被研发和证实。和原始版本的PESI一样,sPESI能可靠识别30天死亡风险较低的患者。
合并DVT是预后不良的因素,与急性PE后3个月内的死亡风险独立相关。伴发DVT可作为PE显著合并症之一。
原始版及简化版的肺栓塞严重程度指数

b.p.m.=次/min;CI=置信区间。
6、预后评估策略
早期识别(或怀疑)高危PE患者是至关重要的。高危PE需紧急诊断并立即启动再灌注治疗,其即刻治疗决策不需要肌钙蛋白和利钠肽等实验室生物标志物的检测。
血流动力学稳定的急性PE患者建议进行进一步的危险分层。下表总结了用于区分中危和低危PE患者的临床、影像和实验室参数。PESI评分(原始或简化版本)将急性PE严重程度有关的参数和患者合并症相整合,是迄今为止验证最广泛且使用最广泛的临床评分。
肺栓塞严重程度和早期(住院或30天)死亡风险的分类

CTPA=CT肺动脉造影;PE=肺栓塞;PESI=肺栓塞严重程度指数;RV=右心室;sPESI=简化版肺栓塞严重程度指数;TTE=经胸超声心动图。
中危PE患者如有右室功能障碍(超声心动或CTPA)和心脏生物标志物升高(尤其是肌钙蛋白升高)将被归为中高危组。右室功能正常(超声心动或CTPA)或者心肌生物标志物正常的中危患者被归入中低危组。
7、预后评估的推荐意见

PE=肺栓塞;PESI=肺栓塞严重程度指数;RV=右心室;sPESI=简化版肺栓塞严重程度指数。
二、2018年《中国肺血栓栓塞症诊治和预防指南》
诊断
急性肺血栓栓塞症(PTE)的临床表现缺乏特异性,容易被漏诊和误诊。应根据临床可能性评估结果对疑诊患者进行检查,一旦确诊PTE,应进一步探寻潜在的其他危险因素。
1、临床表现
急性PTE临床表现多种多样,缺乏特异性,易被忽视或误诊,其严重程度亦有很大差别,从轻者无症状到重者出现血流动力学不稳定,甚或猝死。PTE的诊断中,要注意是否存在DVT,特别是下肢DVT。
2、实验室及其他检查
(一)疑诊相关检查
1、血浆D-二聚体:D-二聚体分子量的异质性很大,基于不同原理的试验方法对D-二聚体检测的敏感性差异显著。因此,临床医师应了解本医疗机构所使用D-二聚体检测方法的诊断效能。D-二聚体对急性PTE的诊断敏感度在92%~100%,对于低度或中度临床可能性患者具有较高的阴性预测价值,若D-二聚体含量<500 μg/L,可基本排除急性PTE。恶性肿瘤、炎症、出血、创伤、手术和坏死等情况可引起血浆D-二聚体水平升高,因此D-二聚体对于诊断PTE的阳性预测价值较低,不能用于确诊。
D-二聚体的诊断特异性随着年龄的升高而逐渐下降,以年龄调整临界值可以提高D-二聚体对老年患者的诊断特异性。证据显示,随年龄调整的D-二聚体临界值[>50岁患者为年龄(岁)×10 μg/L]可使特异度增加到34%~46%,敏感度>97%。
2、动脉血气分析:急性PTE常表现为低氧血症、低碳酸血症和肺泡-动脉血氧分压差[P(A-a)O2]增大。但部分患者的结果可正常。
3、血浆肌钙蛋白:肌钙蛋白I(cTNI)及肌钙蛋白T(cTNT)是评价心肌损伤的指标。急性PTE并发右心功能不全(RVD)可引起肌钙蛋白升高,水平越高,提示心肌损伤程度越严重。
4、脑钠肽(BNP)和N-末端脑钠肽前体(NT-proBNP):血BNP和NT-proBNP水平升高水平可反映RVD及血流动力学紊乱的严重程度,无明确心脏基础疾病患者如果BNP或NT-proBNP增高,需考虑PTE的可能;同时该指标也可用于评估急性PTE的预后。
5、心电图:大多数病例表现有非特异性的心电图异常。较为多见的表现包括V1~V4的T波改变和ST段异常;部分病例可出现SⅠQⅢTⅢ征;其他心电图改变包括完全或不完全右束支传导阻滞;肺型P波;电轴右偏,顺钟向转位等。观察到心电图的动态改变较之静态异常对于提示PTE具有更大意义。心电图表现有助于预测急性PTE不良预后。
6、胸片:表现缺乏特异性,仅凭胸片不能确诊或排除PTE。
7、超声心动图:超声心动图在提示PTE诊断和排除其他心血管疾患方面有重要价值。超声心动图检查可发现右心室后负荷过重的征象,包括出现右心室扩大、右心室游离壁运动减低,室间隔平直,三尖瓣收缩期反流峰值压差>30mmHg(1 mmHg=0.133 kPa)、下腔静脉扩张吸气塌陷率减低等。少数患者中,若超声发现右心系统血栓,同时临床表现符合PTE,即可诊断。超声心动图检查可床旁进行,在血流动力学不稳定的疑似PTE中有诊断及排除诊断的价值。
(二)确诊相关影像学检查
1、CTPA:CTPA可直观地显示肺动脉内血栓形态、部位及血管堵塞程度,对PTE诊断的敏感性和特异性均较高,且无创、便捷,目前已成为确诊的首选检查方法。其直接征象为肺动脉内充盈缺损。CTPA可同时显示肺及肺外的其他胸部病变,具有重要的诊断和鉴别诊断价值。
2、V/Q显像:V/Q显像是PTE重要的诊断方法。典型征象是呈肺段分布的肺灌注缺损,并与通气显像不匹配。但是由于许多疾病可以同时影响患者的肺通气和血流状况,致使V/Q显像在结果判定上较为复杂,需密切结合临床进行判读。
V/Q平面显像结果分为3类:(1)高度可能(2)正常;(3)非诊断性异常。V/Q断层显像(SPECT)发现1个或1个以上肺段V/Q不匹配即为阳性;SPECT检查很少出现非诊断性异常;如果SPECT阴性可基本除外肺栓塞。
V/Q显像辐射剂量低,较少引起过敏反应。因此可优先应用于临床可能性低的门诊患者、年轻患者(尤其是女性)、妊娠、对造影剂过敏、严重的肾功能不全等。
如果患者胸部X线片正常,可以仅行肺灌注显像。
3、MRPA:MRPA可以直接显示肺动脉内的栓子及PTE所致的低灌注区,从而确诊PTE,但对肺段以下水平的PTE诊断价值有限。MRPA无X线辐射,不使用含碘造影剂,可以任意方位成像,但对仪器和技术要求高,检查时间长。肾功能严重受损、对碘造影剂过敏或妊娠患者可考虑选择MRPA。
4、肺动脉造影:选择性肺动脉造影为PTE诊断的「金标准」。其敏感度约为98%,特异度为95%~98%。PTE的直接征象有肺血管内造影剂充盈缺损,伴或不伴轨道征;如缺乏PTE的直接征象,则不能诊断PTE。肺动脉造影是一种有创性检查,随着CTPA的发展和完善,肺动脉造影已很少用于急性PTE的临床诊断,应严格掌握适应证。
(三)DVT相关影像学检查
1、CUS:CUS通过直接观察血栓、探头压迫观察或挤压远侧肢体试验和多普勒血流探测等技术,可以发现95%以上的近端下肢静脉内的血栓。静脉不能被压陷或静脉腔内无血流信号为DVT的特定征象和诊断依据。对腓静脉和无症状的下肢DVT,其检查阳性率较低。CUS具有无创及可重复的特性,基本已取代静脉造影成为DVT首选的诊断技术。
2、CTV:CTV可显示静脉内充盈缺损,部分或完全包围在不透光的血流之间,或呈完全充盈缺损。CTPA联合CTV可同时完成,仅需1次静脉注射造影剂,为PTE及DVT的诊断,尤其是盆腔及髂静脉血栓的诊断提供依据,且可以提高CT对PTE诊断的敏感性,但同时进行两项检查的放射剂量明显增多,需要权衡利弊。
(四)求因相关检查
对于确诊的PTE患者应进行求因相关检查,对于疑似遗传缺陷患者,应先做病史和家族史的初筛,主要评估指标包括(但不限于):血栓发生年龄<50岁、少见的栓塞部位、特发性VTE、妊娠相关VTE、口服避孕药相关VTE以及华法林治疗相关的血栓栓塞等;家族史包括(但不限于):≥2个父系或母系的家族成员发生有(无)诱因的VTE。
1、抗凝蛋白:抗凝血酶是凝血酶(FⅡa)的主要抑制物,此外还可中和其他多种活化的凝血因子(如FⅨa、Ⅹa、Ⅺa和Ⅻa等);蛋白C系统主要灭活FⅤa和FⅧa,蛋白S是蛋白C的辅因子,可加速活化的蛋白C对FⅤa和FⅧa的灭活作用;抗凝蛋白缺陷患者易在合并其他风险因素或无明显诱因的情况下发生VTE。抗凝药物可干扰抗凝蛋白检测的结果。因此,建议在使用普通肝素(UFH)、低分子量肝素(LMWH)、磺达肝癸钠及维生素K拮抗剂(VKAs)期间不应测定抗凝蛋白,其中抗凝血酶活性检测需在停用肝素类药物至少24 h 后进行;蛋白C 和蛋白S活性检测在停VKAs至少2~4周后进行,并通过检测凝血酶原时间或国际标准化比值(INR)以评估患者VKAs停药后的残留抗凝效果。
2、抗磷脂综合征相关检测:实验室检查包括狼疮抗凝物、抗心磷脂抗体和抗β2糖蛋白1抗体。临床上需要对以下患者进行抗磷脂综合征相关检测:<50岁的无明显诱因的VTE和无法解释的动脉血栓栓塞、少见部位发生血栓形成、习惯性流产、血栓形成或病理妊娠合并自身免疫性疾病,部分患者可见活化部分凝血活酶时间(APTT)延长。如果初次狼疮抗凝物、抗心磷脂抗体和β2糖蛋白1抗体检测阳性,建议3个月之后再次复查。
3、易栓症相关基因检测:基因检测尚存争议,近年来针对相关基因外显子潜在突变位点的检测,也需建立在遗传背景调查和蛋白缺陷表型检测的基础上,作为辅助依据。
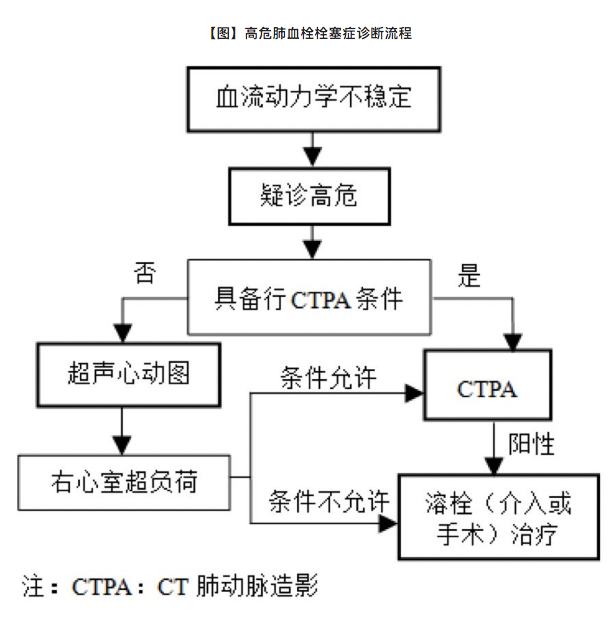
3、危险分层综合评估
血流动力学不稳定的PTE为高危;血流动力学稳定的PTE,可根据是否合并RVD和心脏生物学标志物异常将PTE患者分为中危和低危。
高危PTE:以休克和低血压为主要表现,即体循环收缩压<90mmHg,或较基础值下降幅度≥40mmHg,持续15min以上。须除外新发生的心律失常、低血容量或感染中毒症所致的血压下降。
中危PTE:血流动力学稳定,但存在RVD的影像学证据和或心脏生物学标志物升高为中危组。根据病情的严重程度,可以将中危PTE进行再分层。中高危:RVD和心脏生物学标志物升高同时存在。中低危:单纯存在RVD或心脏生物学标志物升高。
RVD的诊断标准:影像学证据包括超声心动图或CT提示RVD,超声检查符合下述其中2项指标:(1)右心室扩张(右心室舒张末期内径/左心室舒张末期内径>1.0或0.9);(2)右心室前壁运动幅度减低(<5mm);(3)吸气时下腔静脉不萎陷;(4)三尖瓣反流速度增快,估测三尖瓣反流压差>30mmHg。CTPA检查符合以下条件:四腔心层面发现的右心室扩张(右心室舒张末期内径/左心室舒张末期内径>1.0或0.9)。心脏生物学标志物包括BNP、NT-proBNP、肌钙蛋白。其升高与PTE短期预后显著相关。
低危PTE:血流动力学稳定,不存在RVD和心脏生物学标志物升高的PTE。
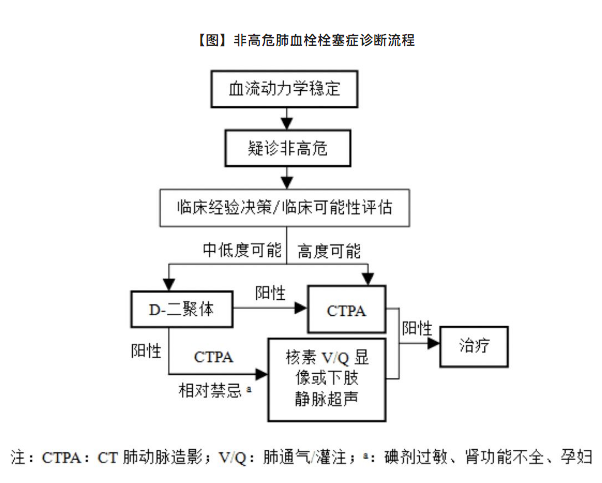
4、诊断策略
临床可能性评估可以提高疑诊PTE的准确性。目前已经研发出多种明确的临床预测评分,最常用的包括简化Wells评分、修订版Geneva评分量表等(见下表)。
【表】PTE临床可能性评分表

要点对比
相同点对比

不同点对比

参考文献
[1] Stein, P. D. et al. Multidetector computed tomography for acute pulmonary embolism. The New England journal of medicine354, 2317-2327, doi:10.1056/NEJMoa052367 (2006).
[2] Anderson, D. R. et al. Computed tomographic pulmonary angiography vs ventilation-perfusion lung scanning in patients with suspected pulmonary embolism: a randomized controlled trial. Jama298, 2743-2753, doi:10.1001/jama.298.23.2743 (2007).
[3] Douma, R. A. et al. Performance of 4 clinical decision rules in the diagnostic management of acute pulmonary embolism: a prospective cohort study. Annals of internal medicine154, 709-718, doi:10.7326/0003-4819-154-11-201106070-00002 (2011).
[4] Barco, S. et al. Prognostic value of right ventricular dysfunction or elevated cardiac biomarkers in patients with low-risk pulmonary embolism: a systematic review and meta-analysis. European heart journal40, 902-910, doi:10.1093/eurheartj/ehy873 (2019).
[5] Kurnicka, K. et al. Echocardiographic Pattern of Acute Pulmonary Embolism: Analysis of 511 Consecutive Patients. Journal of the American Society of Echocardiography : official publication of the American Society of Echocardiography29, 907-913, doi:10.1016/j.echo.2016.05.016 (2016).
[6] 中华医学会呼吸病学分会肺栓塞与肺血管病学组, 中国医师协会呼吸医师分会肺栓塞与肺血管病工作委员会&全国肺栓塞与肺血管病防治协作组. 肺血栓栓塞症诊治与预防指南. 中华医学杂志98, 1060-1087, doi:10.3760/cma.j.issn.0376-2491.2018.14.007 (2018).
[7] 韩婧, 张帅&万钧. 2018版中国《肺血栓栓塞症诊治与预防指南》解读之二:诊断策略. 中国实用内科杂志38, 926-930, doi:10.19538/j.nk2018100111 (2018).
本文完
编辑:Jerry
编译人员:韩婧、杨宏伟、王瑶、席霖枫;审校:谢万木、翟振国
本文转载自公众号「中日肺血管病多学科会诊平台」
原链接:传承、更新与交融:2019版ESC 《急性肺栓塞诊断和治疗指南》与 2018版CTS《肺血栓栓塞症诊治和预防指南》的精萃解读之二



