
骨髓增生异常综合征(MDS)是一组起源于造血干细胞的疾病,主要特征为骨髓造血功能异常、血细胞发育异常,表现为难治性的血细胞减少、造血功能衰竭,并且高风险向急性白血病转化,曾被称为白血病前期。新型隐球菌肺炎(CNP)是由新型隐球菌感染引起的亚急性或慢性肺部真菌性疾病,近年来发病率逐渐升高[1],起病隐匿,临床表现无明显特异性[2],可引起脑膜炎、肺炎等。本文报道1例骨髓增生异常综合征继发CNP病例,通过对患者的临床症状、实验室检查,诊疗过程等进行分析,旨在为临床诊治CNP提供参考。
一、案例经过
基本信息:男,80岁,因“骨髓增生异常综合征,咳嗽、咳痰2天”于2022.9.12收入我院血液内科。
主诉:乏力、纳差8月余,咳嗽、咳痰2天。
现病史:8月前无明显诱因出现乏力、纳差、消瘦,无发热,无腹痛、腹泻、腹账,无咳嗽、咳痰、胸闷,遂至河南省人民医院,行骨穿、骨髓活检、基因、染色体等相关检查诊断为骨髓增生异常综合征,未治疗,定期观察。期间查PET-CT提示:1.右侧锁骨上、纵隔及双肺门、肠系膜根部及右下腹肠系膜淋巴结多发轻中度肿大;后行淋巴结活检提示:肉芽肿性炎伴坏死,考虑结核性;给予“异烟肼、乙胺丁醇、吡嗪酰胺、左氧氟沙星”联合抗结核治疗。患者定期复查血常规,血红蛋白呈缓慢下降趋势。4月前患者乏力症状加重,在河南省胸科医院给予输注红细胞支持治疗。3月前患者抗结核治疗方案更换为“异烟肼,乙胺丁醇、左氧氟沙星”。2月前乏力再次加重来我院,给予“司坦唑醇、强的松,促红素〞方案治疗。后患者外院用药,间断复查血常规,血红蛋白逐渐上升。2天前无明显诱因出现咳嗽、咳痰,无发热,夜间症状加重,为进一步诊治来院。患者本次发病以来,神志清,精神可,饮食、睡眠不佳,大、小便正常,体力差,近半年体重较前减轻10kg。
既往史:高血压病15年余,目前口服苯磺酸氨氯地平片。冠心病12年余,目前口服瑞舒伐他汀钙片治疗。10年前因“胆囊息肉”行“胆囊切除术”。
体格检查:T:36.5℃,P:92次/分,R:21次/分,BP:128/68mmHg。正常面容,皮肤黏膜未见出血点、黄染及皮疹,浅表淋巴结未触及,胸骨无压痛,左肺听诊呼吸音减弱,可闻及湿性啰音。腹软,无压痛、反跳痛,肝脾肋下未触及,双下肢无水肿。
实验室检查:入院查WBC:5.47×109/L,N% 75.3, RBC:2.56×1012/L,HB:85 g/L;CRP:153mg/L;ALB:31.3 g/L;ALT:33.7U/L;AST:43.5U/L;BUN:6.97mmol/L;Cr:63umol/L。
影像学检查:入院后查胸部CT提示1、左肺炎症;右肺纤维灶;2、纵隔内增大淋巴结;3、主动脉及冠状动脉硬化;4.左侧胸腔积液。(见图1-1,1-2)。
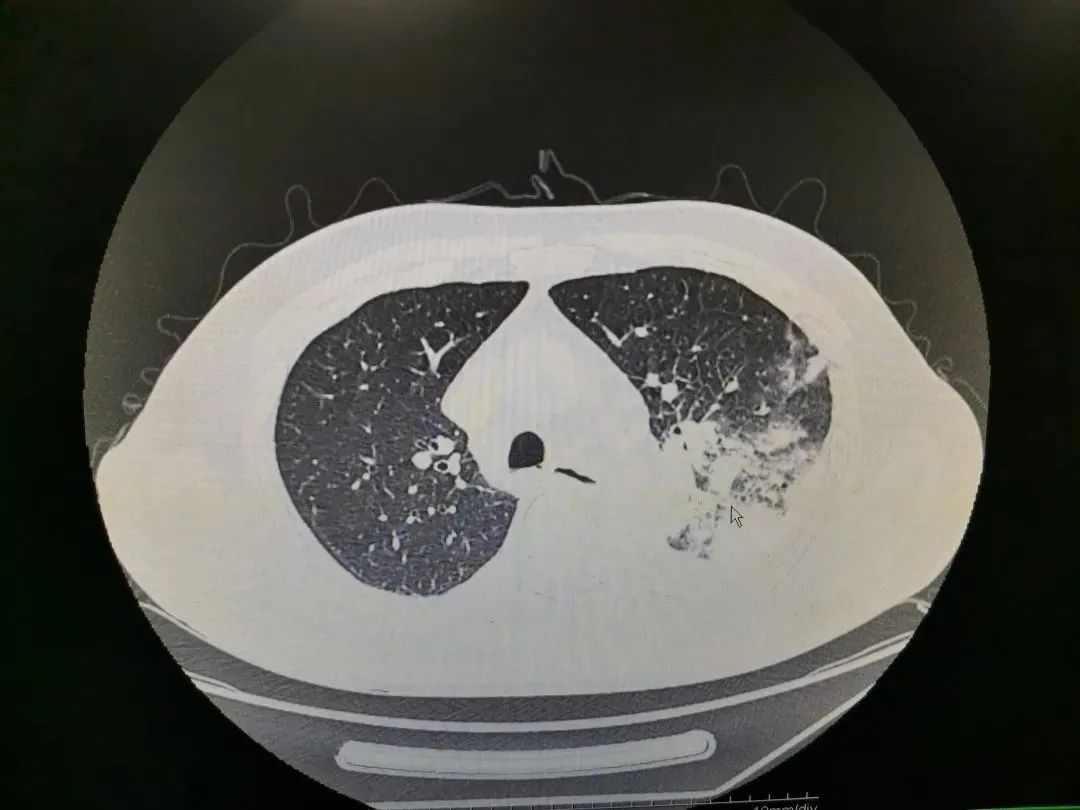
图1-1
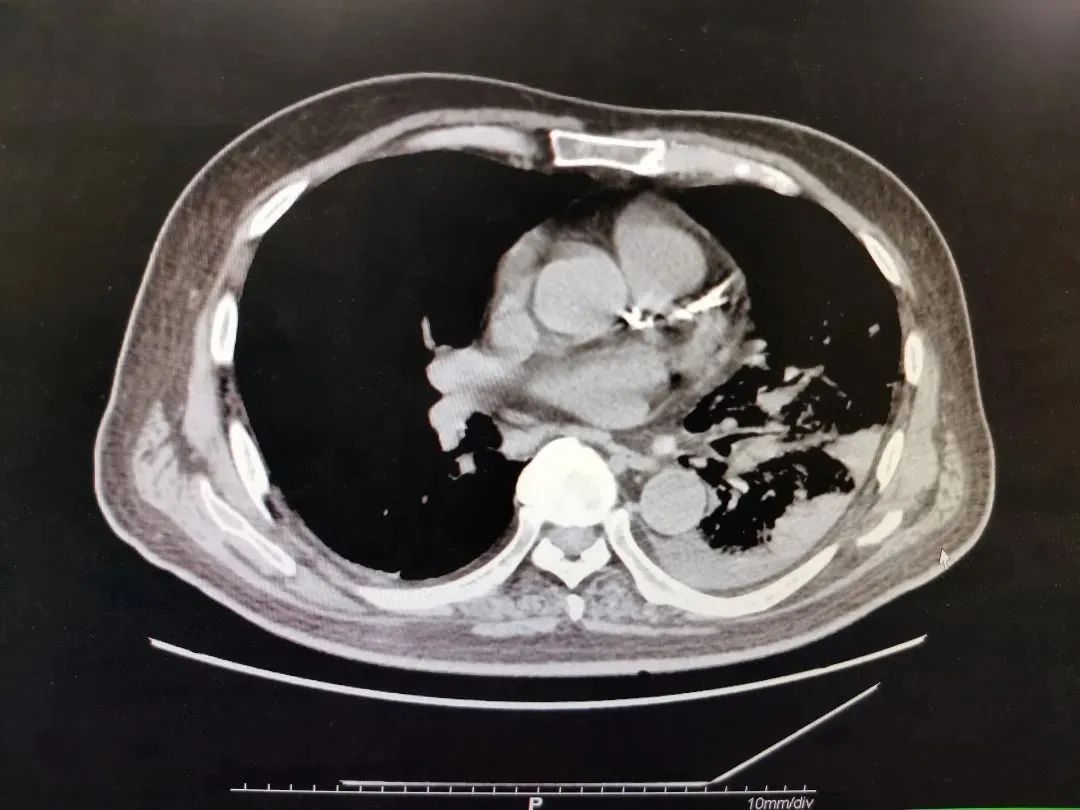
图1-2
入院诊断
1.骨髓增生异常综合征;2.肺部感染;3.结核性淋巴结炎;4.冠状动脉粥样硬化性心脏病;5.高血压病2级;6.胆囊切除术后。
进一步诊治和检查:
2022.9.12结合患者临床表现、实验室检查及胸部影像学,继续给予“异烟肼,乙胺丁醇、左氧氟沙星”抗结核治疗,同时给予“司坦唑醇、强的松、促红素”等对症治疗。
2022.9.13结合患者临床表现、体征、胸部影像学及近期治疗情况,目前考虑肺部感染可能性大。遂请呼吸内科会诊,建议送检痰培养、血培养等检查,行支气管镜检查明确病原体,但患者家属拒绝。后考虑患者年龄偏大、近期一直应用激素,免疫力差,经验性给予美罗培南(1g q8h)抗感染,同时止咳化痰平喘等对症治疗。
2022.9.15患者再次发热,体温最高38.3℃,咳嗽、咳痰。痰细菌、真菌、抗酸杆菌涂片及培养均阴性,经验性抗感染后未见好转,不排除合并革兰阳性球菌感染可能,遂加用利奈唑胺(0.5g q12h)联合抗感染。因患者痰液增多,多次与患者家属沟通后同意行支气管镜检查。
2022.9.17患者无发热,咳嗽、咳痰较前有好转。查血常规:WBC:2. 11×109/L,RBC:2.96×1012/L,HB:89 g/ L,PLT:169×109/L,CRP:92.8mg/ L,ALB:28.1 g/L。
行支气管镜检查取肺泡灌洗液送检涂片、培养、呼吸道病原体靶向测序(tNGS),血清隐球菌抗原等检查。9.18 tNGS结果回报:新生隐球菌,9171序列(见图2-1);血清隐球菌荚膜多糖抗原:阳性(见图2-2)。结合患者情况,给予氟康唑400mg qd治疗,治疗期间注意不良反应。
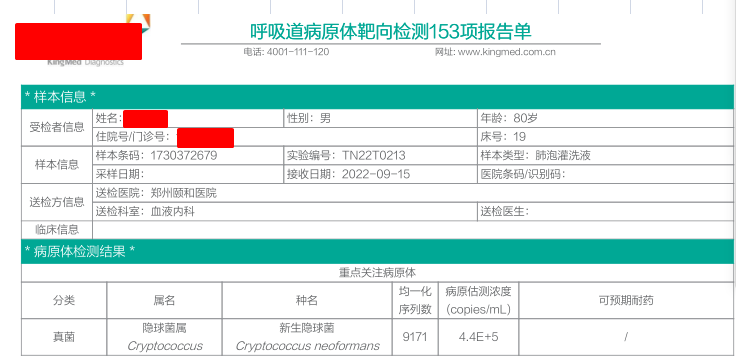
图2-1 肺泡灌洗液tNGS结果
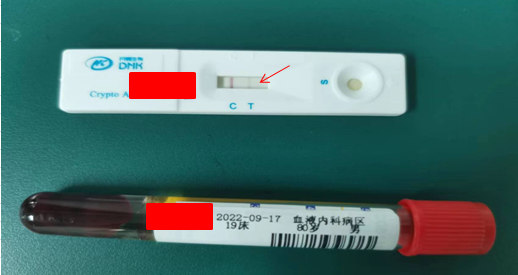
图2-2 血清隐球菌荚膜多糖抗原试验结果
2022.9.20患者仍发热,伴畏寒,咳嗽、咳黄痰,肺部可闻及痰鸣音,肺部症状改善不明显,考虑加用两性霉素B(80mg qd)联合抗感染。另患者查CRP:76.52mg/L,较前下降,停用美罗培南和利奈唑胺,降级为莫西沙星(0.4g qd)继续抗感染治疗。
2022.9.28患者近一周体温正常,咳嗽,咳痰、乏力等较前明显好转,坚持要求出院。考虑隐球菌抗感染疗程长,嘱院外继续口服药物序贯治疗,定期复查血常规、肝功能、电解质及肺部影像学等检查,不适随诊。
2022.11.26患者再次入院,诉乏力、纳差,夜间咳嗽、咳痰且粘稠不易咳出,较前有所加重。入院后查实验室检查提示轻度贫血,重度低钾,考虑患者乏力、纳差原因与低钾血症有关;产生低钾原因与应用两性霉素B有关,停用并给予补钾治疗;咳嗽,咳痰考虑可能与隐球菌肺炎复发有关,继续给予氟康唑(400mg qd)抗真菌治疗,给予止咳化痰雾化等对症治疗。联系呼吸科行支气管镜下肺泡灌洗、吸痰术,给予两性霉素B局部用药,肺泡灌洗液送检涂片、培养及tNGS等。后结果回报:新生隐球菌,2709序列(见图3-1),培养回报:新型隐球菌(见图3-2)。继续给予氟康唑(400mg qd)治疗,定期复查血常规、肝功能等检查。
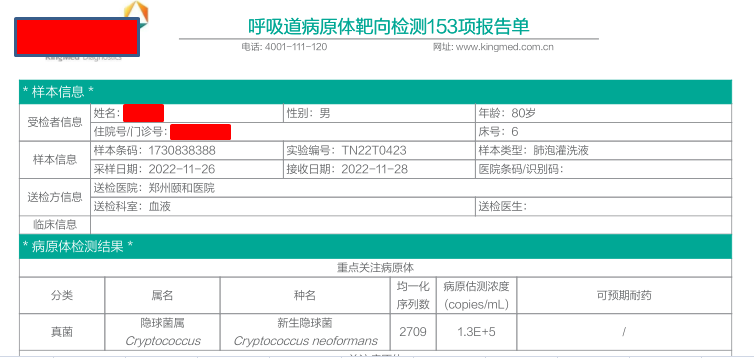
图3-1肺泡灌洗液TNGS结果

图3-2肺泡灌洗液真菌培养结果
2023.10.3患者以“乏力、纳差24月余,加重伴胸闷、咳嗽1天”为主诉再次入院。2023.10.4查血清隐球菌荚膜多糖抗原:阴性(见图4-1)。患者胸闷、咳嗽症状好转,结合患者氟康唑治疗应用时间已达1年余,将氟康唑减量(150mg qd),密切观察临床表现。

图4-1 血清隐球菌荚膜多糖抗原结果
最后诊断
1.骨髓增生异常综合征;2.隐球菌肺炎;3.结核性淋巴结炎;4.低蛋白血症;5.低钾血症;6.冠状动脉粥样硬化性心脏病;7.高血压病2级;8.胆囊切除术后。
二、案例分析
患者老年男性,咳嗽、咳痰,无明显诱因出现乏力、纳差,消瘦,无发热,无腹痛、腹泻,无胸闷,外院诊断骨髓增生异常综合征,未治疗。后患者乏力症状加重,外院行淋巴结活检提示:肉芽肿性炎伴坏死,考虑结核性,给予“异烟肼,乙胺丁醇、左氧氟沙星”抗结核治疗;给予“司坦唑醇、强的松、促红素”方案等对症治疗。后患者无明显诱因出现咳嗽、咳痰,持续发热,肺泡灌洗液tNGS和血清隐球菌荚膜抗原测定均提示新型隐球菌。经问诊患者在本次发病前吃过鸽子肉,考虑为可能的病原菌接触史。先后给予氟康唑,两性霉素B治疗,因两性霉素B致低钾血症等不良反应停用,后继续给予氟康唑治疗。因患者院外未严格规范治疗,后病情反复,间断住院,抗真菌治疗1年后,复查血清隐球菌荚膜多糖抗原为阴性,治疗有效。
三、知识拓展
新型隐球菌是一种有荚膜包绕的酵母菌,广泛存在于土壤等自然界中,属半知菌亚门,芽孢菌纲,隐球酵母目,隐球酵母科,隐球菌属,一般为条件致病菌。新型隐球菌根据细胞表面多糖成分和生化反应的差异,可分为3个变种,新型隐球菌新生变种,格特变种和格鲁比变种;能引起人类致病的主要是新型隐球菌和格特隐球菌。此外可引起人类疾病的还有浅黄隐球菌、浅白隐球菌和罗伦隐球菌等[3-6]。新型隐球菌按血清学分类主要可分为A、B、C、D及AD5型,国内肺隐球菌病以A型最多见。目前鸽粪被认为是最重要的传染源,此外马、奶牛 、狗、猫、山羚羊、猪等也被报道曾分离出本菌[7]。
新型隐球菌广泛分布于世界各地,几乎所有艾滋病患者并发隐球菌感染均由新生变种引起;格特变种主要分布于热带、亚热带地区,但少见艾滋病伴发的隐球菌病是由该变种引起。新型隐球菌属外源性感染,经呼吸道侵入机体,血行播散时可侵犯所有的脏器组织,主要侵犯肺、脑及脑膜,以侵犯中枢神经系统最常见,约占隐球菌感染的80%[8],也可侵犯皮肤、骨和关节。新型隐球菌感染好发于细胞免疫功能低下者,如AIDS、白血病、恶性肿瘤、糖尿病、器官移植及大剂量使用糖皮质激素等患者。
新型隐球菌的实验室诊断主要有形态学检查、培养、血清学及分子生物学检测等。形态学检查包含墨汁染色、氢氧化钾压片及荧光染色等,此类方法是诊断隐球菌病最简单、快速的方法,但阳性率较低且对技术人员的要求较高。培养为诊断隐球菌病的金标准,但耗时较长,尤其对痰液等有菌部位标本,不易识别,漏检可能性较大。血清学检测操作简便,检测速度快,灵敏性和特异性较高,对隐球菌病的诊断、预后等均有一定临床价值,目前已成为实验室诊断的主要方法之一。病原微生物宏基因组二代测序技术(mNGS)近些年在临床应用越来越广泛,尤其对疑难少见病原体的快速诊断,但该技术对隐球菌、结核分枝杆菌等厚壁病原体的检出率不高,且价格昂贵,目前不易在临床上推广。
非侵袭性隐球菌病首选氟康唑治疗,重症播散性感染推荐应用两性霉素B脂质体联合5-氟胞嘧啶强化治疗,巩固期选用氟康唑治疗[9]。伏立康唑和泊沙康唑用于补救治疗,而棘白菌素类(阿尼芬净、卡泊芬净和米卡芬净)对隐球菌没有体内活性。持续感染及复发者,推荐测定最初分离菌株和复发菌株的MIC。另外,如果菌株对氟康唑的MIC≥16mg/L或氟胞嘧啶≥32 mg/L,要考虑耐药更换药物[10]。
四、案例总结
本病例为1例MDS继发隐球菌肺炎,诊断明确。CNP的临床表现多变,可无明显临床症状,也可表现为急性肺部感染,如发热、胸痛、咳嗽、咳痰等。本病例原发病为骨髓增生异常综合征,长期应用糖皮质激素,为新型隐球菌感染的高危患者。CNP往往进展较快,且治疗周期长,如治疗不及时或疗程不规范预后较差。因此如何尽早为临床提供相关病原学依据是微生物实验室亟待解决的问题。尽管mNGS等新技术具有高灵敏度和准确性,在疑难、少见病原体诊断中具很大优势,但其检测成本较高,目前仍缺乏标准化流程和详尽的解释指南。本病例中隐球菌荚膜抗原等血清学检测以其快速、高灵敏性和特异性在疾病中显现出一定优势,只有传统病原学、血清学检测及mNGS等手段相互结合,相互补充,恰到好处的应用,才能更好的助力临床。
参考文献
[1]Fang W,Fa ZZ,Liao WQ. Epidemiology of cryptococcus and cryptococcosis in China[J]. Fungal Genet Biol,2015,78(1):7-15.
[2]蒙冲. 不同免疫状态下肺隐球菌感染[J]. 中国老年学杂志,2014,34(15):4323-4.
[3]王辉,任健康,王明贵.临床微生物学检验[M].北京:人民卫生出版社,2014.
[4]倪语星,尚红. 临床微生物学检验[M].第5版.北京:人民卫生出版社,2012.
[5]王端礼.医学真菌学:实验室检验指南[M].北京:人民卫生出版社,2004.
[6]陈东科,孙长贵.实用临床微生物学检验与图谱[M].北京:人民卫生出版社,2011.
[7] 赖国祥,张玉华,林庆安等.国内2002年肺隐球菌病回顾分析[J].中国实用内科杂志,2005,25(2):176-178.
[8]范琳,肖和平.60例肺隐球菌病的诊断分析[J].传染病信息,2008,2(4):248-250.
[9] Perfect JR, Dismukes WE, Dromer F, et al. Clinical practice guidelines for the management of cryptococcal disease:2010 update by the infectious diseases society of america[J]. Clin Infect Dis, 2010, 50(3): 291-322.
[10]《侵袭性真菌病真菌学检查指南》.中华医学会微生物学和免疫学分会微生物学组.中华检验医学杂志,June 2023, Vol. 46, No. 6:11-27.
作者简介

崔靖
副主任技师,毕业于郑州大学。曾进修于河南省人民医院微生物实验室,河南省人民医院生殖中心实验室。河南省微生物学会临床微生物专业委员会委员。发表学术论文5篇。

秦辉
硕士 主管检验师 河南大学附属郑州颐和医院 临床微生物组长 主要研究方向:耐碳青霉烯类药物肠杆菌科细菌(CRE)耐药机制研究。
作者:崔靖1,秦辉2,冯婵婵3,武婉君4,陈派强5;单位:河南大学附属郑州颐和医院 医学检验科;审校:单斌(昆明医科大学第一附属医院)
本文转载自订阅号「京港感染论坛」
* 文章仅供医疗卫生相关从业者阅读参考
本文完
责编:Jerry



