引言
患者是一位中年女性,因急性脑梗死接受治疗,却意外开启了另一场更为凶险的病程。一枚用于“根治”的卵圆孔封堵器,反而成为进行性呼吸困难的序幕。从脑到心、从肺到血,如何从一团乱麻的线索中锁定隐匿的“肺部杀手”,并顺藤摸瓜揪出导致全身多发性血栓的“幕后真凶”?我们在鉴别诊断本案例的同时,发现了一个临床中极易被忽视的细节,就是治疗药物本身,来看看它是如何悄然加重了患者的危局。
卵圆孔封堵术后胸闷,陷入连锁“谜局”……多系统病变的“一元论”诊断探索
卷宗1
基本资料:女性患者,47岁,主诉“活动后胸闷1年,加重3天”,于2024年10月30日就诊于郑州大学第一附属医院心外科,11月5日转入呼吸与危重症医学五科(河南省肺栓塞与肺动脉高压诊疗中心)。
讲述者:李鹏飞
首先,病人是一名中年女性,急性脑梗死就诊发现房间隔缺损、三尖瓣重度关闭不全、肺动脉高压,卵圆孔封堵术后胸闷却进行性加重。该患者在1年前,也就是2023年11月突发右上肢活动受限,至当地市医院就诊,诊断急性脑梗死,行急诊“经皮颅内动脉取栓术”后肢体功能障碍症状消失。住院期间行心脏超声检查发现:1.右心增大 2.三尖瓣重度反流 3.肺动脉高压(约72mmHg) 4.中央型房间隔缺损(卵圆孔型) 5.左室舒张功能减退,行“经皮卵圆孔封堵术”,口服抗凝、降脂药物出院。术后出现胸闷,呈进行性加重,平路行走稍多即会出现呼吸困难,休息数分钟可缓解,无咳嗽、咳痰、咯血、胸痛、心悸、恶心、纳差、多汗等不适。
半年前,2024年3月,呼吸困难加重,伴右上肢疼痛,当地医院心外科就诊,彩超提示右上肢静脉血栓形成、肺动脉收缩压升高,给予“利伐沙班”抗凝、强心、利尿等处理后,患者症状稍有好转后出院。
2月余前,2024年8月,患者呼吸困难再次加重,仅能满足下床等简单日常活动,伴间断双下肢水肿,至我院心外科就诊,行右心导管检查示mPAP 53/17(31) mmHg,PAWP 4mmHg,SvO2 55%,给予“安立生坦+他达拉非”降肺动脉压、利尿、抗凝治疗,患者自觉呼吸困难症状稍改善。入院3天前,无明显诱因出现胸闷加重,不能平卧,坐起可缓解,伴乏力、纳差、双下肢水肿,无胸痛、头晕、头痛等其他特殊不适,于我院心外科就诊,予以“曲前列尼尔+安立生坦+他达拉非”降肺动脉压,“左西孟旦”改善右心衰,利尿、抗凝、降脂治疗后症状无明显缓解,转入我中心进一步诊治。
回顾病史,2023年11月26日,患者曾因急性脑梗死于当地市医院行“脑血管造影术+经皮颅内动脉取栓术”,术后未遗留肢体活动障碍。2023年12月12日于当地市医院院行“经皮卵圆孔封堵术”。否认高血压病史,否认糖尿病病史,否认肝炎、结核、疟疾病史,否认外伤、输血史,无食物、药物过敏史,预防接种史随社会计划免疫接种。病人适龄结婚,月经周期规则,月经量中等;孕1产1,无自然流产史。个人史、家族史无特殊。体格检查、实验室及影像检查等请见第二份卷宗:
卷宗2
体格检查:体温36.6℃,脉搏87次/分,呼吸28次/分,血压86/55mmHg,身高155cm,体重61.0Kg 。贫血貌,听诊P2>A2,双肺呼吸音清,未闻及干湿性啰音,双下肢轻度指陷性水肿。
实验室检查:
血常规:WBC 4.74×10^9/L,RBC 2.69×10^12/L,Hb 52↓g/L,PLT 165 ×10^9/L,MCV 68.5↓fL,MCH 19.3↓pg,MCHC 283↓g/L。
NT-proBNP:327↑pg/mL。
血气(Fi O2 21%) pH 7.51↑,PO2 25↓mmHg,PCO2 53↓mmHg。
血凝:PT 13.4s,INR 1.23↑,APTT 30.8s,Fib 2.61g/L,TT 17.1s,D-dimer 0.28mg/L。
铁三项:血清铁 43.95↑μmol/L,铁蛋白、不饱和铁结合力、总铁结合力未见异常。
叶酸: 5.04↓ng/mL,维生素B12:156↓pg/mL。
电解质、肝肾功能、血脂、甲功三项、心肌酶、肌钙蛋白、糖化血红蛋白、血沉、炎症3项、传染病四项、尿粪常规均未见明显异常。
影像学检查:心电图(图1):II、III、aVF、V1-V6导联T波低平或倒置;QTc延长(467 ms)。心脏彩超(图2):封堵器位置正常,房水平无分流;三尖瓣轻-中度关闭不全;肺动脉高压(估测sPAP 85mmHg,mPAP 26mmHg),左房增大,右房高值;EF 63%。双下肢静脉超声:双侧下肢深静脉功能不全。甲状腺、肝胆脾胰、泌尿系超声未见明显异常。CT肺动脉造影(CTPA)报告(图3、图4):双肺少许淡薄絮状影,炎性或肺水肿待排?双肺散在小结节,请结合临床。经皮卵圆孔封堵术后改变,请结合临床评估。左侧胸腔积液。
图1 2024.10.30 心电图
图2 2024.10.31 心脏超声
思考题:患者存在呼吸衰竭、肺动脉高压、三尖瓣关闭不全、卵圆孔未闭、脑动脉血栓、上肢静脉血栓、贫血等多系统病变,一元论能否解释?如何确定诊断方向?
按照CTEPH诊断流程,进一步完善肺灌注显像……以影像为切入点,通过血栓求因,快速突破诊断谜团
讲述者:王羽
患者为中年女性,进行性呼吸困难1年,初步检查结果提示I型呼吸衰竭、肺动脉高压、三尖瓣关闭不全、动静脉血栓、贫血,根据上述诊断线索,可以从呼吸衰竭病因、肺动脉高压分类、瓣膜疾病、血栓查因等角度进入第二阶段检查,但是在肺血管中心医生眼里,初步诊断已藏在了CTPA中。
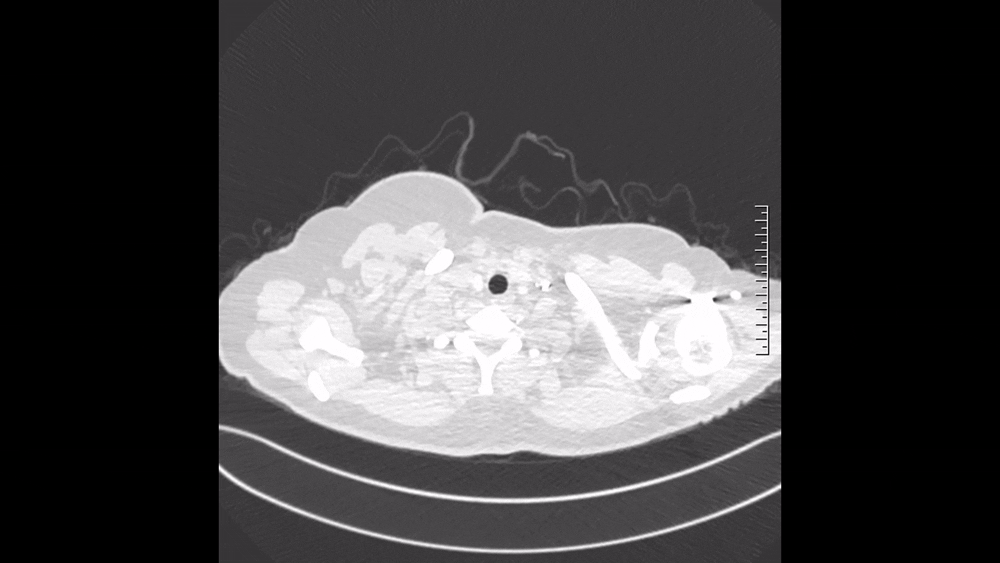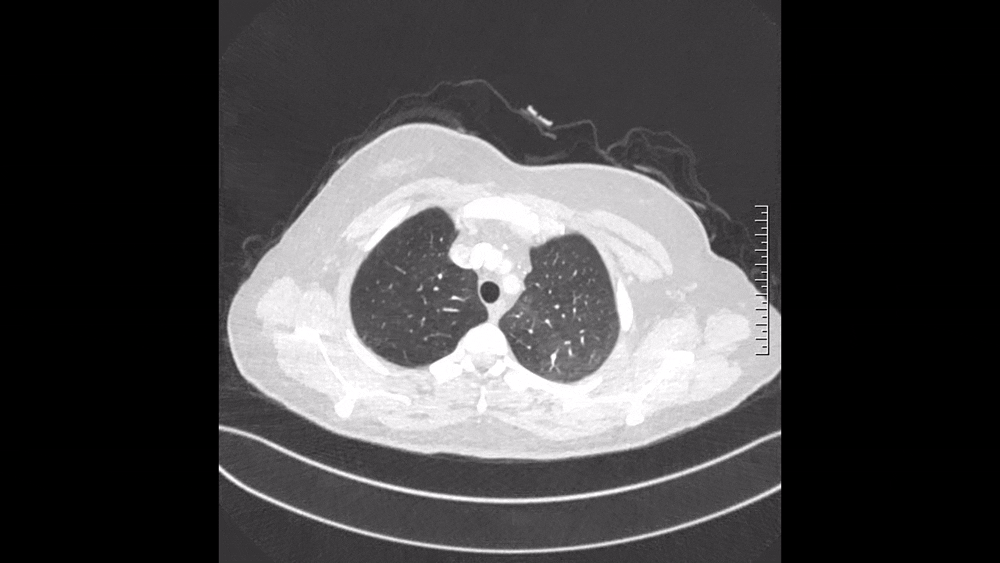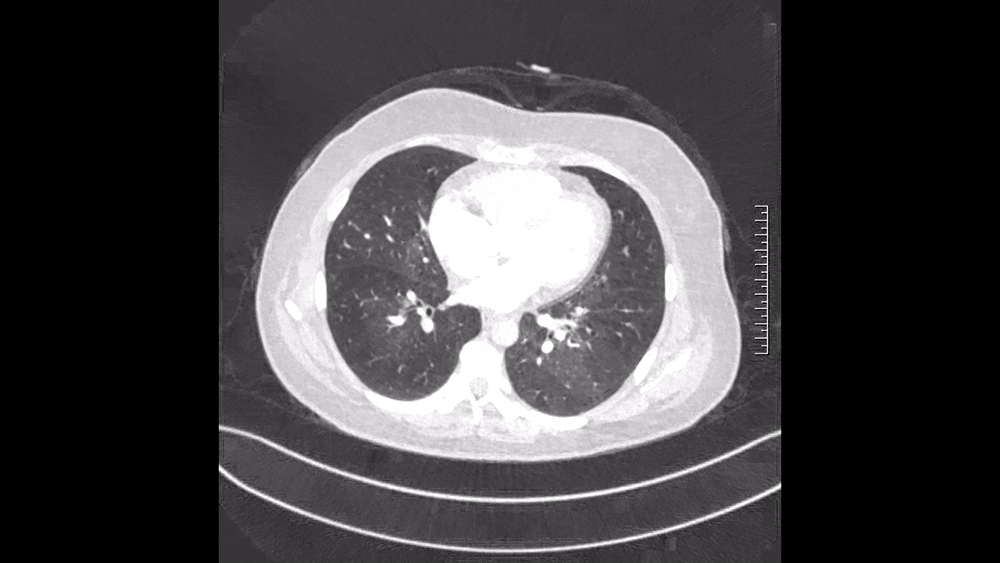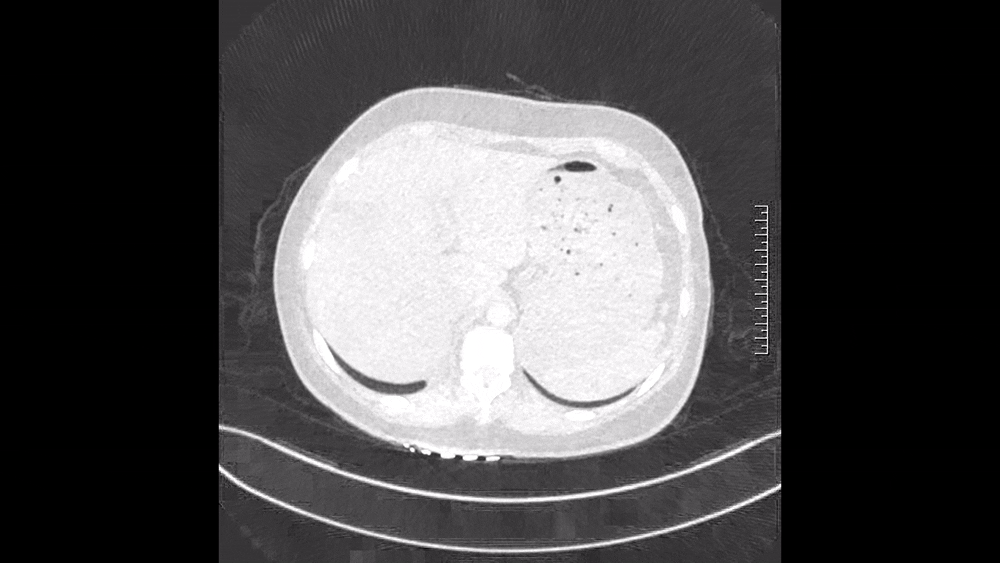
图3 2024.11.4 CTPA肺窗
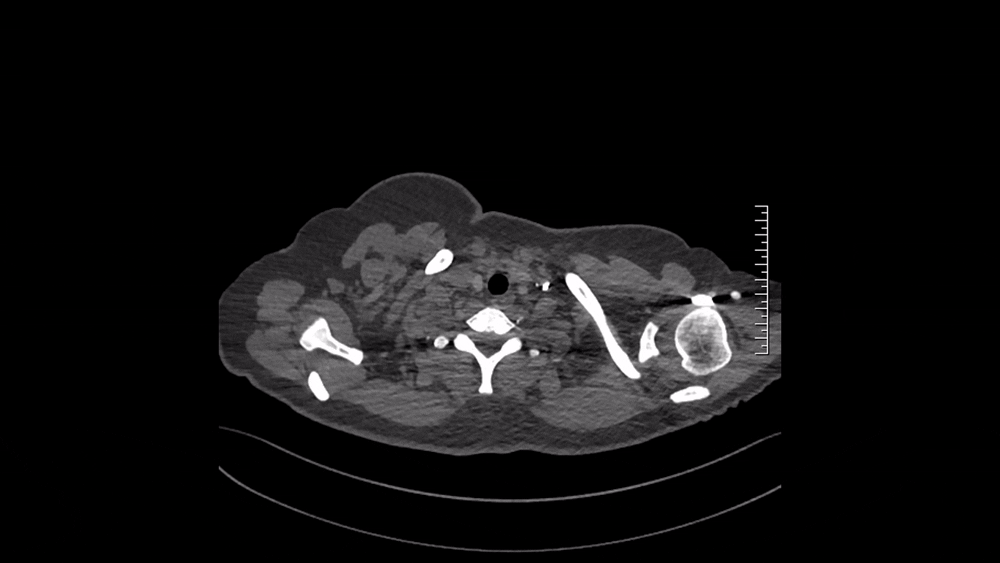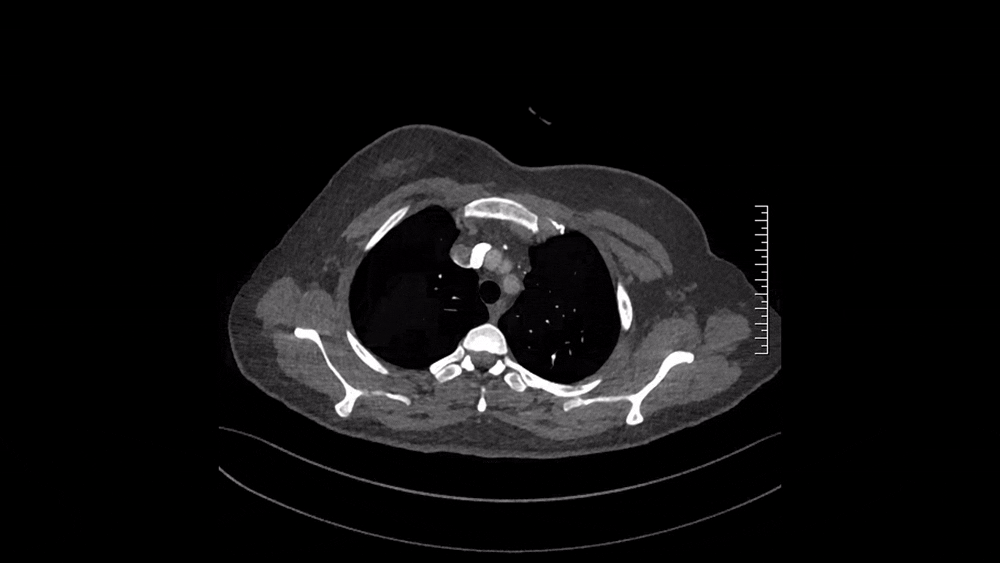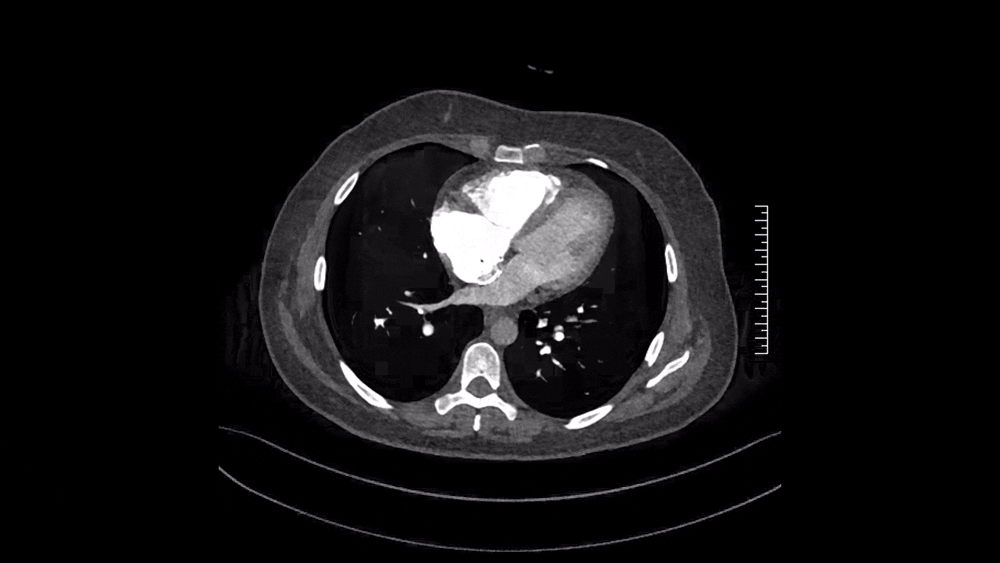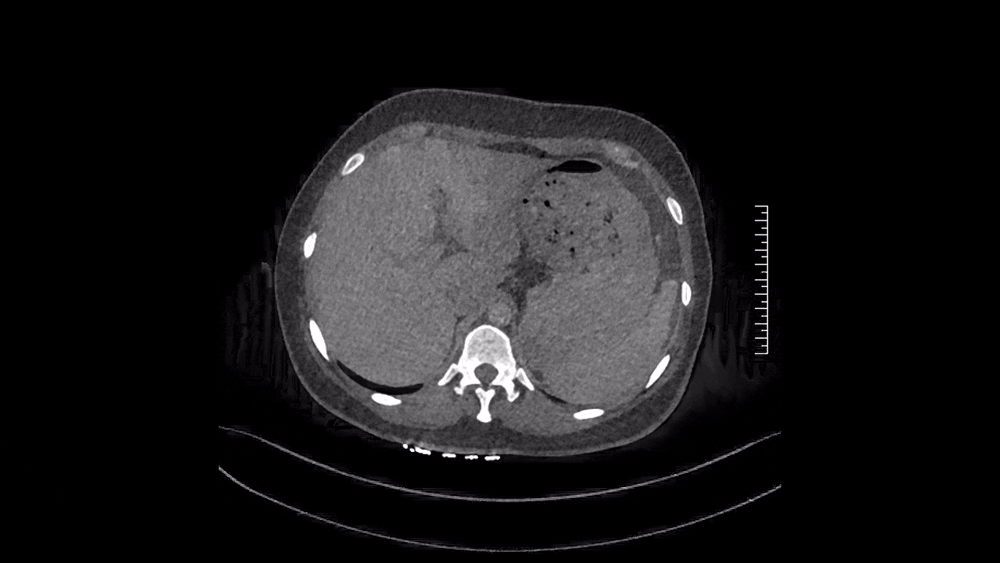
图4 2024.11.4 CTPA纵隔窗
仔细阅读CTPA:肺窗可见多发磨玻璃影,马赛克征象,这是肺血流灌注不均的表现(图3);纵隔窗可见肺动脉主干增粗,提示肺动脉压力升高;右肺上叶、中叶血管纹理稀疏,多个肺动脉亚段及分支(RA1、RA2、RA3、RA4、RA5、RA10、LA4、LA5为著)狭窄、闭塞病变,这些提示肺动脉慢性血栓表现(图4)。
图5 2024.8.31 头颈联合CTA扫及上肺,RA1、RA2、RA3多发狭窄、闭塞,右上肺血管纹理稀疏。
追问患者胸闷病史,患者诉2年余前出现活动后胸闷,因不从事体力劳动而未在意。再次回顾患者3月前心外科就诊时的头颈CTA(扫及双上肺),可见右肺上叶肺动脉及分支多发狭窄、闭塞(图5),经过3个月抗凝治疗,对比此次CTPA无明显变化。结合患者右心衰竭的临床表现,超声提示右心增大、三尖瓣关闭不全、肺动脉高压,拟诊慢性血栓栓塞性肺动脉高压(CTEPH)。
图6 2024.11.7 肺通气灌注显像
按照CTEPH诊断流程,进一步完善肺灌注显像(图6):右肺上叶、中叶,右肺下叶后基底段,左肺上叶舌段血流灌注减低/缺损。
图7 2024.11.12 右心导管检查报告
图8 2024.11.12 肺动脉造影(正位,左右45°斜位)
右心导管检查结果示(图7):mPAP 47/16(26)mmHg,CI 3.2L/min/m2,PVR 4.7WU,SvO2:51.3%。肺动脉造影可见(图8):肺动脉主干增粗,双侧肺动脉及其分支广泛狭窄、闭塞病变,远端血流差,以RA1、RA2、RA3、RA4、RA5、RA10、LA4、LA5、LA8为著。据此,CTEPH诊断明确。
CTEPH除了诊断,还要进行求因。中国人常见遗传性风险因素包括抗凝血酶缺乏、蛋白C缺乏或蛋白C抵抗、蛋白S缺乏等。获得性风险因素包括外科手术、创伤、骨折、因急性内科疾病住院治疗、恶性肿瘤、抗磷脂综合征等。此外,口服避孕药、雌激素类药物、抗肿瘤药物、三环类抗抑郁药,以及高龄、吸烟、肥胖、高同型半胱氨酸血症等因素同样增加血栓形成风险。
进一步完善血栓求因相关检查:
结缔组织病全套:ANA 1:100(±),余抗体阴性;类风湿关节炎抗体谱、ANCA抗体谱:未见异常;肿瘤标志物:未见异常;PET-CT:动脉代谢未见明显异常,未见肿瘤征象。
易栓症筛查:蛋白S活性 90.5%,蛋白C活性 52↓%,抗凝血酶III 89%,V因子活性 84.6%,VIII因子活性 163.3%,XI因子活性 54.7%,vWF活性 148%。
狼疮抗凝物检查:狼疮抗凝物筛选比率 2.12↑,狼疮抗凝物确诊比率 1.67↑,狼疮抗凝物归一化比率 1.27↑(校正后)。
抗磷脂抗体测定:抗心磷脂抗体IgG抗体 42.1↑ CU,抗心磷脂抗体IgA抗体 31.6↑ CU,抗心磷脂抗体IgM抗体 2.9 CU,抗β2糖蛋白1IgG抗体 6.4 CU,抗β2糖蛋白1IgA抗体 4.0 CU,抗β2糖蛋白1IgM抗体 1.1 CU。
抗磷脂综合征(APS)是一种以反复血管性血栓事件、复发性自然流产、血小板减少等为主要临床表现,伴有抗磷脂抗体谱持续中、高滴度阳性的自身免疫病。根据APS悉尼修订分类标准,本患者多次血栓事件(肺栓塞、脑梗死、左上肢静脉血栓),抗心磷脂抗体IgG抗体 42.1↑ CU,诊断APS。请风湿科会诊后加用糖皮质激素(泼尼松 30mg qd 每2周减5mg 减至15mg qd 维持)及免疫抑制剂(他克莫司胶囊 1mg bid 维持血药浓度5-10ng/ml)。
“一元论”诊断分析如下:APS并发血栓形成,2年前出现肺栓塞,未抗凝治疗进展为慢性血栓栓塞性肺动脉高压,继发右心增大、三尖瓣关闭不全、房间隔再次开放(右向左分流,代偿性),患者自觉症状不明显。1年前脑动脉血栓形成引起急性脑梗死,发现房缺行房间隔封堵,实质上是去除了右心减压通道,右向左分流减少,肺动脉血流量和右心负荷增加,加重了右心衰竭,导致胸闷加重。
患者肺动脉压力及肺血管阻力与呼吸困难的严重程度不匹配,呼吸困难是否还有其他因素参与?
讲述者:蒋天赐
患者经“曲前列尼尔+安立生坦+他达拉非”降肺动脉压、“左西孟旦”改善右心衰、利尿后,NT-proBNP下降至327↑pg/mL,右心导管测mPAP 26mmHg、PVR 4.7WU,但是患者仍存在较明显的呼吸困难,心功能III-IV级(WHO分级),6MWD:247米↓,肺动脉压力及肺血管阻力与呼吸困难的严重程度不匹配。患者呼吸困难是否还有其他原因?
呼吸困难按病因可分为肺源性呼吸困难、心源性呼吸困难、中毒性呼吸困难、血源性呼吸困难和神经精神性呼吸困难等。
1.肺源性呼吸困难:由呼吸道、肺、肺循环、胸膜、纵隔、胸廓及呼吸肌的各种疾病引起通气、换气功能障碍,导致缺氧和/或二氧化碳潴留,或因呼吸阻力增强,使呼吸有关感受器兴奋等。
2.心源性呼吸困难:见于各类心脏病引起左心或右心功能衰竭时,尤以左心功能衰竭时更为显著。大量心包积液也可出现呼吸困难。
3.中毒性呼吸困难:由呼吸中枢受毒物刺激或药物抑制所致,见于酸中毒、尿毒症、毒血症、化学毒物中毒及药物中毒等。
4.血源性呼吸困难:由红细胞携带氧减少或大出血休克刺激呼吸中枢等所致,见于重症贫血、休克、白血病及变性血红蛋白血症等。
5.神经精神性与肌病性呼吸困难:常因颅内压升高和供血减少而使呼吸中枢抑制,或神经肌肉麻痹致通气不足,以及心理因素等引起,见于脑部疾病(包括大面积脑梗死、脑出血等)、重症肌无力危象、格林(巴利综合征)和癔症等。
6.其他疾病所致呼吸困难:如大量腹水、气腹、腹内巨大肿瘤、妊娠后期、急性传染性疾病伴高热、肺出血性钩端螺旋体病、肺出血、肾炎综合征、中暑、高原病及移植肺等。
该患者无中毒性和神经精神性相关病史和体征,肺源性和心源性呼吸困难经积极治疗后,仍伴有难以解释的呼吸困难。患者存在重度贫血(Hb 52g/L),红细胞携氧能力下降可造成组织器官缺氧,引起代偿性呼吸、心率增快,加重心脏负荷和呼吸肌疲劳,出现劳力性呼吸困难。经过上述鉴别,我们认为患者呼吸困难难以纠正的原因,除了CTEPH引起的肺血管阻力增加和右心衰竭,还有重度贫血的因素。
2月内患者血红蛋白急剧下降约30g/L,期间无月经增多、黑便、咯血、呕血等出血表现……重度贫血原因如何?原发病APS能否解释?
讲述者:代灵灵
患者3月前我院心外科首次就诊时,血红蛋白(Hb)81g/L(图9),本次入院时Hb 52g/L,MCV 68.5↓fL,MCH 19.3↓pg,MCHC 283↓g/L,网织红细胞百分比3.3%↑,间断输悬浮红细胞2u后,血红蛋白改善不明显(57g/L)。自身免疫性溶血性贫血是APS常见分类标准外临床表现,但是患者无黄疸、尿色改变、血尿胆红素升高等溶血性贫血表现,血常规提示小细胞低色素性贫血。
引起小细胞低色素贫血的常见原因:(1)缺铁性贫血;(2)慢性病贫血;结合患者血清铁稍升高,铁蛋白升高,CRP正常,此两种疾病暂不符合诊断要求,可通过骨髓铁染色进行确认。(3)铁粒幼细胞性贫血;其机制为铁利用障碍,可表现为双相性贫血,外周血红细胞直方图显示单峰,暂不考虑,且患者拒绝骨穿,无法进一步鉴别。(4)珠蛋白生成障碍性贫血;为遗传基因缺陷致使珠蛋白链合成障碍的溶血性贫血,具有地域性,暂不考虑。
图9 血红蛋白变化趋势
患者贫血不能用常见的病因解释,我们再次回顾患者血红蛋白变化趋势(图9)。患者本次入院时血红蛋白(2024年10月30日)与我院首次就诊时(2024年8月29日)比较,2月内急剧下降约30g/L,期间无月经增多、黑便、咯血、呕血等出血表现。但是,患者2月前开始加用降肺动脉压药物,其中包括安立生坦,有没有可能是药物引起的贫血呢?
图10 BPA治疗前后肺血流变化
图11 BPA治疗后复查心脏超声
内皮素受体拮抗剂(包括安立生坦)常见不良反应包括贫血,目前尚不清楚安立生坦导致血红蛋白下降的原因,但它似乎不是由于出血或溶血所致。研究显示:与安慰剂相比,接受安立生坦治疗的患者在治疗结束时的血红蛋白与基线时相比平均下降8g/L,仅有7%的患者出现血红蛋白明显下降(与基线相比降低幅度>15%,并且绝对值低于正常值低限)。该患者血红蛋白显著下降(降低幅度36%),常见贫血原因不能解释,不排除药物导致的贫血。于11月7日停用安立生坦,同时申请输悬浮红细胞2u,4天后复查血常规,患者血红蛋白升高至91 g/L。对比1周前输红细胞2u血红蛋白升高不明显,停用安立生坦后输红细胞2u,患者血红蛋白迅速升高,再次印证了患者贫血原因可能是药物性。
患者贫血改善后,呼吸困难较前明显缓解,可以耐受肺动脉球囊扩张术(BPA)。我们团队先后多次为患者实施BPA治疗,术前术后对比可见肺动脉狭窄、闭塞明显改善(图10),复查心脏超声(图11),患者右心缩小至正常范围,三尖瓣开放正常,患者症状也明显改善,心功能I级,6MWD:432米,可从事正常体力活动。
程哲主任点评
本病例完整演绎了从识别核心病理生理(CTEPH),到追溯根本病因(APS),再到处理治疗并发症(药物性贫血),最终通过病因治疗与介入手段实现病理逆转的全程管理。
在面对复杂临床问题时,识别与确立核心矛盾至关重要。本病例以影像为切入点,快速进行CTEPH诊断和血栓求因,锁定根本病因(APS),实现了真正的“一元论”解释。同时还启示临床医生,加强肺动脉高压靶向治疗不良反应的监测意识。
专家介绍
程哲
从事专业:呼吸与危重症医学科,特别在肺栓塞与肺动脉高压,慢性气道病,感染性疾病,肺癌,间质性肺疾病,以及疑难杂症方面颇有造诣;郑州大学第一附属医院主任医师、教授,医学博士、硕士/博士研究生导师、博士后导师;郑州大学第一附属医院质控处处长;入选中原英才计划(育才系列)-中原医疗卫生领军人才;河南省优秀青年科技专家、河南省卫生科技创新型人才;河南省医学会内科学分会 主任委员;中华医学会内科学分会委员;河南省肺栓塞与肺动脉高压诊疗中心 主任;河南省静脉血栓栓塞症诊疗质量控制中心 主任委员;中华医学会呼吸分会基层学组委员;中国医师协会肺栓塞与肺血管病工作委员会委员;河南省医学会呼吸分会副主任委员;中国康复医学会呼吸康复慢病学组副组长;河南省呼吸与危重症学会肺栓塞与肺血管病分会主任委员。
代灵灵
郑州大学第一附属医院呼吸与危重症五科主治医师,博士。主要研究方向:肺栓塞与肺血管疾病。学术兼职:河南省医学会呼吸分会青年委员,河南省医学会呼吸分会感染学组委员,河南省呼吸与危重症学会肺栓塞与肺血管病分会青委会副主委兼秘书,河南省医学会呼吸病学分会第一届慢阻肺联盟秘书。
李鹏飞
医学博士,郑州大学第一附属医院呼吸与危重症医学科主治医师,河南省呼吸与危重症学会肺栓塞及肺血管病分会青年委员会秘书。2013年毕业于郑州大学获医学学士学位;2016年硕士毕业于郑州大学第一附属医院;2019年博士毕业于中南大学湘雅医院。目前参与国家自然科学基金4项,以第一作者发表SCI论文3篇,以参与作者发表SCI论文16篇,获得国家实用新型专利2项。研究方向为:慢性气道疾病、肺血管病和急性中枢神经系统损伤后肺炎的临床与基础研究。
王羽
医学博士,郑州大学第一附属医院呼吸与危重症医学科主治医师,河南省呼吸与危重症学会肺栓塞及肺血管病分会青年委员会秘书。2013年毕业于郑州大学获医学学士学位;2016年硕士毕业于四川大学华西医院;2019年博士毕业于四川大学华西医院。曾参与国家“十二五”传染病防治重大专项、多项国家自然科学基金委面上项目,主持国家自然科学基金委青年基金1项,以第一作者发表SCI论文6篇,另以参与作者发表SCI论文20余篇。研究方向为:结核病与抗结核药物性肝损害的分子遗传,慢性气道疾病、肺血管病的发病机制和临床应用。
蒋天赐
郑大一附院呼吸与危重症医学五科主治医师,医学硕士;河南省医学会呼吸病学分会第一届慢阻肺联盟秘书;河南省呼吸与危重症学会肺栓塞与肺血管病分会青年委员。主持及参与科研项目5项,发表论文10余篇,获得河南省教育厅及卫计委科技成果奖一等奖3项。
* 文章仅供医疗卫生相关从业者阅读参考
本文完
采写编辑:冬雪凝;责编:Jerry



